ژنتیک مطالعه ژن ها ، تنوع ژنتیکی و وراثت در موجودات است . [1] [2] [3] این شاخه مهم در زیست شناسی است زیرا وراثت برای تکامل موجودات حیاتی است . گرگور مندل ، یک راهب آگوستینی موراویایی که در قرن نوزدهم در برنو کار می کرد ، اولین کسی بود که ژنتیک را به طور علمی مطالعه کرد. مندل "وراثت صفت" را مطالعه کرد، الگوهایی در نحوه انتقال صفات از والدین به فرزندان در طول زمان. او مشاهده کرد که موجودات زنده (گیاهان نخودفرنگی) صفات را از طریق "واحدهای وراثت" مجزا به ارث می برند. این اصطلاح که هنوز هم امروزه مورد استفاده قرار می گیرد، یک تعریف تا حدی مبهم از چیزی است که به عنوان ژن شناخته می شود.
وراثت صفت و مکانیسم های وراثت مولکولی ژن ها هنوز از اصول اولیه ژنتیک در قرن بیست و یکم هستند، اما ژنتیک مدرن برای مطالعه عملکرد و رفتار ژن ها گسترش یافته است. ساختار و عملکرد ژن، تنوع و توزیع در بافت سلول ، ارگانیسم (به عنوان مثال تسلط )، و در بافت یک جمعیت مورد مطالعه قرار می گیرد. ژنتیک باعث ایجاد تعدادی زیرشاخه از جمله ژنتیک مولکولی ، اپی ژنتیک و ژنتیک جمعیت شده است . ارگانیسمهای مورد مطالعه در حوزه وسیع، دامنههای حیات ( باستانها ، باکتریها و یوکاریا ) را در بر میگیرند.
فرآیندهای ژنتیکی در ترکیب با محیط و تجربیات یک ارگانیسم برای تأثیرگذاری بر رشد و رفتار عمل می کنند که اغلب به عنوان طبیعت در مقابل پرورش از آن یاد می شود . محیط درون سلولی یا خارج سلولی یک سلول یا موجود زنده ممکن است رونویسی ژن را افزایش یا کاهش دهد. یک مثال کلاسیک، دو دانه ذرت از نظر ژنتیکی یکسان است، یکی در آب و هوای معتدل و دیگری در آب و هوای خشک (بدون آبشار یا باران کافی). در حالی که ارتفاع متوسطی که دو ساقه ذرت می توانند به آن رشد کنند از نظر ژنتیکی تعیین می شود، ساقه ذرت در آب و هوای خشک به دلیل کمبود آب و مواد مغذی در محیط، تنها تا نصف ارتفاع آن در آب و هوای معتدل رشد می کند.
واژه ژنتیک از واژه یونانی باستان γενετικός genetikos به معنای "تناسب"/"زاینده" گرفته شده است، که به نوبه خود از γένεσις genesis به معنای "منشا" گرفته شده است. [4] [5] [6]
مشاهده این که موجودات زنده صفاتی را از والدین خود به ارث می برند از دوران ماقبل تاریخ برای بهبود گیاهان و حیوانات از طریق اصلاح انتخابی استفاده می شده است . [7] [8] علم مدرن ژنتیک، به دنبال درک این فرآیند، با کار گرگور مندل، برادر آگوستینی ، در اواسط قرن 19 آغاز شد. [9]

قبل از مندل، Imre Festetics ، یک نجیب مجارستانی ، که قبل از مندل در کوسگ زندگی می کرد، اولین کسی بود که کلمه "ژنتیک" را در بافت ارثی به کار برد و به عنوان اولین ژنتیک دان شناخته می شود. او در کار خود قوانین ژنتیکی طبیعت (Die genetischen Gesetze der Natur، 1819) چندین قانون وراثت زیستی را شرح داد . [10] قانون دوم او همان است که مندل منتشر کرد. [11] در قانون سوم خود، او اصول اولیه جهش را توسعه داد (او را می توان پیشرو هوگو دو وریس در نظر گرفت ). [12] Festetics استدلال کرد که تغییرات مشاهده شده در نسل حیوانات مزرعه، گیاهان، و انسان نتیجه قوانین علمی است. [13] فستتیک ها به طور تجربی استنباط کردند که موجودات ویژگی های خود را به ارث می برند، نه کسب آنها. او صفات مغلوب و تنوع ذاتی را با این فرض که صفات نسلهای گذشته میتوانند بعداً ظاهر شوند و ارگانیسمها میتوانند فرزندانی با ویژگیهای متفاوت تولید کنند، تشخیص داد. [14] این مشاهدات مقدمه مهمی برای نظریه وراثت ذرهای مندل را نشان میدهد تا آنجا که با ارائه یک مبنای نظری اساسی برای ژنتیک در قرن بیستم، انتقال وراثت از جایگاه آن به عنوان اسطوره به یک رشته علمی را نشان میدهد. [10] [15]

تئوری های دیگر وراثت قبل از کار مندل بود. یک نظریه رایج در قرن نوزدهم، که توسط چارلز داروین در سال 1859 در مورد منشاء گونه ها تلویحا شد، ترکیب وراثت بود : این ایده که افراد ترکیبی صاف از صفات را از والدین خود به ارث می برند. [16] کار مندل نمونههایی را ارائه میکند که در آن صفات قطعاً پس از هیبریداسیون با هم ترکیب نشدهاند، و نشان میدهد که صفات توسط ترکیبی از ژنهای متمایز به جای یک ترکیب پیوسته تولید میشوند. اختلاط صفات در نتاج اکنون با عمل چندین ژن با اثرات کمی توضیح داده می شود . نظریه دیگری که در آن زمان مورد حمایت قرار گرفت، توارث ویژگی های اکتسابی بود : این باور که افراد صفاتی را به ارث می برند که توسط والدینشان تقویت شده است. این نظریه (که معمولاً با ژان باپتیست لامارک مرتبط است ) اکنون به اشتباه شناخته شده است - تجربیات افراد بر ژن هایی که به فرزندان خود منتقل می کنند تأثیر نمی گذارد. [17] نظریههای دیگر شامل پانژنز داروین (که هم جنبههای اکتسابی و هم جنبههای موروثی داشت) و فرمولبندی مجدد پانژنز توسط فرانسیس گالتون بهعنوان ذرهای و ارثی بود. [18]

ژنتیک مدرن با مطالعات مندل در مورد ماهیت وراثت در گیاهان آغاز شد. مندل در مقاله خود " Versuche über Pflanzenhybriden " (" آزمایش هایی در مورد هیبریداسیون گیاهان ") که در سال 1865 به Naturforschender Verein (انجمن تحقیقات در طبیعت) در برنو ارائه شد ، الگوهای وراثتی برخی از صفات را در گیاهان نخود فرنگی ردیابی کرد و آنها را به صورت ریاضی توصیف کرد. اگرچه این الگوی وراثت فقط برای چند ویژگی قابل مشاهده بود، کار مندل نشان داد که وراثت جزئی است نه اکتسابی، و الگوهای وراثت بسیاری از صفات را می توان از طریق قوانین و نسبت های ساده توضیح داد. [19]
اهمیت کار مندل تا سال 1900، پس از مرگ او، زمانی که هوگو دو وریس و دیگر دانشمندان تحقیقات او را دوباره کشف کردند، درک گسترده ای پیدا نکرد. ویلیام بیتسون ، یکی از طرفداران کار مندل، کلمه ژنتیک را در سال 1905 ابداع کرد. [20] [21] صفت ژنتیک ، که از کلمه یونانی پیدایش — γένεσις، "منشاء" مشتق شده است، پیش از اسم است و برای اولین بار در معنای بیولوژیکی استفاده شد. در سال 1860. [22] بیتسون هر دو به عنوان یک مربی عمل کرد و به طور قابل توجهی توسط کار دانشمندان دیگر از کالج نیونهام در کمبریج، به ویژه کار بکی ساندرز ، نورا داروین بارلو ، و موریل ویلدیل اونسلو ، کمک شد . [23] بیتسون استفاده از کلمه ژنتیک را برای توصیف مطالعه وراثت در سخنرانی افتتاحیه خود در سومین کنفرانس بین المللی هیبریداسیون گیاهان در لندن در سال 1906 رایج کرد. [24]
پس از کشف مجدد کار مندل، دانشمندان سعی کردند تعیین کنند که کدام مولکول ها در سلول مسئول وراثت هستند. در سال 1900، نتی استیونز مطالعه کرم آرد را آغاز کرد. [25] در طول 11 سال بعد، او کشف کرد که زنان فقط کروموزوم X و مردان دارای هر دو کروموزوم X و Y هستند. [25] او توانست به این نتیجه برسد که جنسیت یک عامل کروموزومی است و توسط مرد تعیین می شود. [25] در سال 1911، توماس هانت مورگان بر اساس مشاهدات مربوط به جهش چشم سفید مرتبط با جنسیت در مگس میوه ، استدلال کرد که ژن ها روی کروموزوم ها هستند . [26] در سال 1913، شاگرد او آلفرد استورتوانت از پدیده پیوند ژنتیکی استفاده کرد تا نشان دهد که ژن ها به صورت خطی روی کروموزوم قرار گرفته اند. [27]
اگرچه ژنها بر روی کروموزومها وجود دارند، کروموزومها هم از پروتئین و هم از DNA تشکیل شدهاند و دانشمندان نمیدانستند کدام یک از این دو عامل وراثت است. در سال 1928 ، فردریک گریفیث پدیده دگرگونی را کشف کرد : باکتری های مرده می توانند مواد ژنتیکی را برای "تبدیل" سایر باکتری های هنوز زنده منتقل کنند. شانزده سال بعد، در سال 1944، آزمایش Avery-MacLeod-McCarty DNA را به عنوان مولکول مسئول تبدیل شناسایی کرد. [28] نقش هسته به عنوان مخزن اطلاعات ژنتیکی در یوکاریوت ها توسط هامرلینگ در سال 1943 در کار خود بر روی جلبک تک سلولی استابولاریا مشخص شد . [29] آزمایش هرشی-چیز در سال 1952 تأیید کرد که DNA (به جای پروتئین) ماده ژنتیکی ویروسهایی است که باکتریها را آلوده میکنند و شواهد بیشتری را ارائه میدهد که DNA مولکول مسئول وراثت است. [30]
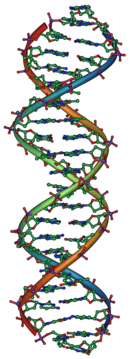
جیمز واتسون و فرانسیس کریک در سال 1953 ساختار DNA را با استفاده از کار کریستالوگرافی اشعه ایکس روزالیند فرانکلین و موریس ویلکینز تعیین کردند که نشان میداد DNA ساختاری مارپیچ دارد (یعنی به شکل یک پیچ در بسته). [31] [32] مدل دو مارپیچ آنها دارای دو رشته DNA با نوکلئوتیدها به سمت داخل بود، که هر یک با یک نوکلئوتید مکمل در رشته دیگر مطابقت دارد تا شبیه به پلههایی روی یک نردبان پیچ خورده باشد. [33] این ساختار نشان داد که اطلاعات ژنتیکی در توالی نوکلئوتیدها در هر رشته DNA وجود دارد. این ساختار همچنین یک روش ساده را برای همانندسازی پیشنهاد میکند : اگر رشتهها از هم جدا شوند، میتوان رشتههای شریک جدیدی را برای هر کدام بر اساس دنباله رشته قدیمی بازسازی کرد. این خاصیت چیزی است که به DNA ماهیت نیمه محافظه کارانه می بخشد که در آن یک رشته DNA جدید از یک رشته اصلی است. [34]
اگرچه ساختار DNA نشان میدهد که وراثت چگونه کار میکند، اما هنوز مشخص نیست که DNA چگونه بر رفتار سلولها تأثیر میگذارد. در سالهای بعد، دانشمندان تلاش کردند تا بفهمند DNA چگونه فرآیند تولید پروتئین را کنترل میکند . [35] کشف شد که سلول از DNA به عنوان الگویی برای ایجاد RNA پیام رسان منطبق استفاده می کند ، مولکول هایی با نوکلئوتیدهای بسیار شبیه به DNA. توالی نوکلئوتیدی یک RNA پیام رسان برای ایجاد یک توالی اسید آمینه در پروتئین استفاده می شود. این ترجمه بین توالی های نوکلئوتیدی و توالی اسید آمینه به عنوان کد ژنتیکی شناخته می شود . [36]
با درک مولکولی تازه کشف شده از وراثت، انفجاری از تحقیقات به وجود آمد. [37] یک نظریه قابل توجه از توموکو اوهتا در سال 1973 با اصلاح او در نظریه خنثی تکامل مولکولی از طریق انتشار نظریه تقریباً خنثی تکامل مولکولی بوجود آمد . در این نظریه، اوهتا بر اهمیت انتخاب طبیعی و محیط برای سرعت وقوع تکامل ژنتیکی تاکید کرد . [38] یکی از پیشرفت های مهم، توالی یابی DNA با پایان زنجیره در سال 1977 توسط فردریک سانگر بود . این فناوری به دانشمندان اجازه می دهد تا توالی نوکلئوتیدی یک مولکول DNA را بخوانند. [39] در سال 1983، Kary Banks Mullis واکنش زنجیرهای پلیمراز را توسعه داد و راهی سریع برای جداسازی و تقویت بخش خاصی از DNA از یک مخلوط ارائه کرد. [40] تلاشهای پروژه ژنوم انسانی ، وزارت انرژی، NIH، و تلاشهای خصوصی موازی توسط Celera Genomics منجر به تعیین توالی ژنوم انسان در سال 2003 شد. [41] [42]
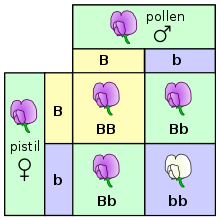
در بنیادی ترین سطح، وراثت در موجودات با انتقال واحدهای ارثی گسسته، به نام ژن ، از والدین به فرزندان اتفاق می افتد. [43] این خاصیت اولین بار توسط گرگور مندل مشاهده شد که جداسازی صفات وراثتی در گیاهان نخود را مورد مطالعه قرار داد ، به عنوان مثال نشان داد که گلهای یک گیاه یا بنفش یا سفید هستند – اما هرگز حد واسط بین این دو رنگ نیستند. نسخههای مجزای همان ژن که ظاهر ارثی (فنوتیپها) را کنترل میکنند، آلل نامیده میشوند . [19] [44]
در مورد نخود که یک گونه دیپلوئیدی است ، هر گیاه جداگانه دارای دو نسخه از هر ژن است که یک نسخه از هر والدین به ارث می رسد. [45] بسیاری از گونه ها، از جمله انسان، این الگوی توارث را دارند. ارگانیسم های دیپلوئیدی با دو نسخه از یک آلل یک ژن در آن مکان ژنی هموزیگوت نامیده می شوند، در حالی که ارگانیسم هایی با دو آلل متفاوت از یک ژن معین هتروزیگوت نامیده می شوند . مجموعه آللهای موجود برای یک ارگانیسم را ژنوتیپ آن و صفات قابل مشاهده موجود را فنوتیپ می نامند . هنگامی که ارگانیسم ها در یک ژن هتروزیگوت هستند، اغلب یک آلل غالب نامیده می شود زیرا کیفیت آن بر فنوتیپ ارگانیسم غالب است، در حالی که آلل دیگر مغلوب نامیده می شود زیرا کیفیت های آن کاهش می یابد و مشاهده نمی شود. برخی از آلل ها تسلط کامل ندارند و در عوض با بیان یک فنوتیپ میانی غلبه ناقص دارند یا با بیان هر دو آلل به یکباره غلبه دارند . [46]
هنگامی که یک جفت ارگانیسم از طریق جنسی تولید مثل می کنند ، فرزندان آنها به طور تصادفی یکی از دو آلل را از هر یک از والدین به ارث می برند. این مشاهدات مربوط به وراثت گسسته و جداسازی آلل ها در مجموع به عنوان قانون اول مندل یا قانون تفکیک شناخته می شوند. با این حال، احتمال دریافت یک ژن نسبت به ژن دیگر می تواند به دلیل ژن های غالب، مغلوب، هموزیگوت یا هتروزیگوت تغییر کند. برای مثال، مندل دریافت که اگر با ارگانیسمهای هتروزیگوت عبور کنید، شانس شما برای بدست آوردن صفت غالب 3:1 است. متخصص ژنتیک واقعی احتمالات را با استفاده از احتمالات نظری، احتمالات تجربی، قانون محصول، قانون جمع و غیره مطالعه و محاسبه می کند. [47]

متخصصان ژنتیک از نمودارها و نمادها برای توصیف وراثت استفاده می کنند. یک ژن با یک یا چند حرف نشان داده می شود. اغلب از نماد "+" برای علامت گذاری آلل معمولی و غیر جهش یافته برای یک ژن استفاده می شود. [48]
در آزمایشهای لقاح و پرورش (و بهویژه هنگام بحث درباره قوانین مندل)، والدین بهعنوان نسل «P» و فرزندان بهعنوان نسل «F1» (نخستین فرزندخواندگی) شناخته میشوند. هنگامی که فرزندان F1 با یکدیگر جفت گیری می کنند، به فرزندان "F2" (دومین فرزندی) می گویند. یکی از نمودارهای متداول که برای پیشبینی نتیجه صلاحیت استفاده میشود، مربع پونت است . [49]
هنگام مطالعه بیماری های ژنتیکی انسان، متخصصان ژنتیک اغلب از نمودارهای شجره نامه برای نشان دادن وراثت صفات استفاده می کنند. [50] این نمودارها وراثت یک صفت را در یک شجره نامه ترسیم می کنند.

ارگانیسم ها هزاران ژن دارند و در ارگانیسم های تولید مثل جنسی، این ژن ها به طور کلی مستقل از یکدیگر دسته بندی می شوند. این بدان معناست که وراثت یک آلل برای رنگ نخودی زرد یا سبز با وراثت آلل های گل های سفید یا بنفش ارتباطی ندارد. این پدیده که به عنوان " قانون دوم مندل " یا "قانون مجموعه مستقل" شناخته میشود، به این معنی است که آللهای ژنهای مختلف بین والدین در هم میآیند تا فرزندانی با ترکیبهای مختلف ایجاد کنند. ژن های مختلف اغلب برای تأثیرگذاری بر یک صفت با هم تعامل دارند. به عنوان مثال، در مریم چشم آبی ( Omphalodes verna )، ژنی با آلل هایی وجود دارد که رنگ گل ها را تعیین می کند: آبی یا سرخابی. با این حال، ژن دیگری کنترل می کند که آیا گل ها اصلاً رنگ دارند یا سفید هستند. وقتی گیاهی دو نسخه از این آلل سفید داشته باشد، گلهایش سفید هستند - صرف نظر از اینکه ژن اول دارای آللهای آبی یا سرخابی است. این برهمکنش بین ژنها اپیستازیس نامیده میشود که ژن دوم نسبت به ژن اول اپیستاتیک است. [51]
بسیاری از صفات ویژگیهای مجزا نیستند (مثلاً گلهای بنفش یا سفید)، بلکه در عوض ویژگیهای پیوسته هستند (مانند قد انسان و رنگ پوست ). این صفات پیچیده محصول بسیاری از ژن ها هستند. [52] تأثیر این ژن ها، به درجات مختلف، توسط محیطی که یک ارگانیسم تجربه کرده است، واسطه می شود. درجه ای که ژن های یک موجود زنده در ایجاد یک صفت پیچیده نقش دارند، وراثت پذیری نامیده می شود . [53] اندازهگیری وراثتپذیری یک صفت نسبی است - در یک محیط متغیرتر، محیط تأثیر بیشتری بر تنوع کلی صفت دارد. به عنوان مثال، قد انسان یک ویژگی با علل پیچیده است. وراثت پذیری آن در ایالات متحده 89٪ است. با این حال، در نیجریه، جایی که مردم دسترسی متغیرتری به تغذیه خوب و مراقبت های بهداشتی را تجربه می کنند ، قد تنها 62 درصد وراثت پذیری دارد. [54]

اساس مولکولی ژن ها دی اکسی ریبونوکلئیک اسید (DNA) است. DNA از دئوکسی ریبوز (مولکول قند)، یک گروه فسفات و یک باز (گروه آمین) تشکیل شده است . چهار نوع باز وجود دارد: آدنین (A)، سیتوزین (C)، گوانین (G) و تیمین (T). فسفات ها با قندها پیوندهای فسفودی استری ایجاد می کنند تا ستون فقرات فسفات-شکر بلندی ایجاد کنند. پایه ها به طور خاص با هم (T&A، C&G) بین دو ستون فقرات جفت می شوند و مانند پله های یک نردبان می شوند. بازها، فسفات ها و قندها با هم یک نوکلئوتید می سازند که به هم متصل می شود و زنجیره های بلند DNA را می سازد. [55] اطلاعات ژنتیکی در توالی این نوکلئوتیدها وجود دارد و ژن ها به صورت امتدادی از توالی در امتداد زنجیره DNA وجود دارند. [56] این زنجیرهها به یک ساختار مارپیچ دوتایی میپیچند و به دور پروتئینهایی به نام هیستون میپیچند که پشتیبانی ساختاری را فراهم میکنند. DNA پیچیده شده در اطراف این هیستون ها کروموزوم نامیده می شود. [57] ویروس ها گاهی از مولکول RNA مشابه به جای DNA به عنوان ماده ژنتیکی خود استفاده می کنند. [58]
DNA معمولاً به صورت یک مولکول دو رشته ای وجود دارد که به شکل یک مارپیچ دوتایی پیچیده شده است . هر نوکلئوتید در DNA ترجیحاً با نوکلئوتید شریک خود در رشته مخالف جفت میشود: A با T جفت میشود و C با G جفت میشود. بنابراین، در شکل دو رشتهای خود، هر رشته به طور مؤثر حاوی تمام اطلاعات لازم است، که با رشته شریک خود اضافی است. این ساختار DNA مبنای فیزیکی برای وراثت است: همانندسازی DNA اطلاعات ژنتیکی را با تقسیم رشته ها و استفاده از هر رشته به عنوان الگویی برای سنتز یک رشته شریک جدید تکرار می کند. [59]

ژن ها به صورت خطی در امتداد زنجیره های بلند توالی های جفت باز DNA قرار گرفته اند. در باکتری ها ، هر سلول معمولاً حاوی یک ژنوفور دایره ای منفرد است ، در حالی که موجودات یوکاریوتی (مانند گیاهان و حیوانات) DNA خود را در کروموزوم های خطی متعددی مرتب می کنند. این رشته های DNA اغلب بسیار طولانی هستند. به عنوان مثال، بزرگترین کروموزوم انسان حدود 247 میلیون جفت باز طول دارد. [60] DNA یک کروموزوم با پروتئین های ساختاری مرتبط است که دسترسی به DNA را سازماندهی، فشرده و کنترل می کند و ماده ای به نام کروماتین را تشکیل می دهد . در یوکاریوتها، کروماتین معمولاً از نوکلئوزومها ، بخشهایی از DNA که در اطراف هستههای پروتئینهای هیستون زخم شدهاند، تشکیل شده است . [61] مجموعه کاملی از مواد ارثی در یک موجود زنده (معمولاً توالیهای DNA ترکیبی همه کروموزومها) ژنوم نامیده میشود .
DNA اغلب در هسته سلول ها یافت می شود، اما روث ساگر در کشف ژن های غیر کروموزومی که در خارج از هسته یافت می شوند کمک کرد. [62] در گیاهان، اینها اغلب در کلروپلاست ها و در سایر موجودات، در میتوکندری یافت می شوند. [62] این ژنهای غیرکروموزومی هنوز میتوانند توسط هر یک از طرفین در تولید مثل جنسی منتقل شوند و آنها ویژگیهای ارثی مختلفی را کنترل میکنند که تکثیر میشوند و در طول نسلها فعال میمانند. [62]
در حالی که موجودات هاپلوئید فقط یک کپی از هر کروموزوم دارند، بیشتر حیوانات و بسیاری از گیاهان دیپلوئید هستند ، که شامل دو نسخه از هر کروموزوم و بنابراین دو نسخه از هر ژن است. دو آلل یک ژن بر روی جایگاه های یکسان دو کروموزوم همولوگ قرار دارند که هر آلل از یک والدین متفاوت به ارث رسیده است. [45]
بسیاری از گونه ها دارای کروموزوم های جنسی هستند که جنسیت هر موجود زنده را تعیین می کنند. [63] در انسان و بسیاری از حیوانات دیگر، کروموزوم Y حاوی ژنی است که باعث ایجاد ویژگیهای خاص مردانه میشود. در تکامل، این کروموزوم بیشتر محتوای خود و همچنین بیشتر ژن های خود را از دست داده است، در حالی که کروموزوم X شبیه کروموزوم های دیگر است و حاوی ژن های زیادی است. همانطور که گفته شد، مری فرانسیس لیون کشف کرد که در طول تولیدمثل غیرفعال شدن کروموزوم X وجود دارد تا از انتقال دو برابر ژن به فرزندان جلوگیری شود. [64] کشف لیون منجر به کشف بیماری های مرتبط با X شد. [64]

هنگامی که سلول ها تقسیم می شوند، ژنوم کامل آنها کپی می شود و هر سلول دختر یک نسخه را به ارث می برد. این فرآیند که میتوز نامیده می شود ، ساده ترین شکل تولید مثل است و اساس تولید مثل غیرجنسی است. تولیدمثل غیرجنسی می تواند در موجودات چند سلولی نیز اتفاق بیفتد و فرزندانی تولید کنند که ژنوم خود را از یک والد به ارث می برند. فرزندانی که از نظر ژنتیکی با والدین خود یکسان هستند، کلون نامیده می شوند . [65]
ارگانیسم های یوکاریوتی اغلب از تولید مثل جنسی برای تولید فرزندانی استفاده می کنند که حاوی ترکیبی از مواد ژنتیکی است که از دو والدین مختلف به ارث رسیده است. فرآیند تولیدمثل جنسی به طور متناوب بین فرم هایی که حاوی نسخه های منفرد از ژنوم ( هاپلوئید ) و دو نسخه ( دیپلوئید ) هستند، می باشد. [45] سلولهای هاپلوئید با ترکیب و ترکیب مواد ژنتیکی یک سلول دیپلوئیدی با کروموزومهای جفتی ایجاد میکنند. ارگانیسمهای دیپلوئید با تقسیم، بدون تکثیر DNA، هاپلوئیدها را تشکیل میدهند تا سلولهای دختری ایجاد کنند که به طور تصادفی یکی از هر جفت کروموزوم را به ارث میبرند. بیشتر حیوانات و بسیاری از گیاهان در بیشتر طول عمر خود دیپلوئید هستند و شکل هاپلوئید به گامت های تک سلولی مانند اسپرم یا تخمک کاهش می یابد . [66]
اگرچه باکتری ها از روش هاپلوئید/دیپلوئید تولید مثل جنسی استفاده نمی کنند، اما باکتری ها روش های زیادی برای به دست آوردن اطلاعات ژنتیکی جدید دارند. برخی از باکتریها میتوانند تحت کونژوگه قرار بگیرند و یک قطعه دایرهای کوچک از DNA را به باکتری دیگری منتقل کنند. [67] باکتری ها همچنین می توانند قطعات DNA خام موجود در محیط را بگیرند و آنها را در ژنوم خود ادغام کنند، پدیده ای که به عنوان تبدیل شناخته می شود . [68] این فرآیندها منجر به انتقال افقی ژن ، انتقال قطعات اطلاعات ژنتیکی بین ارگانیسمهایی میشود که در غیر این صورت نامرتبط هستند. تبدیل طبیعی باکتریایی در بسیاری از گونه های باکتریایی رخ می دهد و می تواند به عنوان یک فرآیند جنسی برای انتقال DNA از یک سلول به سلول دیگر (معمولاً از همان گونه) در نظر گرفته شود. [69] دگرگونی نیاز به عمل چندین محصول ژن باکتریایی دارد و به نظر میرسد عملکرد تطبیقی اولیه آن ترمیم آسیبهای DNA در سلول گیرنده باشد. [69]

ماهیت دیپلوئید کروموزوم ها به ژن های روی کروموزوم های مختلف اجازه می دهد تا به طور مستقل از جفت همولوگ خود در طول تولید مثل جنسی که در آن گامت هاپلوئید تشکیل می شود جدا شوند. به این ترتیب ترکیبات جدیدی از ژن ها می تواند در فرزندان یک جفت جفت گیری رخ دهد. ژنهای روی یک کروموزوم از نظر تئوری هرگز دوباره ترکیب نمیشوند. با این حال، آنها از طریق فرآیند سلولی متقاطع کروموزومی انجام می دهند . در طول تقاطع، کروموزومها بخشهایی از DNA را مبادله میکنند و به طور موثر آللهای ژنی را بین کروموزومها به هم میریزند. [70] این فرآیند متقاطع کروموزومی به طور کلی در طول میوز رخ می دهد ، مجموعه ای از تقسیمات سلولی که سلول های هاپلوئید را ایجاد می کند. به نظر می رسد نوترکیبی میوز ، به ویژه در یوکاریوت های میکروبی ، عملکرد تطبیقی ترمیم آسیب های DNA را انجام می دهد. [69]
اولین تظاهرات سیتولوژیک متقاطع توسط هریت کریتون و باربارا مک کلینتاک در سال 1931 انجام شد. تحقیقات و آزمایشات آنها بر روی ذرت شواهد سیتولوژیکی برای نظریه ژنتیکی ارائه کرد که ژنهای مرتبط روی کروموزومهای جفت شده در واقع مکانهایی را از یک همولوگ به دیگری مبادله میکنند. [71]
احتمال وقوع متقاطع کروموزومی بین دو نقطه داده شده روی کروموزوم به فاصله بین نقاط مربوط می شود. برای یک مسافت خودسرانه طولانی، احتمال متقاطع به اندازهای زیاد است که وراثت ژنها به طور مؤثر ارتباطی ندارد. [72] اما برای ژنهایی که به هم نزدیکتر هستند، احتمال کمتر متقاطع به این معنی است که ژنها پیوند ژنتیکی را نشان میدهند. آلل های این دو ژن با هم به ارث می رسند. مقادیر پیوند بین یک سری از ژن ها را می توان برای تشکیل یک نقشه پیوند خطی ترکیب کرد که تقریباً آرایش ژن ها را در امتداد کروموزوم توصیف می کند. [73]
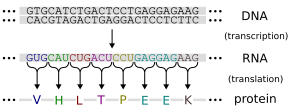
ژنها اثر عملکردی خود را از طریق تولید پروتئینها، که مولکولهایی هستند که اکثر عملکردها را در سلول بر عهده دارند، بیان میکنند . پروتئین ها از یک یا چند زنجیره پلی پپتیدی تشکیل شده اند که هر کدام از دنباله ای از اسیدهای آمینه تشکیل شده اند . توالی DNA یک ژن برای تولید یک توالی اسید آمینه خاص استفاده می شود . این فرآیند با تولید یک مولکول RNA با توالی منطبق با توالی DNA ژن آغاز می شود، فرآیندی که رونویسی نامیده می شود .
سپس این مولکول RNA پیام رسان برای تولید یک توالی اسید آمینه مربوطه از طریق فرآیندی به نام ترجمه عمل می کند . هر گروه از سه نوکلئوتید در توالی، که کدون نامیده می شود ، یا به یکی از بیست اسید آمینه ممکن در یک پروتئین یا دستورالعملی برای پایان دادن به توالی اسید آمینه مربوط است . این تطابق را کد ژنتیکی می نامند . [74] جریان اطلاعات یک جهته است: اطلاعات از توالی های نوکلئوتیدی به توالی اسید آمینه پروتئین ها منتقل می شود، اما هرگز از پروتئین به دنباله DNA منتقل نمی شود - پدیده ای که فرانسیس کریک آن را جزم اصلی زیست شناسی مولکولی می نامد . [75]
توالی خاص اسیدهای آمینه منجر به یک ساختار سه بعدی منحصر به فرد برای آن پروتئین می شود و ساختارهای سه بعدی پروتئین ها با عملکرد آنها مرتبط است. [76] [77] برخی مولکولهای ساختاری ساده هستند، مانند الیافی که توسط پروتئین کلاژن تشکیل میشوند . پروتئین ها می توانند به پروتئین های دیگر و مولکول های ساده متصل شوند و گاهی اوقات با تسهیل واکنش های شیمیایی در مولکول های متصل (بدون تغییر ساختار خود پروتئین) به عنوان آنزیم عمل می کنند. ساختار پروتئین پویا است. پروتئین هموگلوبین به شکل های کمی متفاوت خم می شود زیرا جذب، انتقال و آزادسازی مولکول های اکسیژن در خون پستانداران را تسهیل می کند. [ نیازمند منبع ]
یک تفاوت تک نوکلئوتیدی در DNA می تواند باعث تغییر در توالی اسید آمینه یک پروتئین شود. از آنجایی که ساختارهای پروتئینی نتیجه توالی اسیدهای آمینه آنهاست، برخی تغییرات می توانند با بی ثبات کردن ساختار یا تغییر سطح پروتئین به گونه ای که برهمکنش آن را با سایر پروتئین ها و مولکول ها تغییر دهد، خواص پروتئین را به طرز چشمگیری تغییر دهد. به عنوان مثال، کم خونی سلول داسی شکل یک بیماری ژنتیکی انسانی است که از یک تفاوت پایه در ناحیه کدکننده بخش β-گلوبین هموگلوبین ناشی می شود و باعث تغییر اسید آمینه منفرد می شود که خواص فیزیکی هموگلوبین را تغییر می دهد. [78] نسخههای داسی شکل هموگلوبین به خود میچسبند و روی هم میچسبند تا فیبرهایی را تشکیل دهند که شکل گلبولهای قرمز حامل پروتئین را تغییر میدهند. این سلولهای داسی شکل دیگر به آرامی در رگهای خونی جریان نمییابند و تمایل به انسداد یا تحلیل رفتن دارند و باعث مشکلات پزشکی مرتبط با این بیماری میشوند. [ نیازمند منبع ]
برخی از توالیهای DNA به RNA رونویسی میشوند، اما به محصولات پروتئینی ترجمه نمیشوند - این گونه مولکولهای RNA RNA غیر کدکننده نامیده میشوند . در برخی موارد، این محصولات به ساختارهایی تبدیل می شوند که در عملکردهای حیاتی سلول نقش دارند (مانند RNA ریبوزومی و RNA انتقالی ). RNA همچنین می تواند از طریق برهمکنش های هیبریداسیون با سایر مولکول های RNA (مانند microRNA ) اثرات تنظیمی داشته باشد. [ نیازمند منبع ]

اگرچه ژن ها حاوی تمام اطلاعاتی هستند که یک موجود زنده برای عملکرد استفاده می کند، اما محیط نقش مهمی در تعیین فنوتیپ های نهایی یک موجود زنده دارد. عبارت « طبیعت و پرورش » به این رابطه مکمل اشاره دارد. فنوتیپ یک موجود زنده به تعامل ژن ها و محیط بستگی دارد. یک مثال جالب رنگ کت گربه سیامی است . در این حالت دمای بدن گربه نقش محیط را بازی می کند. ژنهای گربه برای موهای تیره کد میکنند، بنابراین سلولهای تولیدکننده مو در گربه پروتئینهای سلولی میسازند که در نتیجه موهای تیره ایجاد میشود. اما این پروتئین های تولید کننده موهای تیره به دما حساس هستند (یعنی جهشی دارند که باعث حساسیت به دما می شود) و در محیط های با دمای بالاتر دناتوره می شوند و در مناطقی که گربه دمای بدن بالاتری دارد رنگدانه موهای تیره تولید نمی کند. با این حال، در یک محیط با دمای پایین، ساختار پروتئین پایدار است و رنگدانه موهای تیره را به طور معمول تولید می کند. این پروتئین در نواحی سردتر پوست مانند پاها، گوشها، دم و صورتش فعال میماند، بنابراین گربه موهای تیره در انتهای خود دارد. [79]
محیط نقش عمده ای در اثرات بیماری ژنتیکی انسانی فنیل کتونوری ایفا می کند . جهشی که باعث فنیل کتونوری می شود، توانایی بدن برای تجزیه اسید آمینه فنیل آلانین را مختل می کند و باعث ایجاد سمی در یک مولکول میانی می شود که به نوبه خود باعث علائم شدید ناتوانی ذهنی پیشرونده و تشنج می شود. با این حال، اگر فردی با جهش فنیل کتونوری از رژیم غذایی سختی پیروی کند که از این اسید آمینه اجتناب کند، طبیعی و سالم میماند. [80]
یک روش متداول برای تعیین اینکه چگونه ژن ها و محیط ("طبیعت و پرورش") به یک فنوتیپ کمک می کنند، شامل مطالعه دوقلوهای همسان و برادر ، یا سایر خواهر و برادرهای چند قلوزایی است . [81] خواهر و برادرهای یکسان از نظر ژنتیکی یکسان هستند زیرا از یک زیگوت می آیند. در همین حال، دوقلوهای برادر به اندازه خواهر و برادرهای عادی از نظر ژنتیکی با یکدیگر متفاوت هستند. دانشمندان با مقایسه تعداد دفعات بروز یک اختلال خاص در یک جفت دوقلوهای همسان با تعداد دفعات بروز آن در یک جفت دوقلوهای همسان، می توانند تعیین کنند که آیا این اختلال ناشی از عوامل محیطی ژنتیکی است یا پس از زایمان. یک مثال معروف شامل مطالعه چهارقلوهای Genain بود که چهار قلوهای یکسانی بودند که همگی مبتلا به اسکیزوفرنی بودند . [82]
ژنوم یک موجود زنده حاوی هزاران ژن است، اما لازم نیست همه این ژن ها در هر لحظه فعال باشند. یک ژن زمانی بیان میشود که به mRNA رونویسی میشود و روشهای سلولی زیادی برای کنترل بیان ژنها وجود دارد، به طوری که پروتئینها فقط در صورت نیاز سلول تولید میشوند. فاکتورهای رونویسی پروتئینهای تنظیمکنندهای هستند که به DNA متصل میشوند و رونویسی یک ژن را تقویت یا مهار میکنند. [83] برای مثال، در ژنوم باکتری اشریشیا کلی ، یک سری ژن لازم برای سنتز اسید آمینه تریپتوفان وجود دارد . با این حال، زمانی که تریپتوفان از قبل در دسترس سلول باشد، دیگر به این ژنها برای سنتز تریپتوفان نیازی نیست. وجود تریپتوفان به طور مستقیم بر فعالیت ژن ها تأثیر می گذارد - مولکول های تریپتوفان به سرکوب کننده تریپتوفان (یک عامل رونویسی) متصل می شوند و ساختار رپرسور را تغییر می دهند به طوری که رپرسور به ژن ها متصل می شود. رپرسور تریپتوفان رونویسی و بیان ژن ها را مسدود می کند و در نتیجه تنظیم بازخورد منفی فرآیند سنتز تریپتوفان را ایجاد می کند. [84]
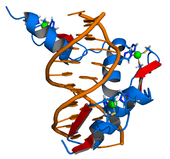
تفاوت در بیان ژن به ویژه در موجودات چند سلولی واضح است ، جایی که سلول ها همه حاوی ژنوم یکسانی هستند اما ساختارها و رفتارهای بسیار متفاوتی به دلیل بیان مجموعه های مختلف ژن ها دارند. تمام سلولهای موجود در یک ارگانیسم چند سلولی از یک سلول منفرد مشتق میشوند که در پاسخ به سیگنالهای خارجی و بین سلولی به انواع سلولهای متفاوت تمایز مییابند و به تدریج الگوهای مختلف بیان ژن را برای ایجاد رفتارهای متفاوت ایجاد میکنند. از آنجایی که هیچ ژن واحدی مسئول توسعه ساختارهای موجودات چند سلولی نیست، این الگوها از تعاملات پیچیده بین بسیاری از سلول ها ناشی می شوند. [ نیازمند منبع ]
در یوکاریوت ها ، ویژگی های ساختاری کروماتین وجود دارد که بر رونویسی ژن ها تأثیر می گذارد، اغلب به شکل تغییراتی در DNA و کروماتین که به طور پایدار توسط سلول های دختر به ارث می رسند. [85] این ویژگیها « اپی ژنتیک » نامیده میشوند زیرا «در بالای» توالی DNA وجود دارند و از نسلی به نسل دیگر وراثت را حفظ میکنند. به دلیل ویژگی های اپی ژنتیکی، انواع سلول های مختلف رشد کرده در یک محیط می توانند خواص بسیار متفاوتی را حفظ کنند. اگرچه ویژگی های اپی ژنتیکی به طور کلی در طول دوره رشد پویا هستند، برخی مانند پدیده پاراموتاسیون دارای وراثت چند نسلی هستند و به عنوان استثناهای نادری از قاعده کلی DNA به عنوان مبنای وراثت وجود دارند. [86]

در طول فرآیند تکثیر DNA، گاهی اوقات خطاهایی در پلیمریزاسیون رشته دوم رخ می دهد. این خطاها که جهش نامیده می شوند، می توانند بر فنوتیپ ارگانیسم تأثیر بگذارند، به خصوص اگر در توالی کدکننده پروتئین یک ژن رخ دهند. نرخ خطا معمولاً بسیار پایین است - یک خطا در هر 100-100 میلیون باز - به دلیل توانایی "تصحیح" DNA پلیمرازها . [۸۷] [۸۸] فرآیندهایی که سرعت تغییرات در DNA را افزایش میدهند، جهشزا نامیده میشوند : مواد شیمیایی جهشزا باعث ایجاد خطا در همانندسازی DNA میشوند، اغلب با تداخل در ساختار جفتسازی باز، در حالی که اشعه ماوراء بنفش با ایجاد آسیب به ساختار DNA باعث ایجاد جهش میشود. . [89] آسیب شیمیایی به DNA به طور طبیعی نیز رخ می دهد و سلول ها از مکانیسم های ترمیم DNA برای ترمیم ناهماهنگی ها و شکستگی ها استفاده می کنند. با این حال، تعمیر همیشه توالی اصلی را بازیابی نمی کند. به نظر می رسد یک منبع مهم آسیب های DNA، گونه های فعال اکسیژن [90] باشد که توسط تنفس هوازی سلولی تولید می شود و این می تواند منجر به جهش شود. [91]
در ارگانیسمهایی که از متقاطع کروموزومی برای تبادل DNA و ترکیب مجدد ژنها استفاده میکنند، اشتباهات در همسویی در طول میوز نیز میتواند باعث جهش شود. اشتباهات در متقاطع به ویژه زمانی محتمل است که توالی های مشابه باعث شوند کروموزوم های شریک یک تراز اشتباه اتخاذ کنند. این باعث می شود که برخی از مناطق در ژنوم مستعد جهش به این روش باشند. این خطاها تغییرات ساختاری بزرگی را در توالی DNA ایجاد میکند - تکرار ، وارونگی ، حذف کل مناطق - یا تبادل تصادفی بخشهای کامل توالی بین کروموزومهای مختلف، جابهجایی کروموزومی . [92]

جهش ها ژنوتیپ ارگانیسم را تغییر می دهند و گهگاه این امر باعث پدیدار شدن فنوتیپ های مختلف می شود. بیشتر جهشها تأثیر کمی بر فنوتیپ، سلامت یا تناسب تولید مثل ارگانیسم دارند . [93] جهش هایی که تأثیر دارند معمولاً مضر هستند، اما گاهی اوقات برخی از آنها می توانند مفید باشند. [94] مطالعات روی مگس مگس سرکه مگس سرکه نشان می دهد که اگر یک جهش پروتئین تولید شده توسط یک ژن را تغییر دهد، حدود 70 درصد از این جهش ها مضر هستند و بقیه خنثی یا ضعیف هستند. [95]

ژنتیک جمعیت توزیع تفاوت های ژنتیکی در جمعیت ها و چگونگی تغییر این توزیع ها در طول زمان را مطالعه می کند. [96] تغییرات در فراوانی یک آلل در یک جمعیت عمدتاً تحت تأثیر انتخاب طبیعی است ، جایی که یک آلل معین مزیت انتخابی یا تولیدمثلی را برای ارگانیسم فراهم میکند، [97] و همچنین عوامل دیگری مانند جهش ، رانش ژنتیکی ، ژنتیکی. سوارکاری ، [98] انتخاب مصنوعی و مهاجرت . [99]
در طول چندین نسل، ژنوم موجودات می تواند به طور قابل توجهی تغییر کند و منجر به تکامل شود. در فرآیندی که سازگاری نامیده میشود ، انتخاب برای جهشهای مفید میتواند باعث شود که گونهها به شکلهایی تبدیل شوند که بهتر بتوانند در محیط خود زنده بمانند. [100] گونههای جدید از طریق فرآیند گونهزایی شکل میگیرند که اغلب به دلیل جداییهای جغرافیایی ایجاد میشوند که از تبادل ژنها با یکدیگر جلوگیری میکند. [101]
با مقایسه همسانی بین ژنوم گونههای مختلف، میتوان فاصله تکاملی بین آنها و زمانی که ممکن است از هم جدا شده باشند را محاسبه کرد . مقایسات ژنتیکی به طور کلی روش دقیق تری برای توصیف ارتباط بین گونه ها نسبت به مقایسه ویژگی های فنوتیپی در نظر گرفته می شود. از فواصل تکاملی بین گونه ها می توان برای تشکیل درختان تکاملی استفاده کرد . این درختان نشان دهنده تبار و واگرایی مشترک گونه ها در طول زمان هستند، اگرچه انتقال مواد ژنتیکی را بین گونه های غیر مرتبط نشان نمی دهند (که به عنوان انتقال افقی ژن شناخته می شود و در باکتری ها رایج است). [102]
.jpg/440px-Drosophila_melanogaster_-_side_(aka).jpg)
اگرچه ژنتیک دانان در ابتدا وراثت را در طیف گسترده ای از ارگانیسم ها مورد مطالعه قرار دادند، دامنه گونه های مورد مطالعه محدود شده است. یکی از دلایل این است که وقتی تحقیقات قابل توجهی در حال حاضر برای یک موجود زنده وجود دارد، محققان جدید به احتمال زیاد آن را برای مطالعه بیشتر انتخاب می کنند، و بنابراین در نهایت تعداد کمی از ارگانیسم های مدل مبنای اکثر تحقیقات ژنتیکی شدند. موضوعات تحقیقاتی رایج در ژنتیک ارگانیسم مدل شامل مطالعه تنظیم ژن و دخالت ژن ها در توسعه و سرطان است . ارگانیسمها تا حدی برای راحتی انتخاب شدند - زمان کوتاه نسل و دستکاری ژنتیکی آسان ، برخی از موجودات را به ابزارهای تحقیقاتی ژنتیکی محبوب تبدیل کرد. ارگانیسم های مدل پرکاربرد شامل باکتری روده اشریشیا کلی ، گیاه Arabidopsis thaliana ، مخمر نانوایی ( Saccharomyces cerevisiae )، نماتد Caenorhabditis elegans ، مگس میوه معمولی ( Drosophila melanogaster )، گورخرماهی ( دانیو معمولی) Mus musculus ). [103]

ژنتیک پزشکی به دنبال درک چگونگی ارتباط تنوع ژنتیکی با سلامت و بیماری انسان است. [104] هنگام جستجوی یک ژن ناشناخته که ممکن است در یک بیماری نقش داشته باشد، محققان معمولاً از پیوند ژنتیکی و نمودارهای شجره ژنتیکی برای یافتن مکان روی ژنوم مرتبط با بیماری استفاده می کنند. در سطح جمعیت، محققان از تصادفیسازی مندلی برای جستجوی مکانهایی در ژنوم که با بیماریها مرتبط هستند، استفاده میکنند، روشی که مخصوصاً برای صفات چند ژنی که به وضوح توسط یک ژن مشخص نشدهاند، مفید است. [105] هنگامی که یک ژن کاندید پیدا شد، تحقیقات بیشتر اغلب بر روی ژن های مربوطه (یا همولوگ ) موجودات مدل انجام می شود. علاوه بر مطالعه بیماریهای ژنتیکی، افزایش دسترسی به روشهای ژنوتیپسازی منجر به ایجاد زمینه فارماکوژنتیک شده است : مطالعه چگونگی تأثیر ژنوتیپ بر پاسخهای دارویی. [106]
گرایش ارثی افراد به سرطان متفاوت است و سرطان یک بیماری ژنتیکی است. روند رشد سرطان در بدن ترکیبی از رویدادها است. گاهی اوقات جهش در سلول های بدن هنگام تقسیم آنها رخ می دهد. اگرچه این جهشها توسط هیچ فرزندی به ارث نمیرسند، اما میتوانند بر رفتار سلولها تأثیر بگذارند و گاهی اوقات باعث رشد و تقسیم بیشتر آنها شوند. مکانیسم های بیولوژیکی وجود دارد که تلاش می کند این روند را متوقف کند. سیگنال هایی به سلول های در حال تقسیم نامناسب داده می شود که باید باعث مرگ سلولی شود ، اما گاهی اوقات جهش های اضافی رخ می دهد که باعث می شود سلول ها این پیام ها را نادیده بگیرند. یک فرآیند درونی انتخاب طبیعی در بدن رخ می دهد و در نهایت جهش ها در سلول ها جمع می شوند تا رشد خود را تقویت کنند و یک تومور سرطانی ایجاد می کنند که رشد می کند و به بافت های مختلف بدن حمله می کند. به طور معمول، یک سلول تنها در پاسخ به سیگنال هایی به نام فاکتورهای رشد تقسیم می شود و یک بار در تماس با سلول های اطراف و در پاسخ به سیگنال های بازدارنده رشد، رشد خود را متوقف می کند. معمولاً تعداد محدودی دفعات تقسیم میشود و میمیرد و در داخل اپیتلیوم باقی میماند ، جایی که قادر به مهاجرت به سایر اندامها نیست. برای تبدیل شدن به یک سلول سرطانی، یک سلول باید جهش هایی را در تعدادی از ژن ها (سه تا هفت) جمع کند. یک سلول سرطانی می تواند بدون فاکتور رشد تقسیم شود و سیگنال های بازدارنده را نادیده بگیرد. همچنین، فناناپذیر است و حتی پس از تماس با سلول های همسایه می تواند به طور نامحدود رشد کند. ممکن است از اپیتلیوم و در نهایت از تومور اولیه فرار کند . سپس، سلول فراری میتواند از اندوتلیوم یک رگ خونی عبور کند و توسط جریان خون برای استعمار یک عضو جدید منتقل شود و متاستاز مرگبار ایجاد کند . اگرچه در بخش کوچکی از سرطانها برخی زمینههای ژنتیکی وجود دارد، بخش عمده آن به دلیل مجموعهای از جهشهای ژنتیکی جدید است که در ابتدا ظاهر میشوند و در یک یا تعداد کمی از سلولها تجمع مییابند که برای تشکیل تومور تقسیم میشوند و به آنها منتقل نمیشوند. نتاج ( جهش های جسمی ). شایع ترین جهش ها از دست دادن عملکرد پروتئین p53 ، یک سرکوب کننده تومور ، یا در مسیر p53، و افزایش جهش عملکرد در پروتئین های Ras یا سایر انکوژن ها است . [107] [108]
DNA را می توان در آزمایشگاه دستکاری کرد. آنزیم های محدود کننده معمولاً آنزیم هایی هستند که DNA را در توالی های خاص برش می دهند و قطعات قابل پیش بینی DNA را تولید می کنند. [109] قطعات DNA را می توان با استفاده از الکتروفورز ژل مشاهده کرد ، که قطعات را بر اساس طول آنها جدا می کند. [110]
استفاده از آنزیم های بستن اجازه می دهد تا قطعات DNA به هم متصل شوند. با اتصال ("بستن") قطعات DNA به یکدیگر از منابع مختلف، محققان می توانند DNA نوترکیب ایجاد کنند ، DNA که اغلب با ارگانیسم های اصلاح شده ژنتیکی مرتبط است . DNA نوترکیب معمولاً در زمینه پلاسمیدها استفاده می شود : مولکول های DNA دایره ای کوتاه با چند ژن روی آنها. در فرآیندی که به عنوان شبیهسازی مولکولی شناخته میشود ، محققان میتوانند قطعات DNA را با وارد کردن پلاسمیدها در باکتریها و سپس کشت آنها روی صفحات آگار (برای جداسازی کلونهای سلولهای باکتری ) تقویت کنند. "کلونینگ" همچنین می تواند به ابزارهای مختلف ایجاد موجودات شبیه سازی شده ("کلونال") اشاره داشته باشد. [111]
DNA همچنین می تواند با استفاده از روشی به نام واکنش زنجیره ای پلیمراز (PCR) تقویت شود. [112] با استفاده از توالی های کوتاه خاص DNA، PCR می تواند یک ناحیه هدف از DNA را جدا کرده و به صورت نمایی تقویت کند. از آنجایی که می تواند از مقادیر بسیار کمی DNA تکثیر شود، PCR اغلب برای تشخیص وجود توالی های DNA خاص نیز استفاده می شود. [113] [114]
توالی یابی DNA، یکی از اساسی ترین فناوری های توسعه یافته برای مطالعه ژنتیک، به محققان اجازه می دهد تا توالی نوکلئوتیدها را در قطعات DNA تعیین کنند. تکنیک توالی یابی خاتمه زنجیره ای که در سال 1977 توسط تیمی به رهبری فردریک سانگر توسعه یافت ، هنوز به طور معمول برای تعیین توالی قطعات DNA استفاده می شود. با استفاده از این فناوری، محققان توانستهاند توالیهای مولکولی مرتبط با بسیاری از بیماریهای انسانی را مطالعه کنند. [115]
از آنجایی که توالی یابی ارزان تر شده است، محققان ژنوم بسیاری از ارگانیسم ها را با استفاده از فرآیندی به نام مونتاژ ژنوم تعیین توالی کرده اند که از ابزارهای محاسباتی برای به هم پیوند زدن توالی از قطعات مختلف استفاده می کند. [ 116] این فناوریها برای تعیین توالی ژنوم انسان در پروژه ژنوم انسانی که در سال 2003 تکمیل شد، استفاده شد . ژنوم انسان به هزار دلار رسید. [117]
توالییابی نسل بعدی (یا توالییابی با توان عملیاتی بالا) به دلیل تقاضای روزافزون برای توالییابی کم هزینه به وجود آمد. این فناوریهای توالییابی امکان تولید میلیونها توالی را به طور همزمان فراهم میکنند. [118] [119] حجم زیادی از داده های توالی موجود، زیرشاخه ژنومیک را ایجاد کرده است ، تحقیقاتی که از ابزارهای محاسباتی برای جستجو و تجزیه و تحلیل الگوها در ژنوم کامل موجودات استفاده می کند. ژنومیک را می توان زیر شاخه ای از بیوانفورماتیک نیز در نظر گرفت که از رویکردهای محاسباتی برای تجزیه و تحلیل مجموعه های بزرگی از داده های بیولوژیکی استفاده می کند . یک مشکل رایج در این زمینه های تحقیقاتی نحوه مدیریت و به اشتراک گذاری داده هایی است که با موضوع انسانی و اطلاعات قابل شناسایی شخصی سروکار دارد . [ نیازمند منبع ]
در 19 مارس 2015، گروهی از زیست شناسان برجسته خواستار ممنوعیت جهانی استفاده بالینی از روش ها، به ویژه استفاده از CRISPR و انگشت روی ، برای ویرایش ژنوم انسان به روشی که می تواند ارثی باشد، شد. [120] [121] [122] [123] در آوریل 2015، محققان چینی نتایج تحقیقات پایه را برای ویرایش DNA جنین های غیرقابل زنده انسان با استفاده از CRISPR گزارش کردند . [124] [125]