بیوشیمی یا شیمی بیولوژیکی مطالعه فرآیندهای شیمیایی درون موجودات زنده و مرتبط با آنها است . [1] یکی از زیرشاخه های شیمی و زیست شناسی ، بیوشیمی را می توان به سه زمینه تقسیم کرد: زیست شناسی ساختاری ، آنزیم شناسی ، و متابولیسم . در دهه های آخر قرن بیستم، بیوشیمی در توضیح فرآیندهای زنده از طریق این سه رشته موفق شده است. تقریباً تمام حوزههای علوم زیستی از طریق روششناسی و تحقیقات بیوشیمیایی کشف و توسعه مییابند. [2] بیوشیمی بر درک اساس شیمیایی تمرکز دارد که به مولکولهای بیولوژیکی اجازه میدهد تا فرآیندهایی را که در سلولهای زنده و بین سلولها اتفاق میافتد، ایجاد کنند، [3] که به نوبه خود بسیار به درک بافتها و اندامها و همچنین ساختار و عملکرد ارگانیسم مربوط میشود. . [4] بیوشیمی ارتباط نزدیکی با زیست شناسی مولکولی ، مطالعه مکانیسم های مولکولی پدیده های بیولوژیکی دارد. [5]
بیشتر بیوشیمی با ساختارها، عملکردها و برهمکنشهای ماکرومولکولهای بیولوژیکی مانند پروتئینها ، اسیدهای نوکلئیک ، کربوهیدراتها و لیپیدها سر و کار دارد . آنها ساختار سلول ها را فراهم می کنند و بسیاری از عملکردهای مرتبط با زندگی را انجام می دهند. [6] شیمی سلول همچنین به واکنشهای مولکولهای کوچک و یونها بستگی دارد . اینها می توانند غیر آلی (به عنوان مثال، یون های آب و فلز ) یا آلی (به عنوان مثال، اسیدهای آمینه ، که برای سنتز پروتئین ها استفاده می شود ) باشند. [7] مکانیسمهایی که سلولها برای مهار انرژی از محیط خود از طریق واکنشهای شیمیایی استفاده میکنند به عنوان متابولیسم شناخته میشوند . یافته های بیوشیمی عمدتاً در پزشکی ، تغذیه و کشاورزی کاربرد دارد . در پزشکی، بیوشیمی دانان علل و درمان بیماری ها را بررسی می کنند . [8] تغذیه به مطالعه چگونگی حفظ سلامت و تندرستی و همچنین اثرات کمبودهای تغذیه ای می پردازد . [9] در کشاورزی، بیوشیمی دانان خاک و کودها را با هدف بهبود کشت محصول، ذخیره سازی محصول و کنترل آفات بررسی می کنند . در دهههای اخیر، اصول و روشهای بیوشیمیایی با رویکردهای حل مسئله از مهندسی تا دستکاری سیستمهای زنده ترکیب شدهاند تا ابزارهای مفیدی برای تحقیقات، فرآیندهای صنعتی، و تشخیص و کنترل بیماری - رشته بیوتکنولوژی - تولید کنند .
_and_Carl_Ferdinand_Cori_-_restoration1.jpg/440px-Gerty_Theresa_Radnitz_Cori_(1896-1957)_and_Carl_Ferdinand_Cori_-_restoration1.jpg)
در جامع ترین تعریف خود، بیوشیمی را می توان مطالعه ای در مورد اجزاء و ترکیب موجودات زنده و چگونگی گرد هم آمدن آنها برای تبدیل شدن به حیات دانست. از این نظر، تاریخ بیوشیمی ممکن است به یونانیان باستان بازگردد . [10] با این حال، بیوشیمی به عنوان یک رشته علمی خاص زمانی در قرن نوزدهم یا کمی زودتر شروع شد، بسته به اینکه روی کدام جنبه از بیوشیمی متمرکز شده است. برخی استدلال کردند که آغاز بیوشیمی ممکن است کشف اولین آنزیم ، دیاستاز (که اکنون آمیلاز نامیده می شود ) در سال 1833 توسط آنسلم پاین باشد ، [11] در حالی که برخی دیگر اولین نمایش ادوارد بوخنر از یک فرآیند بیوشیمیایی پیچیده تخمیر الکلی را در نظر گرفتند . عصاره های بدون سلول در سال 1897 تولد بیوشیمی است. [12] [13] برخی همچنین ممکن است به عنوان آغاز آن به کار تأثیرگذار 1842 توسط Justus von Liebig ، شیمی جانوری، یا، شیمی آلی در کاربردهای آن در فیزیولوژی و آسیب شناسی اشاره کنند ، که یک نظریه شیمیایی متابولیسم ارائه کرد، [10] یا حتی قبل از قرن 18 مطالعاتی در مورد تخمیر و تنفس توسط Antoine Lavoisier . [14] [15] بسیاری از پیشگامان دیگر در این زمینه که به کشف لایه های پیچیدگی بیوشیمی کمک کردند، بنیانگذاران بیوشیمی مدرن اعلام شده اند. امیل فیشر ، که شیمی پروتئین ها را مطالعه کرد ، [16] و اف. گاولند هاپکینز ، که آنزیم ها و ماهیت دینامیکی بیوشیمی را مطالعه کرد، دو نمونه از بیوشیمی دانان اولیه را نشان می دهند. [17]
اصطلاح "بیوشیمی" اولین بار زمانی استفاده شد که Vinzenz Kletzinsky (1826-1882) "Compendium der Biochemie" خود را در سال 1858 در وین چاپ کرد. از ترکیبی از زیست شناسی و شیمی گرفته شده است . در سال 1877، فلیکس هوپ-سایلر در مقدمه اولین شماره مجله Zeitschrift für Physiologische Chemie (ژورنال شیمی فیزیولوژیکی) از اصطلاح ( بیوشیمی در آلمانی) به عنوان مترادف شیمی فیزیولوژیکی استفاده کرد ، جایی که او برای تأسیس مؤسسههایی که به این موضوع اختصاص داده شده بود استدلال کرد. این رشته تحصیلی [18] [19] شیمیدان آلمانی کارل نوبرگ اغلب ذکر می شود که این کلمه را در سال 1903 ابداع کرده است، [20] [21] [22] در حالی که برخی آن را به فرانتس هافمایستر نسبت می دهند . [23]
زمانی عموماً اعتقاد بر این بود که حیات و مواد آن دارای خاصیت یا جوهری هستند (که اغلب به عنوان « اصل حیاتی » نامیده میشود) متمایز از هر موجودی که در ماده غیر زنده یافت میشود، و تصور میشد که فقط موجودات زنده میتوانند مولکولهای آن را تولید کنند. زندگی [25] در سال 1828، فردریش ویلر مقاله ای در مورد سنتز اوره سرندیپیتی خود از سیانات پتاسیم و سولفات آمونیوم منتشر کرد . برخی آن را سرنگونی مستقیم حیات گرایی و ایجاد شیمی آلی می دانستند . [26] [27] با این حال، سنتز Wöhler جنجال برانگیخته است زیرا برخی مرگ حیات گرایی به دست او را رد می کنند. [28] از آن زمان، بیوشیمی، به ویژه از اواسط قرن بیستم، با توسعه تکنیکهای جدید مانند کروماتوگرافی ، پراش اشعه ایکس ، تداخل سنجی قطبش دوگانه ، طیفسنجی NMR ، برچسبگذاری رادیوایزوتوپی ، میکروسکوپ الکترونی و دینامیک مولکولی پیشرفت کرده است . این تکنیکها امکان کشف و تجزیه و تحلیل دقیق بسیاری از مولکولها و مسیرهای متابولیکی سلول ، مانند گلیکولیز و چرخه کربس (چرخه اسید سیتریک) را فراهم کرد و منجر به درک بیوشیمی در سطح مولکولی شد. [ نیازمند منبع ]
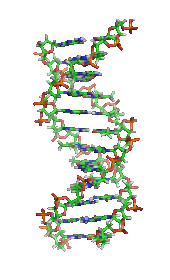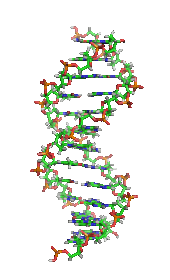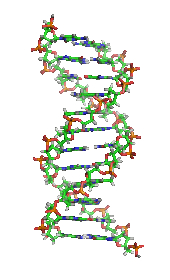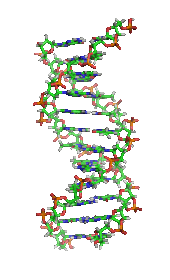
یکی دیگر از رویدادهای تاریخی مهم در بیوشیمی، کشف ژن و نقش آن در انتقال اطلاعات در سلول است. در دهه 1950، جیمز دی واتسون ، فرانسیس کریک ، روزالیند فرانکلین و موریس ویلکینز در حل ساختار DNA و پیشنهاد رابطه آن با انتقال ژنتیکی اطلاعات نقش مهمی داشتند. [29] در سال 1958، جورج بیدل و ادوارد تاتوم جایزه نوبل را برای کار در قارچها دریافت کردند که نشان میداد یک ژن یک آنزیم را تولید میکند . [30] در سال 1988، کالین پیچفورک اولین فردی بود که با شواهد DNA به قتل محکوم شد ، که منجر به رشد علم پزشکی قانونی شد . [31] اخیراً، اندرو زی فایر و کریگ سی ملو جایزه نوبل سال 2006 را برای کشف نقش تداخل RNA (RNAi) در خاموش کردن بیان ژن دریافت کردند . [32]
حدود دوجین عنصر شیمیایی برای انواع مختلف حیات بیولوژیکی ضروری هستند . بیشتر عناصر کمیاب روی زمین مورد نیاز حیات نیستند (به استثنای سلنیوم و ید )، [33] در حالی که تعدادی از عناصر رایج ( آلومینیوم و تیتانیوم ) استفاده نمی شوند. اکثر موجودات نیاز به عناصر مشترک دارند، اما چند تفاوت بین گیاهان و حیوانات وجود دارد . برای مثال، جلبکهای اقیانوسی از برم استفاده میکنند ، اما به نظر نمیرسد که گیاهان و جانوران خشکی نیازی به آن نداشته باشند. همه حیوانات به سدیم نیاز دارند ، اما عنصر ضروری برای گیاهان نیست. گیاهان به بور و سیلیکون نیاز دارند ، اما حیوانات ممکن است نه (یا ممکن است به مقادیر بسیار کمی نیاز داشته باشند). [ نیازمند منبع ]
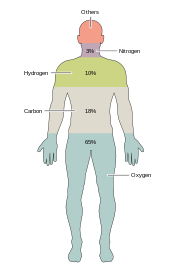
فقط شش عنصر - کربن ، هیدروژن ، نیتروژن ، اکسیژن ، کلسیم و فسفر - تقریباً 99 درصد از جرم سلولهای زنده را تشکیل میدهند، از جمله سلولهای بدن انسان ( برای فهرست کامل به ترکیب بدن انسان مراجعه کنید). علاوه بر شش عنصر اصلی که بیشتر بدن انسان را تشکیل می دهند، انسان به مقادیر کمتری احتمالاً 18 عنصر دیگر نیاز دارد. [34]
4 دسته اصلی مولکول ها در بیوشیمی (که اغلب بیومولکول نامیده می شود) کربوهیدرات ها ، لیپیدها ، پروتئین ها و اسیدهای نوکلئیک هستند . [35] بسیاری از مولکولهای بیولوژیکی پلیمر هستند : در این اصطلاح، مونومرها درشت مولکولهای نسبتاً کوچکی هستند که برای ایجاد درشت مولکولهای بزرگ به نام پلیمر به یکدیگر متصل میشوند. هنگامی که مونومرها برای سنتز یک پلیمر بیولوژیکی به یکدیگر متصل می شوند ، تحت فرآیندی به نام سنتز کم آبی قرار می گیرند . ماکرومولکولهای مختلف میتوانند در کمپلکسهای بزرگتری که اغلب برای فعالیتهای بیولوژیکی مورد نیاز هستند، جمع شوند .
دو مورد از وظایف اصلی کربوهیدرات ها ذخیره انرژی و ایجاد ساختار است. یکی از قندهای رایج که به نام گلوکز شناخته می شود کربوهیدرات است، اما همه کربوهیدرات ها قند نیستند. کربوهیدرات های بیشتری نسبت به هر نوع زیست مولکول شناخته شده دیگری در زمین وجود دارد. از آنها برای ذخیره انرژی و اطلاعات ژنتیکی و همچنین نقش مهمی در تعاملات و ارتباطات سلول به سلول استفاده می شود . [ نیازمند منبع ]
ساده ترین نوع کربوهیدرات یک مونوساکارید است که در میان خواص دیگر آن حاوی کربن ، هیدروژن و اکسیژن است که عمدتاً به نسبت 1:2:1 است (فرمول کلی C n H 2 n O n که n حداقل 3 است). گلوکز (C 6 H 12 O 6 ) یکی از مهم ترین کربوهیدرات ها است. سایرین عبارتند از فروکتوز (C 6 H 12 O 6 )، قندی که معمولاً با طعم شیرین میوه ها مرتبط است ، [36] [a] و دئوکسی ریبوز (C 5 H 10 O 4 ) که جزء DNA است . یک مونوساکارید می تواند بین فرم غیر حلقوی (زنجیره باز) و شکل حلقوی جابجا شود . شکل زنجیره باز را می توان به حلقه ای از اتم های کربن تبدیل کرد که توسط یک اتم اکسیژن ایجاد شده از گروه کربونیل یک سر و گروه هیدروکسیل در انتهای دیگر پل شده اند. بسته به اینکه شکل خطی آن آلدوز یا کتوز باشد، مولکول حلقوی دارای یک گروه همی استال یا همیکتال است . [38]
در این اشکال حلقوی، حلقه معمولاً دارای 5 یا 6 اتم است. این اشکال به ترتیب فورانوز و پیرانوز نامیده میشوند —بر اساس قیاس با فوران و پیران ، سادهترین ترکیبات با حلقه کربن-اکسیژن یکسان (اگرچه فاقد پیوندهای دوگانه کربن-کربن این دو مولکول هستند). به عنوان مثال، گلوکز آلدوهگزوز ممکن است یک پیوند همی استال بین هیدروکسیل روی کربن 1 و اکسیژن موجود در کربن 4 ایجاد کند و مولکولی با یک حلقه 5 عضوی به نام گلوکوفورانوز ایجاد کند . همین واکنش می تواند بین کربن های 1 و 5 اتفاق بیفتد تا یک مولکول با یک حلقه 6 عضوی به نام گلوکوپیرانوز تشکیل شود . اشکال حلقوی با یک حلقه 7 اتمی به نام هپتوز نادر است. [ نیازمند منبع ]
دو مونوساکارید را می توان توسط یک پیوند گلیکوزیدی یا استری به یک دی ساکارید از طریق واکنش کم آبی که طی آن یک مولکول آب آزاد می شود، متصل کرد. واکنش معکوس که در آن پیوند گلیکوزیدی یک دی ساکارید به دو مونوساکارید شکسته می شود، هیدرولیز نامیده می شود . شناخته شده ترین دی ساکارید ساکارز یا شکر معمولی است که از یک مولکول گلوکز و یک مولکول فروکتوز به هم متصل شده است. دی ساکارید مهم دیگر لاکتوز موجود در شیر است که از یک مولکول گلوکز و یک مولکول گالاکتوز تشکیل شده است. لاکتوز ممکن است توسط لاکتاز هیدرولیز شود و کمبود این آنزیم منجر به عدم تحمل لاکتوز می شود .
هنگامی که چند (حدود سه تا شش) مونوساکارید به هم متصل می شوند، به آن الیگوساکارید ( الیگو به معنی "چند") می گویند. این مولکول ها معمولاً به عنوان نشانگر و سیگنال و همچنین استفاده های دیگر مورد استفاده قرار می گیرند. [39] بسیاری از مونوساکاریدها به هم پیوسته یک پلی ساکارید را تشکیل می دهند . آنها می توانند در یک زنجیره خطی بلند به هم متصل شوند یا ممکن است منشعب شوند . دو تا از رایج ترین پلی ساکاریدها سلولز و گلیکوژن هستند که هر دو از مونومرهای گلوکز مکرر تشکیل شده اند . سلولز یک جزء ساختاری مهم دیواره سلولی گیاهان است و گلیکوژن به عنوان نوعی ذخیره انرژی در حیوانات استفاده می شود.
قند را می توان با داشتن انتهای کاهنده یا غیر کاهنده مشخص کرد. انتهای کاهنده کربوهیدرات، اتم کربنی است که می تواند با آلدهید با زنجیره باز ( آلدوز ) یا کتو ( کتوز ) در تعادل باشد. اگر به هم پیوستن مونومرها در چنین اتم کربنی صورت گیرد، گروه هیدروکسی آزاد شکل پیرانوز یا فورانوز با یک زنجیره جانبی OH از قند دیگری مبادله می شود و یک استال کامل به دست می آید . این از باز شدن زنجیره به شکل آلدئید یا کتو جلوگیری می کند و باقیمانده اصلاح شده را احیا نمی کند. لاکتوز حاوی یک انتهای کاهنده در قسمت گلوکز خود است، در حالی که قسمت گالاکتوز یک استال کامل را با گروه گلوکز C4-OH تشکیل می دهد. ساکاروز به دلیل تشکیل کامل استال بین کربن آلدهید گلوکز (C1) و کتو کربن فروکتوز (C2) انتهای احیا کننده ندارد.

لیپیدها طیف متنوعی از مولکولها را شامل میشوند و تا حدی عامل جذب ترکیبات نسبتاً نامحلول در آب یا غیرقطبی با منشأ بیولوژیکی هستند ، از جمله مومها ، اسیدهای چرب ، فسفولیپیدهای مشتق شده از اسیدهای چرب، اسفنگولیپیدها ، گلیکولیپیدها ، وترپنوئیدها ( مثلاً). برخی از لیپیدها مولکول های آلیفاتیک خطی و با زنجیره باز هستند، در حالی که برخی دیگر دارای ساختار حلقه ای هستند. برخی معطر هستند (با ساختار حلقوی و مسطح [مسطح]) در حالی که برخی دیگر معطر نیستند. برخی انعطاف پذیر هستند، در حالی که برخی دیگر سفت و سخت هستند. [42]
لیپیدها معمولا از یک مولکول گلیسرول ترکیب شده با مولکول های دیگر ساخته می شوند. در تری گلیسیریدها ، گروه اصلی لیپیدهای حجیم، یک مولکول گلیسرول و سه اسید چرب وجود دارد . اسیدهای چرب در آن حالت مونومر در نظر گرفته می شوند و ممکن است اشباع (بدون پیوند دوگانه در زنجیره کربن) یا غیر اشباع (یک یا چند پیوند دوگانه در زنجیره کربنی). [ نیازمند منبع ]
بیشتر لیپیدها دارای خاصیت قطبی هستند و تا حد زیادی غیرقطبی هستند. به طور کلی، بخش عمده ای از ساختار آنها غیرقطبی یا آبگریز است ("آب ترس")، به این معنی که به خوبی با حلال های قطبی مانند آب تعامل ندارد . بخش دیگری از ساختار آنها قطبی یا آبدوست ("آب دوست") است و تمایل دارند با حلال های قطبی مانند آب مرتبط شوند. این باعث میشود که مولکولهای آمفیفیل (دارای بخشهای آبگریز و آبدوست) باشند. در مورد کلسترول ، گروه قطبی یک –OH (هیدروکسیل یا الکل) است. [ نیازمند منبع ]
در مورد فسفولیپیدها، گروه های قطبی به طور قابل توجهی بزرگتر و قطبی تر هستند، همانطور که در زیر توضیح داده شده است.
لیپیدها بخشی جدایی ناپذیر از رژیم غذایی روزانه ما هستند. بیشتر روغن ها و فرآورده های شیری که برای پخت و پز و خوردن استفاده می کنیم مانند کره ، پنیر ، قیمه و غیره از چربی تشکیل شده اند . روغنهای گیاهی سرشار از اسیدهای چرب غیراشباع مختلف (PUFA) هستند. غذاهای حاوی لیپید در بدن هضم می شوند و به اسیدهای چرب و گلیسرول، محصولات نهایی تجزیه چربی ها و لیپیدها، تجزیه می شوند. لیپیدها، به ویژه فسفولیپیدها ، همچنین در محصولات دارویی مختلف ، یا به عنوان حل کننده های کمکی (مثلاً در انفوزیون تزریقی) و یا به عنوان اجزای حامل دارو (مثلاً در لیپوزوم یا ترانسفرزوم ) استفاده می شوند .
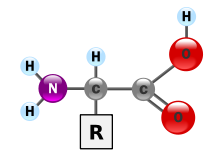
پروتئین ها مولکول های بسیار بزرگی هستند - ماکرو بیوپلیمرها - که از مونومرهایی به نام اسیدهای آمینه ساخته شده اند . یک اسید آمینه شامل یک اتم کربن آلفا متصل به یک گروه آمینه ، -NH 2 ، یک گروه اسید کربوکسیلیک ، -COOH (اگرچه اینها به صورت -NH 3 + و -COO - در شرایط فیزیولوژیک وجود دارند)، یک اتم هیدروژن ساده ، و یک زنجیره جانبی که معمولاً با "–R" نشان داده می شود. زنجیره جانبی "R" برای هر اسید آمینه متفاوت است که 20 اسید آمینه استاندارد وجود دارد . این گروه "R" است که هر اسید آمینه را متفاوت می کند، و خواص زنجیره های جانبی تا حد زیادی بر ساختار کلی سه بعدی یک پروتئین تأثیر می گذارد. برخی از اسیدهای آمینه به خودی خود یا به شکل اصلاح شده عملکرد دارند. به عنوان مثال، گلوتامات به عنوان یک انتقال دهنده عصبی مهم عمل می کند . اسیدهای آمینه را می توان از طریق پیوند پپتیدی به یکدیگر متصل کرد . در این سنتز آبگیری ، یک مولکول آب حذف می شود و پیوند پپتیدی نیتروژن گروه آمینه یک اسید آمینه را به کربن گروه اسید کربوکسیلیک دیگری متصل می کند. مولکول به دست آمده دی پپتید نامیده می شود و امتداد کوتاهی از اسیدهای آمینه (معمولاً کمتر از سی) پپتید یا پلی پپتید نامیده می شود . کشش های طولانی تر شایستگی عنوان پروتئین ها را دارد . به عنوان مثال، پروتئین مهم سرم خون آلبومین حاوی 585 اسید آمینه باقی مانده است . [43]


پروتئین ها می توانند نقش های ساختاری و/یا عملکردی داشته باشند. به عنوان مثال، حرکات پروتئینهای اکتین و میوزین در نهایت مسئول انقباض ماهیچههای اسکلتی هستند. یکی از ویژگیهای بسیاری از پروتئینها این است که آنها به طور خاص به یک مولکول یا کلاس خاصی از مولکولها متصل میشوند—ممکن است در آنچه که متصل میشوند بسیار انتخابی باشند. آنتی بادی ها نمونه ای از پروتئین هایی هستند که به یک نوع خاصی از مولکول متصل می شوند. آنتی بادی ها از زنجیره های سنگین و سبک تشکیل شده اند. دو زنجیره سنگین از طریق پیوندهای دی سولفیدی بین اسیدهای آمینه خود به دو زنجیره سبک متصل می شوند . آنتی بادی ها از طریق تنوع بر اساس تفاوت در دامنه N ترمینال خاص هستند. [44]
سنجش ایمونوسوربنت متصل به آنزیم (ELISA) که از آنتی بادی ها استفاده می کند، یکی از حساس ترین آزمایش هایی است که پزشکی مدرن برای شناسایی مولکول های زیستی مختلف از آن استفاده می کند. با این حال، احتمالا مهم ترین پروتئین ها، آنزیم ها هستند . تقریباً هر واکنشی در یک سلول زنده به یک آنزیم برای کاهش انرژی فعال سازی واکنش نیاز دارد. این مولکول ها مولکول های واکنش دهنده خاصی به نام سوبسترا را تشخیص می دهند . آنها سپس واکنش بین خود را کاتالیز می کنند . با کاهش انرژی فعال سازی ، آنزیم آن واکنش را با سرعت 10 11 یا بیشتر سرعت می بخشد. واکنشی که به طور معمول بیش از 3000 سال طول می کشد تا به طور خود به خود تکمیل شود ممکن است کمتر از یک ثانیه با یک آنزیم طول بکشد. خود آنزیم در این فرآیند مصرف نمی شود و آزاد است که همان واکنش را با مجموعه جدیدی از سوبستراها کاتالیز کند. با استفاده از اصلاحکنندههای مختلف، فعالیت آنزیم را میتوان تنظیم کرد و کنترل بیوشیمی سلول را به طور کلی امکانپذیر کرد.
ساختار پروتئین ها به طور سنتی در یک سلسله مراتب از چهار سطح توصیف می شود. ساختار اولیه یک پروتئین از توالی خطی اسیدهای آمینه آن تشکیل شده است. به عنوان مثال، "آلانین-گلیسین-تریپتوفان-سرین-گلوتامات-آسپارژین-گلیسین-لیزین-...". ساختار ثانویه مربوط به مورفولوژی محلی است (مورفولوژی مطالعه ساختار است). برخی از ترکیبات آمینو اسیدها در یک سیم پیچ به نام مارپیچ α یا به ورقه ای به نام ورقه β خم می شوند . برخی از مارپیچ های α را می توان در شماتیک هموگلوبین بالا مشاهده کرد. ساختار سوم کل شکل سه بعدی پروتئین است. این شکل توسط توالی اسیدهای آمینه تعیین می شود. در واقع یک تغییر می تواند کل ساختار را تغییر دهد. زنجیره آلفای هموگلوبین حاوی 146 اسید آمینه باقی مانده است. جایگزینی باقی مانده گلوتامات در موقعیت 6 با باقی مانده والین ، رفتار هموگلوبین را به قدری تغییر می دهد که منجر به بیماری سلول داسی می شود . در نهایت، ساختار چهارتایی مربوط به ساختار یک پروتئین با زیر واحدهای پپتیدی متعدد، مانند هموگلوبین با چهار زیرواحد آن است. همه پروتئین ها بیش از یک زیر واحد ندارند. [45]


پروتئین های بلعیده شده معمولاً در روده کوچک به اسیدهای آمینه یا دی پپتیدهای منفرد شکسته می شوند و سپس جذب می شوند. سپس می توان آنها را به هم متصل کرد تا پروتئین های جدید را تشکیل دهند. محصولات واسطه گلیکولیز، چرخه اسید سیتریک و مسیر پنتوز فسفات را می توان برای تشکیل هر بیست اسید آمینه استفاده کرد و اکثر باکتری ها و گیاهان دارای تمام آنزیم های لازم برای سنتز آنها هستند. با این حال، انسان و سایر پستانداران فقط نیمی از آنها را می توانند سنتز کنند. آنها نمی توانند ایزولوسین ، لوسین ، لیزین ، متیونین ، فنیل آلانین ، ترئونین ، تریپتوفان و والین را سنتز کنند . از آنجا که آنها باید بلعیده شوند، اینها اسیدهای آمینه ضروری هستند . پستانداران دارای آنزیم هایی برای سنتز آلانین ، آسپاراژین ، آسپارتات ، سیستئین ، گلوتامات ، گلوتامین ، گلیسین ، پرولین ، سرین و تیروزین ، اسیدهای آمینه غیر ضروری هستند. در حالی که آنها می توانند آرژنین و هیستیدین را سنتز کنند ، نمی توانند آن را به مقدار کافی برای حیوانات جوان و در حال رشد تولید کنند، بنابراین اینها اغلب اسیدهای آمینه ضروری در نظر گرفته می شوند.
اگر گروه آمینه از یک اسید آمینه جدا شود، یک اسکلت کربنی به نام آلفا- کتو اسید باقی میماند . آنزیم هایی به نام ترانس آمینازها می توانند به راحتی گروه آمینه را از یک آمینو اسید (که آن را به یک آلفا کتو اسید تبدیل می کنند) به یک آلفا-کتو اسید دیگر (آن را به یک اسید آمینه تبدیل می کنند) منتقل کنند. این امر در بیوسنتز اسیدهای آمینه مهم است، زیرا برای بسیاری از مسیرها، واسطههای سایر مسیرهای بیوشیمیایی به اسکلت اسید α-کتو تبدیل میشوند و سپس یک گروه آمینه، اغلب از طریق ترانس آمینو ، اضافه میشود . سپس آمینو اسیدها ممکن است برای تشکیل پروتئین به یکدیگر متصل شوند.
فرآیند مشابهی برای تجزیه پروتئین ها استفاده می شود. ابتدا به آمینو اسیدهای تشکیل دهنده آن هیدرولیز می شود. آمونیاک آزاد (NH3) که به عنوان یون آمونیوم (NH4+) در خون وجود دارد، برای اشکال حیات سمی است. بنابراین یک روش مناسب برای دفع آن باید وجود داشته باشد. تاکتیک های مختلفی در حیوانات مختلف بسته به نیاز حیوانات تکامل یافته است. موجودات تک سلولی آمونیاک را در محیط آزاد می کنند. به همین ترتیب، ماهی های استخوانی می توانند آمونیاک را در آب آزاد کنند، جایی که به سرعت رقیق می شود. به طور کلی، پستانداران آمونیاک را از طریق چرخه اوره به اوره تبدیل می کنند .
به منظور تعیین اینکه آیا دو پروتئین به هم مرتبط هستند یا به عبارت دیگر برای تصمیم گیری در مورد همولوگ بودن یا نبودن آنها، دانشمندان از روش های مقایسه توالی استفاده می کنند. روشهایی مانند همترازیهای توالی و همترازیهای ساختاری ابزارهای قدرتمندی هستند که به دانشمندان کمک میکنند تا همسانشناسی بین مولکولهای مرتبط را شناسایی کنند. ارتباط یافتن همسانی بین پروتئین ها فراتر از تشکیل یک الگوی تکاملی خانواده های پروتئینی است . با یافتن اینکه دو توالی پروتئین چقدر شبیه هم هستند، اطلاعاتی در مورد ساختار و در نتیجه عملکرد آنها به دست می آوریم.

اسیدهای نوکلئیک که به دلیل فراوانی در هسته های سلولی نامیده می شوند ، نام عمومی خانواده پلیمرهای زیستی است . آنها ماکرومولکول های بیوشیمیایی پیچیده و با وزن مولکولی بالا هستند که می توانند اطلاعات ژنتیکی را در تمام سلول های زنده و ویروس ها منتقل کنند. [2] مونومرها نوکلئوتید نامیده می شوند و هر کدام از سه جزء تشکیل شده است: یک پایه هتروسیکلیک نیتروژنی (یا یک پورین یا یک پیریمیدین )، یک قند پنتوز و یک گروه فسفات . [46]

رایج ترین اسیدهای نوکلئیک اسید دئوکسی ریبونوکلئیک (DNA) و اسید ریبونوکلئیک (RNA) هستند. گروه فسفات و قند هر نوکلئوتید با یکدیگر پیوند می خورند و ستون فقرات اسید نوکلئیک را تشکیل می دهند، در حالی که توالی بازهای نیتروژنی اطلاعات را ذخیره می کند. رایج ترین بازهای نیتروژن دار عبارتند از آدنین ، سیتوزین ، گوانین ، تیمین و اوراسیل . بازهای نیتروژنی هر رشته از یک اسید نوکلئیک پیوندهای هیدروژنی را با برخی از بازهای نیتروژنی دیگر در یک رشته مکمل اسید نوکلئیک تشکیل می دهند. آدنین با تیمین و اوراسیل، تیمین فقط با آدنین و سیتوزین و گوانین فقط به یکدیگر متصل می شوند. آدنین، تیمین و اوراسیل حاوی دو پیوند هیدروژنی هستند، در حالی که پیوندهای هیدروژنی تشکیل شده بین سیتوزین و گوانین سه پیوند است.
جدا از ماده ژنتیکی سلول، اسیدهای نوکلئیک اغلب نقشی به عنوان پیام رسان دوم دارند و همچنین مولکول پایه آدنوزین تری فسفات (ATP)، مولکول حامل انرژی اولیه موجود در همه موجودات زنده را تشکیل می دهند. همچنین، بازهای نیتروژنی ممکن در دو اسید نوکلئیک متفاوت است: آدنین، سیتوزین و گوانین در هر دو RNA و DNA وجود دارند، در حالی که تیمین فقط در DNA و اوراسیل در RNA وجود دارد.
گلوکز یک منبع انرژی در اکثر اشکال زندگی است. به عنوان مثال، پلی ساکاریدها توسط آنزیم ها به مونومرهای خود تجزیه می شوند ( گلیکوژن فسفوریلاز باقی مانده گلوکز را از گلیکوژن، یک پلی ساکارید، حذف می کند). دی ساکاریدهایی مانند لاکتوز یا ساکارز به مونوساکاریدهای دو جزء خود تقسیم می شوند. [47]
گلوکز عمدتاً توسط یک مسیر ده مرحله ای بسیار مهم به نام گلیکولیز متابولیزه می شود که نتیجه خالص آن تجزیه یک مولکول گلوکز به دو مولکول پیروات است . این همچنین یک خالص دو مولکول ATP ، واحد پول انرژی سلول ها، همراه با دو معادل کاهنده تبدیل NAD + (نیکوتین آدنین دی نوکلئوتید: شکل اکسید شده) به NADH (نیکوتین آدنین دی نوکلئوتید: شکل کاهش یافته) تولید می کند. این نیازی به اکسیژن ندارد. اگر اکسیژن در دسترس نباشد (یا سلول نتواند از اکسیژن استفاده کند)، NAD با تبدیل پیرووات به لاکتات (اسید لاکتیک) (مثلاً در انسان) یا به اتانول به اضافه دی اکسید کربن (مثلاً در مخمر ) بازیابی می شود. مونوساکاریدهای دیگر مانند گالاکتوز و فروکتوز می توانند به واسطه های مسیر گلیکولیتیک تبدیل شوند. [48]
در سلول های هوازی با اکسیژن کافی ، مانند اکثر سلول های انسانی، پیروات بیشتر متابولیزه می شود. به طور برگشت ناپذیری به استیل-CoA تبدیل می شود و یک اتم کربن را به عنوان محصول زائد دی اکسید کربن تولید می کند و معادل کاهش دهنده دیگری به عنوان NADH تولید می کند . دو مولکول استیل کوآ (از یک مولکول گلوکز) سپس وارد چرخه اسید سیتریک می شوند و دو مولکول ATP، شش مولکول NADH دیگر و دو کینون احیا شده (از طریق FADH 2 به عنوان کوفاکتور متصل به آنزیم) تولید می کنند و آزاد می شوند. اتم های کربن باقی مانده به عنوان دی اکسید کربن. مولکولهای NADH و کینول تولید شده سپس وارد مجتمعهای آنزیمی زنجیره تنفسی میشوند، یک سیستم انتقال الکترون که الکترونها را در نهایت به اکسیژن منتقل میکند و انرژی آزاد شده را به شکل شیب پروتون بر روی یک غشاء حفظ میکند ( غشای میتوکندری داخلی در یوکاریوتها). بنابراین، اکسیژن به آب کاهش می یابد و گیرنده های الکترون اصلی NAD + و کینون بازسازی می شوند. به همین دلیل است که انسان اکسیژن را تنفس می کند و دی اکسید کربن را خارج می کند. انرژی آزاد شده از انتقال الکترون ها از حالت های پرانرژی در NADH و کینول ابتدا به عنوان گرادیان پروتون حفظ می شود و از طریق سنتاز ATP به ATP تبدیل می شود. این 28 مولکول اضافی ATP تولید می کند (24 مولکول از 8 NADH + 4 از 2 کینول)، که در مجموع به 32 مولکول ATP حفظ می شود در هر گلوکز تجزیه شده (دو مورد از گلیکولیز + دو مولکول از چرخه سیترات). [49] واضح است که استفاده از اکسیژن برای اکسید کردن کامل گلوکز انرژی بسیار بیشتری را نسبت به هر ویژگی متابولیکی مستقل از اکسیژن به ارگانیسم میدهد، و تصور میشود که این دلیلی است که زندگی پیچیده تنها پس از انباشته شدن مقادیر زیادی اکسیژن در جو زمین ظاهر شد.
در مهره داران ، ماهیچه های اسکلتی که به شدت منقبض می شوند (مثلاً در حین وزنه برداری یا دوی سرعت) اکسیژن کافی برای پاسخگویی به نیاز انرژی دریافت نمی کنند و بنابراین به متابولیسم بی هوازی تبدیل می شوند و گلوکز را به لاکتات تبدیل می کنند. ترکیب گلوکز از منشا غیر کربوهیدراتی مانند چربی و پروتئین. این تنها زمانی اتفاق می افتد که ذخایر گلیکوژن در کبد فرسوده شود. این مسیر یک معکوس اساسی از گلیکولیز از پیرووات به گلوکز است و می تواند از منابع بسیاری مانند اسیدهای آمینه، گلیسرول و چرخه کربس استفاده کند . کاتابولیسم پروتئین و چربی در مقیاس بزرگ معمولاً زمانی اتفاق میافتد که افرادی از گرسنگی یا برخی اختلالات غدد درون ریز رنج میبرند. [50] کبد با استفاده از فرآیندی به نام گلوکونئوژنز ، گلوکز را بازسازی می کند . این فرآیند کاملاً برعکس گلیکولیز نیست و در واقع به سه برابر انرژی بدست آمده از گلیکولیز نیاز دارد (شش مولکول ATP در مقایسه با دو مولکول بدست آمده در گلیکولیز استفاده می شود). مشابه واکنشهای فوق، گلوکز تولید شده میتواند در بافتهایی که به انرژی نیاز دارند، گلیکولیز شود، به عنوان گلیکوژن (یا نشاسته در گیاهان) ذخیره شود، یا به مونوساکاریدهای دیگر تبدیل شود یا به دی یا الیگوساکاریدها ملحق شود. مسیرهای ترکیبی گلیکولیز در طول ورزش، عبور لاکتات از طریق جریان خون به کبد، گلوکونئوژنز متعاقب آن و انتشار گلوکز در جریان خون، چرخه کوری نامیده می شود . [51]

محققان در بیوشیمی از تکنیکهای خاص بومی بیوشیمی استفاده میکنند، اما به طور فزایندهای این تکنیکها و ایدههای توسعهیافته در زمینههای ژنتیک ، زیستشناسی مولکولی و بیوفیزیک را ترکیب میکنند . مرز مشخصی بین این رشته ها وجود ندارد. بیوشیمی شیمی مورد نیاز برای فعالیت بیولوژیکی مولکول ها را مطالعه می کند، زیست شناسی مولکولی فعالیت بیولوژیکی آنها را مطالعه می کند، ژنتیک به مطالعه وراثت آنها می پردازد که اتفاقاً توسط ژنوم آنها حمل می شود . این در شماتیک زیر نشان داده شده است که یک نمای احتمالی از روابط بین فیلدها را نشان می دهد:
{{cite book}}: CS1 maint: multiple names: authors list (link)