بیماری سلول داسی شکل ( SCD ) که به سادگی سلول داسی نیز نامیده می شود ، گروهی از اختلالات خونی مرتبط با هموگلوبین است که معمولاً به ارث می رسد . [2] شایع ترین نوع آن به عنوان کم خونی داسی شکل شناخته می شود . [2] منجر به ناهنجاری در هموگلوبین پروتئین حامل اکسیژن موجود در گلبول های قرمز می شود . [2] این منجر به شکلی سفت و داس مانند در شرایط خاص می شود. [2] مشکلات در بیماری سلول داسی شکل معمولاً در حدود 5 تا 6 ماهگی شروع می شود. [1] تعدادی از مشکلات سلامتی ممکن است ایجاد شود، مانند حملات درد (معروف به بحران سلول داسی شکل ) در مفاصل، کم خونی ، تورم در دست ها و پاها، عفونت های باکتریایی ، سرگیجه [9] و سکته مغزی . [1] درد طولانی مدت ممکن است با بالا رفتن سن افراد ایجاد شود. [2] میانگین امید به زندگی در کشورهای توسعه یافته 40 تا 60 سال است. اغلب با افزایش سن بدتر می شود. [10] همه اندام های اصلی تحت تأثیر بیماری سلول داسی قرار می گیرند. کبد، قلب، کلیهها، کیسه صفرا، چشمها، استخوانها و مفاصل نیز میتوانند از عملکرد غیرطبیعی سلولهای داسی و ناتوانی آنها در جریان صحیح در رگهای خونی کوچک آسیب ببینند. [11]
بیماری سلول داسی شکل زمانی رخ می دهد که فرد دو نسخه غیر طبیعی از ژن β-گلوبین ( HBB ) که هموگلوبین را می سازد، به ارث می برد، یکی از هر یک از والدین. [3] این ژن در کروموزوم 11 وجود دارد . [12] بسته به جهش دقیق در هر ژن هموگلوبین، چندین زیرگروه وجود دارد. [2] حمله را می توان با تغییرات دما، استرس، کم آبی و ارتفاع زیاد آغاز کرد. [1] فردی که دارای یک نسخه غیرطبیعی است معمولاً علائمی ندارد و گفته میشود که دارای صفت سلول داسی است . [3] به چنین افرادی ناقل نیز گفته می شود . [5] تشخیص با آزمایش خون است ، و برخی از کشورها همه نوزادان را در بدو تولد برای این بیماری آزمایش میکنند. [4] تشخیص در دوران بارداری نیز امکان پذیر است. [4]
مراقبت از افراد مبتلا به بیماری سلول داسی شکل ممکن است شامل پیشگیری از عفونت با واکسیناسیون و آنتی بیوتیک ها ، مصرف زیاد مایعات، مکمل اسید فولیک و داروهای ضد درد باشد . [5] [6] اقدامات دیگر ممکن است شامل انتقال خون و داروی هیدروکسی کاربامید (هیدروکسی اوره) باشد. [6] در سال 2023، ژن درمانی جدید تایید شد. [13] [14] درصد کمی از افراد را می توان با پیوند سلول های مغز استخوان درمان کرد .
تا سال 2015 [به روز رسانی]، حدود 4.4 میلیون نفر به بیماری سلول داسی شکل مبتلا هستند، در حالی که 43 میلیون نفر دیگر دارای ویژگی سلول داسی هستند. [7] [15] اعتقاد بر این است که حدود 80٪ موارد بیماری سلول داسی شکل در جنوب صحرای آفریقا رخ می دهد . [16] همچنین به میزان کمتری در بخشهایی از هند ، اروپای جنوبی ، غرب آسیا ، شمال آفریقا و در میان مردم آفریقایی منشاء (در جنوب صحرا) که در سایر نقاط جهان زندگی میکنند، دیده میشود. [17] در سال 2015، حدود 114800 کشته برجای گذاشت. [8] این بیماری برای اولین بار در ادبیات پزشکی توسط پزشک آمریکایی جیمز بی. هریک در سال 1910 توصیف شد. [18] [19] در سال 1949، انتقال ژنتیکی آن توسط EA Beet و JV Neel تعیین شد. [19] در سال 1954، اثر محافظتی در برابر مالاریا صفت سلول داسی شکل توصیف شد. [19]
_(14768428942).jpg/440px-The_diseases_of_infancy_and_childhood_(1920)_(14768428942).jpg)


علائم بیماری سلول داسی شکل معمولا در اوایل کودکی شروع می شود. شدت علائم می تواند از فردی به فرد دیگر متفاوت باشد، همچنین فراوانی رویدادهای بحران نیز متفاوت است. [20] [16] بیماری سلول داسی شکل ممکن است منجر به عوارض حاد و مزمن مختلفی شود که تعدادی از آنها میزان مرگ و میر بالایی دارند. [21]
ویژگی های معمول اولین رویدادی که منجر به تشخیص SCD می شود به سن کودک بستگی دارد. هنگامی که بیماری در سال اول زندگی خود را نشان می دهد، شایع ترین مشکل یک دوره درد و تورم در دست و پا است که به عنوان داکتیلیت یا "سندرم دست و پا" شناخته می شود. رنگ پریدگی، زردی و خستگی نیز می تواند از علائم اولیه کم خونی ناشی از بیماری سلول داسی شکل باشد. [22]
تقریباً نیمی از بیماران SCD اتوزوم مغلوب کلاسیک تا پنج سالگی یا بیشتر دچار بحران نمی شوند. [22] برخی از این بیماران و برخی دیگر که دارای ژنوتیپهای دیگر هستند، ممکن است فقط در شرایط هیپوکسی متوسط تا شدید با علائم ظاهر شوند و بنابراین ممکن است تا اواخر عمر از ابتلای خود به این بیماری غافل باشند. [16] در میان کودکان بزرگتر از 2 سال، شایع ترین تظاهرات اولیه یک رویداد دردناک از نوع عمومی یا متغیر است، و یک نسخه کمی کمتر شایع به عنوان یک رویداد درد حاد قفسه سینه ظاهر می شود. داکتیلیت به ندرت یا هرگز در کودکان بزرگتر از 2 سال رخ نمی دهد. [22]
اصطلاحات "بحران سلول داسی شکل" یا "بحران داسی شکل" ممکن است برای توصیف چندین وضعیت حاد مستقل در بیماران مبتلا به SCD استفاده شود که منجر به کم خونی و بحران هایی می شود که می تواند انواع مختلفی داشته باشد، از جمله بحران انسداد عروق ، بحران آپلاستیک ، بحران جداسازی طحال ، بحران همولیتیک ، و غیره. علائم اولیه [23] رنگ زرد پوست یا سفیدی چشم است که زمانی ظاهر می شود که تعداد زیادی گلبول قرمز تحت همولیز قرار می گیرند. اکثر دوره های بحران سلول داسی بین پنج تا هفت روز طول می کشد. [24] "اگرچه عفونت، کم آبی، و اسیدوز (که همگی به سود داسی شدن هستند) می توانند به عنوان محرک عمل کنند، در بیشتر موارد، هیچ علت مستعد کننده ای شناسایی نشده است." [25]
بحران انسداد عروق توسط گلبولهای قرمز داسی شکل ایجاد میشود که مویرگها را مسدود میکنند و جریان خون را به یک اندام محدود میکنند و منجر به ایسکمی ، درد ، نکروز و اغلب آسیبهای اندام میشوند. فراوانی، شدت و مدت این بحران ها به طور قابل توجهی متفاوت است. بحران های دردناک با هیدراتاسیون، مسکن ها و تزریق خون درمان می شوند . مدیریت درد نیاز به تجویز داروهای مخدر در فواصل منظم تا زمانی که بحران برطرف شود، دارد. برای بحرانهای خفیفتر، زیر گروهی از بیماران داروهای ضدالتهابی غیراستروئیدی مانند دیکلوفناک یا ناپروکسن را مدیریت میکنند . برای بحرانهای شدیدتر، اکثر بیماران نیاز به مدیریت بستری برای اپیوئیدهای داخل وریدی دارند. معمولاً در این محیط از دستگاههای بیدردی کنترلشده توسط بیمار استفاده میشود. بحران انسداد عروقی که اعضایی مانند آلت تناسلی [26] یا ریه ها را درگیر می کند یک اورژانس در نظر گرفته می شود و با تزریق گلبول های قرمز درمان می شود. اسپیرومتری انگیزشی ، تکنیکی برای تشویق تنفس عمیق برای به حداقل رساندن ایجاد آتلکتازی ، توصیه می شود. [27]
طحال اغلب در بیماری سلول داسی شکل تحت تأثیر قرار می گیرد، زیرا گلبول های قرمز داسی شکل باعث باریک شدن رگ های خونی و کاهش عملکرد در پاکسازی سلول های معیوب می شود . [28] معمولاً قبل از پایان دوران کودکی در افراد مبتلا به کم خونی سلول داسی شکل انفارکتوس می شود. این آسیب طحال خطر عفونت از ارگانیسم های محصور شده را افزایش می دهد . [29] [30] آنتی بیوتیک ها و واکسیناسیون های پیشگیرانه برای کسانی که عملکرد مناسب طحال ندارند توصیه می شود .
بحرانهای جداسازی طحال، بزرگ شدن حاد و دردناک طحال است که در اثر گیر افتادن سلولهای قرمز درون طحال و در نتیجه کاهش شدید سطح هموگلوبین با پتانسیل شوک هیپوولمیک ایجاد میشود . بحران های جداسازی به عنوان یک وضعیت اضطراری در نظر گرفته می شود. در صورت عدم درمان، بیماران ممکن است در عرض 1 تا 2 ساعت به دلیل نارسایی گردش خون بمیرند. مدیریت حمایتی است، گاهی اوقات با انتقال خون. [31] این بحران ها گذرا هستند. آنها برای 3-4 ساعت ادامه می یابند و ممکن است برای یک روز ادامه داشته باشند. [32]
سندرم حاد قفسه سینه با حداقل دو مورد از این علائم یا علائم تعریف می شود: درد قفسه سینه، تب، ارتشاح ریوی یا ناهنجاری کانونی، علائم تنفسی یا هیپوکسمی. [27] این دومین عارضه شایع است و حدود 25 درصد از مرگ و میرها در بیماران مبتلا به SCD را تشکیل می دهد. اکثر موارد با بحران های انسداد عروقی تظاهر می کنند و سپس دچار سندرم حاد قفسه سینه می شوند. [33] [34] با این وجود، حدود 80٪ از مردم در طول سندرم حاد قفسه سینه دچار بحرانهای انسداد عروقی میشوند. [35]
بحران آپلاستیک مواردی از بدتر شدن حاد کم خونی پایه بیمار، ایجاد ظاهر رنگ پریده ، ضربان قلب سریع و خستگی است. این بحران معمولاً توسط پاروویروس B19 ایجاد می شود که مستقیماً بر تولید گلبول های قرمز با حمله به پیش سازهای گلبول قرمز و تکثیر و از بین بردن آنها تأثیر می گذارد. [36] عفونت پاروویروس [37] تقریباً به طور کامل از تولید گلبول های قرمز برای دو تا سه روز جلوگیری می کند. در افراد عادی، این نتیجه چندانی ندارد، اما کوتاه شدن عمر گلبول های قرمز بیماران SCD منجر به یک وضعیت ناگهانی و تهدید کننده زندگی می شود. تعداد رتیکولوسیت ها در طول بیماری به طور چشمگیری کاهش می یابد (باعث رتیکولوسیتوپنی می شود )، و گردش سریع گلبول های قرمز منجر به افت هموگلوبین می شود. این بحران چهار تا هفت روز طول می کشد تا از بین برود. اکثر بیماران را می توان به صورت حمایتی مدیریت کرد. برخی نیاز به تزریق خون دارند. [38]
بحران های همولیتیک افت حاد تسریع در سطح هموگلوبین است. گلبول های قرمز خون با سرعت بیشتری تجزیه می شوند. این امر به ویژه در افراد مبتلا به کمبود G6PD رایج است . [39] یکی دیگر از تأثیرات بحران های همولیتیک در بیماری سلول داسی، استرس اکسیداتیو بر گلبول های قرمز، لکوسیت ها و پلاکت ها است. زمانی که تولید گلبول قرمز به اندازه کافی در مغز استخوان وجود نداشته باشد، اکسیژنی که بدن دریافت، پردازش و انتقال می دهد با آنتی اکسیدان های بدن نامتعادل می شود. عدم تعادل در گونههای فعال اکسیژن در سلولها وجود دارد که منجر به تولید بیشتر گلبولهای قرمز خونی میشود که به درستی اکسیژن یا تشکیل نشدهاند. استرس اکسیداتیو به دلیل عدم تعادل اکسیژن در بافت ممکن است منجر به کم خونی شود. [40]
مدیریت کمکی است، گاهی اوقات با انتقال خون. [27]
یکی از اولین تظاهرات بالینی داکتیلیت است که در اوایل شش ماهگی ظاهر می شود و ممکن است در کودکان دارای صفت سلول داسی شکل رخ دهد. [41] بحران می تواند تا یک ماه ادامه یابد. [42] با توجه به اینکه پنومونی و داسی شدن در ریه هر دو می توانند علائم سندرم حاد قفسه سینه را ایجاد کنند، بیمار برای هر دو بیماری تحت درمان قرار می گیرد. [43] ممکن است با بحران دردناک، عفونت تنفسی، آمبولیزاسیون مغز استخوان، یا احتمالاً با آتلکتازی، تجویز مواد افیونی یا جراحی ایجاد شود. [44] زخم های خونساز نیز ممکن است رخ دهد. [45]
کم خونی داسی شکل می تواند منجر به عوارض مختلفی شود، از جمله:



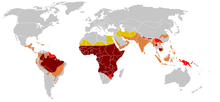
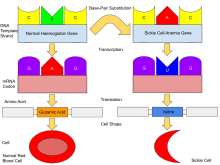
به طور معمول، انسان دارای هموگلوبین A است که از دو زنجیره آلفا و دو زنجیره بتا، هموگلوبین A2 که از دو زنجیره آلفا و دو زنجیره دلتا تشکیل شده و هموگلوبین F (HbF) که از دو زنجیره آلفا و دو زنجیره گاما تشکیل شده است، در بدن خود دارند. از این سه نوع، هموگلوبین F تا حدود 6 هفتگی غالب است. پس از آن، هموگلوبین A در طول زندگی غالب می شود. [63] در افراد مبتلا به بیماری سلول داسی شکل، حداقل یکی از زیرواحدهای β-گلوبین در هموگلوبین A با چیزی که به نام هموگلوبین S شناخته می شود جایگزین می شود. در کم خونی سلول داسی شکل، شکل رایج بیماری سلول داسی، هموگلوبین S جایگزین هر دو می شود. زیرواحدهای β-گلوبین در هموگلوبین. [20]
بیماری سلول داسی شکل دارای الگوی توارث اتوزومال مغلوب از والدین است. [64] انواع هموگلوبین که یک فرد در گلبول های قرمز می سازد بستگی به ژن های هموگلوبین دارد که از او یا والدینش به ارث می رسد. اگر یکی از والدین مبتلا به کم خونی سلول داسی شکل باشد و دیگری دارای صفت سلول داسی شکل باشد، در این صورت هر کودک معینی 50 درصد احتمال ابتلا به بیماری سلول داسی شکل و 50 درصد احتمال ابتلا به ویژگی سلول داسی دارد. وقتی هر دو والدین دارای صفت سلول داسی شکل باشند، هر کودک معینی 25 درصد احتمال ابتلا به بیماری سلول داسی دارد. 25% احتمال عدم وجود آلل سلول داسی شکل و 50% احتمال بیماری هتروزیگوت. [65] [66] [ منبع پزشکی غیر قابل اعتماد؟ ]
جهش ژن سلول داسی احتمالاً به طور خود به خود در مناطق مختلف جغرافیایی ایجاد شده است، [67] همانطور که توسط تجزیه و تحلیل اندونوکلئاز محدود پیشنهاد می شود. این گونه ها با نام های کامرون، سنگال، بنین، بانتو و عربستانی-آسیایی شناخته می شوند. اهمیت بالینی آنها به این دلیل است که برخی از آنها با سطوح بالاتر HbF مرتبط هستند، به عنوان مثال، انواع سنگال و عربستان سعودی-آسیایی، و تمایل به بیماری خفیف تری دارند. [68]
نقص ژن یک جهش تک نوکلئوتیدی (نگاه کنید به پلی مورفیسم تک نوکلئوتیدی - SNP) ( کدون GAG که به GTG تغییر می کند) ژن β-گلوبین است که منجر به جایگزینی گلوتامات (E/Glu) توسط والین (V/Val) می شود. موقعیت 6 (تعویض E6V). [69] [یادداشت 1] هموگلوبین S با این جهش به عنوان HbS نامیده می شود، برخلاف HbA بالغ طبیعی. این جهش معمولاً یک جهش خوش خیم است و در شرایط غلظت طبیعی اکسیژن هیچ اثر آشکاری بر ساختارهای ثانویه ، سوم یا چهارم هموگلوبین ایجاد نمی کند . با این حال، تحت غلظت کم اکسیژن ، HbS پلیمریزه می شود و رسوبات فیبری تشکیل می دهد، زیرا شکل دئوکسی هموگلوبین یک لکه آبگریز را روی پروتئین بین مارپیچ های E و F نشان می دهد (Phe 85، Leu 88). [70]
در افراد هتروزیگوت برای HbS ( ناقل هموگلوبین داسی شکل)، مشکلات پلیمریزاسیون جزئی است زیرا آلل طبیعی می تواند نیمی از هموگلوبین را تولید کند. در افراد هموزیگوت برای HbS، وجود پلیمرهای با زنجیره بلند HbS، شکل گلبول قرمز را از شکلی صاف و شبیه دونات به ناهموار و پر از خوشه تغییر میدهد و آن را شکننده و مستعد شکستن درون مویرگها میکند . ناقلین تنها در صورت کمبود اکسیژن (مثلاً در هنگام بالا رفتن از کوه) یا زمانی که به شدت کم آب باشند ، علائم را نشان می دهند . [ نیازمند منبع ]
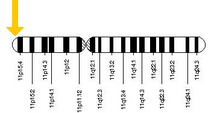
آلل مسئول کم خونی داسی شکل را می توان در بازوی کوتاه کروموزوم 11 ، به طور خاص تر 11p15.5 یافت. فردی که ژن معیوب را از پدر و مادر دریافت می کند به این بیماری مبتلا می شود. فردی که یک آلل معیوب و یک آلل سالم دریافت می کند سالم می ماند، اما می تواند بیماری را منتقل کند و به عنوان ناقل یا هتروزیگوت شناخته می شود. هتروزیگوت ها هنوز هم می توانند به مالاریا مبتلا شوند، اما علائم آنها عموماً شدت کمتری دارند. [71]
با توجه به مزیت تطبیقی هتروزیگوت، این بیماری همچنان شایع است، به ویژه در میان افرادی که اجداد اخیر در مناطق مالاریا زده، مانند آفریقا ، مدیترانه ، هند و خاورمیانه دارند . [72] مالاریا از نظر تاریخی در جنوب اروپا بومی بود، اما در اواسط قرن بیستم ریشه کن شد، به استثنای موارد پراکنده نادر. [73]
انگل مالاریا چرخه زندگی پیچیده ای دارد و بخشی از آن را در گلبول های قرمز خون می گذراند. در یک ناقل، وجود انگل مالاریا باعث می شود گلبول های قرمز خون با هموگلوبین معیوب پاره شوند و انگل پلاسمودیوم قادر به تولید مثل نباشد. علاوه بر این، پلیمریزاسیون Hb در وهله اول بر توانایی انگل برای هضم Hb تأثیر می گذارد. بنابراین، در مناطقی که مالاریا یک مشکل است، شانس زنده ماندن افراد در صورت داشتن صفات سلول داسی شکل (انتخاب برای هتروزیگوت) در واقع افزایش می یابد. [ نیازمند منبع ]
در ایالات متحده، بدون مالاریا بومی، شیوع کم خونی داسی شکل در میان افراد با اصل و نسب آفریقایی کمتر (حدود 0.25٪) نسبت به مردم غرب آفریقا (حدود 4.0٪) است و در حال کاهش است. بدون مالاریا بومی، جهش سلول داسی کاملاً زیان آور است و در جمعیت آسیب دیده با انتخاب طبیعی کاهش می یابد و اکنون به صورت مصنوعی از طریق غربالگری ژنتیکی قبل از تولد . با این حال، جامعه آفریقایی آمریکایی از چندین گروه قومی آفریقایی و غیر آفریقایی از جمله بردگان آمریکایی تبار است. بنابراین، درجه ای از رقیق شدن ژنتیکی از طریق تلاقی با افراد غیر آفریقایی و فشار انتخابی بهداشتی بالا از طریق برده داری (به ویژه تجارت برده و اغلب کشنده ترین پاساژ میانی ) ممکن است معقول ترین توضیح برای شیوع کمتر کم خونی سلول داسی شکل باشد (و ، احتمالاً سایر بیماری های ژنتیکی) در بین آمریکایی های آفریقایی تبار در مقایسه با غرب آفریقا. عامل دیگری که گسترش ژن های سلول داسی شکل را در آمریکای شمالی محدود می کند، عدم وجود نسبی چندهمسری است . در جوامع چندهمسری، مردان مبتلا ممکن است دارای فرزندان زیادی با چندین همسر باشند. [74]
از دست دادن خاصیت ارتجاعی گلبول های قرمز در پاتوفیزیولوژی بیماری سلول داسی شکل مرکزی است. گلبول های قرمز معمولی کاملاً الاستیک هستند و شکل دیسکی دو مقعر دارند که به سلول ها اجازه می دهد برای عبور از مویرگ ها تغییر شکل دهند. [75] در بیماری سلول داسی، تنش کم اکسیژن باعث افزایش داسی شدن گلبول های قرمز می شود و دوره های مکرر داسی شدن به غشای سلولی آسیب می رساند و خاصیت ارتجاعی سلول را کاهش می دهد. این سلولها وقتی تنش طبیعی اکسیژن بازیابی میشود، نمیتوانند به شکل طبیعی بازگردند. در نتیجه، این سلول های خونی سفت و سخت قادر به تغییر شکل در هنگام عبور از مویرگ های باریک نیستند که منجر به انسداد عروق و ایسکمی می شود . [ نیازمند منبع ]
کم خونی واقعی این بیماری ناشی از همولیز ، تخریب گلبول های قرمز، به دلیل شکل آنها است. اگرچه مغز استخوان تلاش می کند تا با ایجاد گلبول های قرمز جدید جبران کند، اما با سرعت تخریب مطابقت ندارد. [76] گلبولهای قرمز سالم معمولاً 90 تا 120 روز کار میکنند، اما سلولهای داسی شکل تنها 10 تا 20 روز دوام میآورند. [77]
در HbS، شمارش کامل خون سطوح هموگلوبین را در محدوده 6-8 گرم در دسی لیتر با تعداد رتیکولوسیت بالا نشان می دهد (زیرا مغز استخوان با تولید گلبول های قرمز بیشتر، تخریب سلول های داسی شکل را جبران می کند). در سایر اشکال بیماری سلول داسی شکل، سطح Hb بیشتر است. یک فیلم خون ممکن است ویژگی های هیپوسپلنیسم ( سلول های هدف و اجسام هاول-ژولی ) را نشان دهد. [78]
داسی شدن گلبول های قرمز روی یک لایه خونی را می توان با افزودن متابی سولفیت سدیم القا کرد . وجود هموگلوبین داسی را می توان با "آزمایش حلالیت داسی" (که "سیکلدکس" نیز نامیده می شود) نشان داد. [79] مخلوطی از هموگلوبین S (HbS) در یک محلول احیا کننده (مانند دی تیونیت سدیم ) ظاهری کدر می دهد، در حالی که Hb معمولی یک محلول شفاف می دهد. [80]
اشکال غیرطبیعی هموگلوبین را می توان در الکتروفورز هموگلوبین ، شکلی از الکتروفورز ژل که در آن انواع مختلف هموگلوبین با سرعت های متفاوتی حرکت می کنند، تشخیص داد. هموگلوبین داسی شکل (HgbS) و هموگلوبین C با داسی شکل (HgbSC) - دو شکل رایج - از آنجا قابل شناسایی هستند. تشخیص را می توان با کروماتوگرافی مایع با کارایی بالا تایید کرد . آزمایش ژنتیکی به ندرت انجام می شود، زیرا سایر تحقیقات برای HbS و HbC بسیار اختصاصی هستند. [81]
بحران سلول داسی شکل حاد اغلب با عفونت ایجاد می شود. بنابراین، آزمایش ادرار برای تشخیص عفونت مخفی دستگاه ادراری و رادیوگرافی قفسه سینه برای بررسی پنومونی پنهان باید به طور معمول انجام شود. [82]
افرادی که ناقلین شناخته شده بیماری هستند یا در معرض خطر داشتن فرزند مبتلا به کم خونی داسی شکل هستند، ممکن است تحت مشاوره ژنتیک قرار گیرند . مشاوران ژنتیک با خانواده ها کار می کنند تا در مورد مزایا، محدودیت ها و تدارکات گزینه های آزمایش ژنتیک و همچنین تأثیر بالقوه آزمایش و نتایج آزمایش بر روی فرد بحث کنند. [83] [84] در طول بارداری، آزمایش ژنتیکی را می توان بر روی نمونه خون جنین یا نمونه مایع آمنیوتیک انجام داد . در طول سه ماهه اول بارداری، نمونه برداری از پرزهای کوریونی (CVS) نیز تکنیکی است که برای تشخیص قبل از تولد SCD استفاده می شود. [85] از آنجایی که گرفتن نمونه خون از جنین خطرات بیشتری دارد، معمولاً از آزمایش دوم استفاده می شود. غربالگری نوزادان که گاهی اوقات به عنوان غربالگری نوزادان شناخته می شود ، نه تنها روشی برای تشخیص زودهنگام برای افراد مبتلا به بیماری سلول داسی شکل فراهم می کند، بلکه امکان شناسایی گروه هایی از افرادی که دارای ویژگی سلول داسی هستند را نیز فراهم می کند. [86] مشاوران ژنتیک می توانند به افراد رنگین پوست و خانواده هایشان کمک کنند تا با تفاوت های نژادی و قومیتی که در مراقبت های بهداشتی وجود دارد مقابله کنند. [87]
در سال 2010، بررسی ها و بحث های قابل توجهی در مورد غربالگری جامع ورزشکاران برای SCD در ایالات متحده وجود داشت. [88] [89] [90] [91] در سال 2012، انجمن هماتولوژی آمریکا به این نتیجه رسید که آنها از آزمایش یا افشای وضعیت صفت سلول داسی به عنوان پیش نیاز شرکت در فعالیت های ورزشی به دلیل عدم وجود شواهد علمی، ناسازگاری حمایت نمی کنند. با عملکرد خوب پزشکی، و ناسازگاری با اخلاق بهداشت عمومی. آنها مداخلات جهانی را برای کاهش صدمات و مرگ و میر ناشی از فعالیت توصیه کردند که برای همه ورزشکاران صرف نظر از وضعیت سلول داسی شکل آنها مؤثر است. [92]
درمان شامل تعدادی اقدامات است. در حالی که از لحاظ تاریخی توصیه شده است که افراد مبتلا به بیماری سلول داسی شکل از ورزش اجتناب کنند، ورزش منظم ممکن است برای افراد مفید باشد. [93] از کم آبی بدن باید اجتناب شود. [94] رژیم غذایی سرشار از کلسیم توصیه می شود [95] اما اثربخشی مکمل ویتامین D نامشخص است. [96] استفاده از ال-گلوتامین توسط FDA از سن 5 سالگی حمایت شد، زیرا عوارض را کاهش می دهد. [97]
از بدو تولد تا پنج سالگی، پنی سیلین روزانه، به دلیل سیستم ایمنی نابالغ که آنها را مستعد ابتلا به بیماری های اولیه دوران کودکی می کند، توصیه می شود. [98] مکمل غذایی اسید فولیک قبلاً توسط WHO توصیه شده بود. [5] بررسی کاکرین در سال 2016 در مورد استفاده از آن نشان داد که «اثر مکملها بر کمخونی و هرگونه علائم کمخونی نامشخص است» به دلیل فقدان شواهد پزشکی. [99]

اثر محافظتی صفت سلول داسی شکل برای افراد مبتلا به بیماری سلول داسی صدق نمی کند. در واقع، آنها در برابر مالاریا آسیب پذیرتر هستند، زیرا شایع ترین علت بحران های دردناک در کشورهای مالاریا، عفونت با مالاریا است. افراد مبتلا به بیماری سلول داسی شکل که در کشورهای مالاریا زندگی می کنند باید برای پیشگیری از داروهای مادام العمر استفاده کنند . [100]
اکثر افراد مبتلا به بیماری سلول داسی شکل، دوره های شدید دردناکی به نام بحران های انسداد عروق دارند. با این حال، فراوانی، شدت و مدت این بحران ها بسیار متفاوت است. بحران های دردناک به طور علامتی با داروهای مسکن درمان می شوند . مدیریت درد نیاز به تجویز داروهای مخدر در فواصل منظم تا زمانی که بحران برطرف شود، دارد. برای بحرانهای خفیفتر، زیرگروهی از بیماران داروهای NSAID (مانند دیکلوفناک یا ناپروکسن ) را درمان میکنند. برای بحران های شدیدتر، اکثر بیماران نیاز به مدیریت بستری برای داروهای مخدر داخل وریدی دارند. [101]
مایعات اضافی که به صورت خوراکی یا داخل وریدی تجویز میشوند، بخشی از درمان بحرانهای انسداد عروق هستند، اما شواهد در مورد مؤثرترین مسیر، مقدار و نوع جایگزینی مایع نامشخص است. [102]
در سال 2019، Crizanlizumab ، یک هدف آنتی بادی مونوکلونال نسبت به p-selectin در ایالات متحده تایید شد تا دفعات بحران انسداد عروق را در افراد 16 سال و بالاتر کاهش دهد. [103]
سونوگرافی داپلر ترانس کرانیال (TCD) می تواند کودکان مبتلا به سلول داسی شکل را که در معرض خطر بالای سکته هستند، تشخیص دهد. آزمایش اولتراسوند رگهای خونی را که تا حدی توسط سلولهای داسی شکل مسدود شده است، با اندازهگیری سرعت خون در مغز تشخیص میدهد، زیرا سرعت جریان خون با قطر شریان رابطه معکوس دارد و در نتیجه، سرعت بالای جریان خون با باریک شدن شریانها مرتبط است. [104] در سال 2002، مؤسسه ملی بهداشت (NIH) بیانیهای صادر کرد که در آن توصیه میکرد که کودکان مبتلا به سلول داسیشکل سالانه سونوگرافی داپلر ترانس کرانیال را دریافت کنند، و در سال 2014، هیئتی از کارشناسان که توسط NIH تشکیل شد دستورالعملهایی را صادر کردند که همان توصیه را تکرار میکردند. یک بررسی سوابق پزشکی، توسط دکتر جولی کانتر، هماتولوژیست در دانشگاه آلاباما در بیرمنگام، نشان داد که به طور متوسط تنها 48.4 درصد از کودکان مبتلا به سلول داسی شکل، آزمایش اولتراسوند توصیه شده را انجام می دهند. [105]
یک مطالعه NIH در سال 1994 نشان داد که کودکان در معرض خطر سکته مغزی که تزریق خون دریافت کردند، میزان سکته مغزی سالانه کمتر از 1 درصد داشتند، در حالی که کودکانی که تزریق خون دریافت نکردند، 10 درصد نرخ سکته در سال داشتند. ( همچنین به مطالعه 1998 در مجله پزشکی نیوانگلند مراجعه کنید ) . دستورالعمل های NIH که در سال 2014 منتشر شد، بیان می کند که همه کودکان و نوجوانان باید هیدروکسی اوره مصرف کنند، همانطور که بزرگسالان با عوارض جدی یا سه یا بیشتر بحران درد در یک سال باید از هیدروکسی اوره استفاده کنند. [105]
مدیریت مشابه بحران انسداد عروق است، با افزودن آنتی بیوتیک ها (معمولاً یک کینولون یا ماکرولید، زیرا تصور می شود باکتری های کمبود دیواره سلولی ["آتیپیک"] در ایجاد سندرم نقش دارند)، [106] مکمل اکسیژن برای هیپوکسی ، و مشاهده نزدیک در غیاب شواهد با کیفیت بالا در مورد اثربخشی آنتی بیوتیک ها برای سندرم حاد قفسه سینه در افراد مبتلا به بیماری سلول داسی شکل، هیچ درمان استاندارد آنتی بیوتیکی از سال 2019 وجود ندارد. [107] توصیه می شود افراد مشکوک به سندرم حاد قفسه سینه باید بستری شوند. بیمارستان با شیب Aa وخیم تر، نشانه ای برای پذیرش در ICU. [27]
اگر انفیلتراسیون ریوی بدتر شود یا نیاز به اکسیژن افزایش یابد، تزریق خون ساده یا تعویض خون نشان داده می شود. دومی شامل تبادل بخش قابل توجهی از توده گلبول قرمز فرد با گلبول های قرمز طبیعی است که باعث کاهش سطح هموگلوبین S در خون بیمار می شود. با این حال، در حال حاضر شواهد نامشخصی در مورد فواید یا مضرات احتمالی انتقال خون برای سندرم حاد قفسه سینه در افراد مبتلا به بیماری سلول داسی شکل وجود دارد. [108]
هیدروکسی اوره که به نام هیدروکسی کاربامید نیز شناخته می شود ، احتمالاً دفعات دوره های دردناک و خطر بیماری یا مرگ تهدید کننده زندگی را کاهش می دهد، اما در حال حاضر شواهد کافی در مورد خطر عوارض جانبی وجود ندارد. [109] ترکیب هیدروکسی اوره و فلبوتومی ممکن است از نظر درد، بیماری های تهدید کننده زندگی و خطر مرگ موثرتر از انتقال خون و شلیت همراه باشد. [109]
این اولین داروی تایید شده برای درمان کم خونی داسی شکل بود و در سال 1995 تعداد و شدت حملات را کاهش داد [110] و در مطالعه ای در سال 2003 نشان داد که احتمالاً زمان بقا را افزایش می دهد. [111] این به دست آمد. تا حدی با فعال کردن مجدد تولید هموگلوبین جنینی به جای هموگلوبین S که باعث کم خونی سلول داسی می شود. هیدروکسی اوره قبلاً به عنوان یک عامل شیمی درمانی استفاده می شد و نگرانی هایی وجود دارد که استفاده طولانی مدت ممکن است مضر باشد، اما این خطر یا وجود ندارد یا بسیار کم است و فواید آن احتمالاً بیشتر از خطرات است. [21] [112]
Voxelotor در سال 2019 در ایالات متحده تایید شد تا هموگلوبین را در افراد مبتلا به بیماری SS افزایش دهد. [113] با این حال، به دنبال افزایش خطر تشنج های انسداد عروق و مرگ مشاهده شده در ثبت و کارآزمایی های بالینی، آژانس دارویی اروپا مجوز بازاریابی برای voxelotor را در سپتامبر 2024 به حالت تعلیق درآورد و به دنبال آن سازنده، Pfizer ، آن را از بازار در سراسر جهان خارج کرد. [114] [115]
انتقال خون اغلب در مدیریت بیماری سلول داسی شکل در موارد حاد و برای جلوگیری از عوارض با کاهش تعداد گلبول های قرمز خون (RBC) که با افزودن گلبول های قرمز طبیعی می توانند داسی شوند، استفاده می شود. [116] در کودکان، نشان داده شده است که درمان پیشگیرانه با انتقال RBC خطر اولین سکته مغزی یا سکته مغزی خاموش را زمانی که سونوگرافی داپلر ترانس کرانیال جریان خون غیرطبیعی مغزی را نشان میدهد، کاهش میدهد. [6] در کسانی که یک رویداد سکته مغزی قبلی را پشت سر گذاشتهاند، خطر سکته مغزی مکرر و سکتههای بیصدا اضافی را نیز کاهش میدهد. [117] [118]
پیوند مغز استخوان در کودکان مؤثر بوده است. آنها تنها درمان شناخته شده برای SCD هستند. [119] با این حال، پیوند مغز استخوان به دلیل نوع خاص HLA ضروری است. در حالت ایده آل، یکی از بستگان نزدیک (آلوژنیک) مغز استخوان لازم برای پیوند را اهدا می کند. بستگان نزدیک باید گروه خونی مشابهی با بیمار داشته باشند. برخی از ژندرمانیها در دست توسعه هستند که سلولهای بنیادی مغز استخوان خود بیمار را در شرایط خارج از بدن تغییر میدهند، که پس از شیمیدرمانی که سلولهای اصلاحنشده اولیه را از بین میبرد، میتوانند دوباره به بیمار پیوند شوند. [120]
پیوند سلول های بنیادی خونساز (HSCT)
درمان کم خونی داسی شکل به طور ضمنی شامل پیوند سلول های بنیادی خونساز (HSCT) است. [121] این مستلزم جایگزینی سلولهای بنیادی ناکارآمد در مورد با استخوانهای سالم از یک اهداکننده همسان است. یافتن مشتری ایده آل - معمولاً یک سهام یا شخصی تقریباً مشابه - برای موفقیت این فرآیند ضروری است. با این حال، هنوز برخی از اشکالات پیوند سلول های بنیادی خونساز (HSCT) وجود دارد، مانند نیاز به جزئیات دقیق برای مهار سیستم حساس و مشکلات ناشی از عدم تثبیت سلول های جدید. با این حال، HSCT موفقیت آمیز می تواند منجر به درمان طولانی مدت کم خونی داسی شکل برای بیمار شود. [122]
هنگام درمان نکروز آواسکولار استخوان در افراد مبتلا به بیماری سلول داسی شکل، هدف از درمان کاهش یا توقف درد و حفظ تحرک مفصل است . [50] گزینههای درمانی فعلی شامل استراحت مفصل، فیزیوتراپی ، داروهای مسکن ، جراحی جایگزینی مفصل یا پیوند استخوان است . [50] برای ارزیابی موثرترین گزینه درمانی و تعیین اینکه آیا ترکیبی از فیزیوتراپی و جراحی موثرتر از فیزیوتراپی به تنهایی است یا خیر، به کارآزماییهای با کیفیت بالا، تصادفیسازی شده و کنترلشده نیاز است. [123] [124]
درمانهای روانشناختی مانند آموزش به بیمار ، شناخت درمانی ، رفتاردرمانی و رواندرمانی روانپویشی که با هدف تکمیل درمانهای پزشکی فعلی انجام میشوند، نیازمند تحقیقات بیشتر برای تعیین اثربخشی آنها هستند. [28]
در سال 2023، هم اگزاگمگلوژن اتوتمسل و هم لووتی بیگلوژن اتوتمسل برای درمان بیماری سلول داسی شکل تایید شدند. [13] [125]
حدود 90 درصد از افراد تا سن 20 سالگی زنده می مانند و نزدیک به 50 درصد بیشتر از 50 سالگی زنده می مانند. [126] در سال 2001، طبق یک مطالعه انجام شده در جامائیکا، میانگین بقای افراد برای مردان 53 سال و برای زنان 58 سال بود. با SCD هموزیگوت. [127] امید به زندگی در بسیاری از کشورهای در حال توسعه ناشناخته است. [128] در سال 1975، حدود 7.3 درصد از افراد مبتلا به SCD قبل از تولد 23 سالگی جان خود را از دست دادند. در حالی که در سال 1989، 2.6٪ از افراد مبتلا به SCD در سن 20 سالگی مردند. [129] : 348
ژن HbS را می توان در هر گروه قومی یافت. [130] بیشترین فراوانی بیماری سلول داسی شکل در مناطق گرمسیری، به ویژه جنوب صحرای آفریقا، مناطق قبیله ای هند و خاورمیانه مشاهده می شود. [131] اعتقاد بر این است که حدود 80٪ موارد بیماری سلول داسی شکل در جنوب صحرای آفریقا رخ می دهد . [16] مهاجرت جمعیت قابل توجهی از این مناطق با شیوع بالا به کشورهای با شیوع پایین در اروپا در دهه های اخیر به طور چشمگیری افزایش یافته است و در برخی از کشورهای اروپایی، بیماری سلول داسی شکل اکنون بر شرایط ژنتیکی آشناتر مانند هموفیلی و فیبروز کیستیک غلبه کرده است . [132] در سال 2015، حدود 114800 کشته برجای گذاشت. [8]
بیماری سلول داسی شکل بیشتر در میان افرادی رخ می دهد که اجدادشان در مناطق گرمسیری و نیمه گرمسیری جنوب صحرا زندگی می کردند که مالاریا در آن شایع است یا شایع بود. در مواردی که مالاریا شایع است، حمل یک آلل سلول داسی شکل (ویژگی) یک مزیت هتروزیگوت ایجاد می کند . انسانهای مبتلا به یکی از دو آلل سلول داسی شکل در هنگام آلوده شدن به مالاریا علائم شدیدتری نشان میدهند. [133]
این وضعیت در الگوی اتوزومال مغلوب به ارث می رسد، به این معنی که هر دو نسخه از ژن در هر سلول دارای جهش هستند. والدین هر کدام حامل یک نسخه از ژن جهش یافته هستند، اما معمولاً علائم و نشانه های این بیماری را نشان نمی دهند. [134]
سه چهارم موارد سلول داسی شکل در آفریقا رخ می دهد. گزارش اخیر سازمان جهانی بهداشت تخمین زده است که حدود 2 درصد از نوزادان در نیجریه به کم خونی سلول داسی شکل مبتلا هستند که در مجموع 150000 کودک مبتلا را هر ساله تنها در نیجریه به دنیا می آورند. فرکانس حامل بین 10 تا 40 درصد در سراسر آفریقای استوایی، به 1 تا 2 درصد در سواحل آفریقای شمالی و کمتر از 1 درصد در آفریقای جنوبی کاهش می یابد. [135] مطالعات در آفریقا کاهش قابل توجهی در میزان مرگ و میر نوزادان در سنین 2 تا 16 ماهگی به دلیل ویژگی سلول داسی شکل نشان می دهد. این اتفاق در مناطقی با موارد غالب مالاریا رخ داد. [136]
اوگاندا پنجمین بیماری سلول داسی شکل را در آفریقا دارد. [137] یک مطالعه نشان می دهد که 20000 نوزاد در سال با بیماری سلول داسی شکل با صفت سلول داسی شکل در 13.3٪ و با بیماری 0.7٪ متولد می شوند. [138]
تعداد افراد مبتلا به این بیماری در ایالات متحده حدود 100000 نفر (یکی از هر 3300) است که بیشتر آمریکایی های آفریقایی تبار جنوب صحرا را تحت تاثیر قرار می دهند. [139] در ایالات متحده، از هر 365 کودک آفریقایی-آمریکایی، یک کودک و از هر 16300 کودک اسپانیایی-آمریکایی، یک کودک دارای کم خونی سلول داسی شکل است. [140] امید به زندگی برای مردان مبتلا به SCD تقریباً 42 سال است در حالی که زنان تقریباً شش سال بیشتر عمر می کنند. [141] 2 میلیون نفر دیگر نیز ناقل صفت سلول داسی هستند. [142] اکثر نوزادان مبتلا به SCD که در ایالات متحده متولد می شوند با غربالگری معمول نوزادان شناسایی می شوند. از سال 2016، همه 50 ایالت غربالگری برای بیماری سلول داسی شکل را به عنوان بخشی از غربالگری نوزادان خود در نظر می گیرند. [143] خون نوزاد از طریق نیش پاشنه نمونه برداری می شود و برای آزمایش به آزمایشگاه فرستاده می شود. قبل از انجام تست خراش پاشنه، کودک باید حداقل 24 ساعت غذا بخورد. در برخی از ایالت ها نیز برای اطمینان از نتایج، نیاز به انجام آزمایش خون دوم در دو هفتهگی نوزاد است. [144]
کم خونی داسی شکل شایع ترین اختلال ژنتیکی در میان آمریکایی های آفریقایی تبار است. تقریباً 8 درصد ناقل هستند و از هر 375 نفر 1 نفر با این بیماری متولد می شوند. [145] حامیان بیماران برای بیماری سلول داسی شکایت کرده اند که بودجه تحقیقاتی دولتی و خصوصی کمتری نسبت به بیماری های نادر مشابه مانند فیبروز کیستیک دریافت می کند ، به گفته محقق الیوت ویچینسکی، این نشان دهنده تبعیض نژادی یا نقش ثروت در حمایت از مراقبت های بهداشتی است. [146] به طور کلی، بدون در نظر گرفتن نژاد، تقریباً 1.5٪ از نوزادان متولد شده در ایالات متحده ناقل حداقل یک نسخه از ژن جهش یافته (بیمارساز) هستند. [147]

در نتیجه رشد جمعیت در مناطق آفریقایی-کارائیب در خارج از کشور فرانسه و مهاجرت از شمال و جنوب صحرای آفریقا به سرزمین اصلی فرانسه، بیماری سلول داسی شکل به یک مشکل عمده بهداشتی در فرانسه تبدیل شده است. [148] SCD به شایع ترین بیماری ژنتیکی در کشور تبدیل شده است، با شیوع کلی تولد یک در 2415 در کلان شهر فرانسه ، بالاتر از فنیل کتونوری (یک در 10862)، کم کاری مادرزادی تیروئید (یک در 3132)، هیپرپلازی مادرزادی آدرنال (one). در 19008) و فیبروز کیستیک (یک در 5014) برای همان دوره مرجع. [149]

از سال 2000، غربالگری نوزادان SCD در سطح ملی برای همه نوزادانی که به عنوان "در معرض خطر" برای SCD بر اساس منشأ قومی تعریف شده اند (تعریف شده به عنوان کسانی که از والدین متولد شده از جنوب صحرای آفریقا، شمال آفریقا، مدیترانه متولد شده اند، انجام شده است. منطقه (جنوب ایتالیا، یونان و ترکیه )، شبه جزیره عربی، جزایر فرادریایی فرانسه و شبه قاره هند). [150]
در بریتانیا، بین 12000 تا 15000 نفر تصور می شود که به بیماری سلول داسی شکل [151] مبتلا هستند و تخمین زده می شود که 250000 ناقل این بیماری تنها در انگلستان باشد. از آنجایی که تعداد ناقلان فقط تخمین زده می شود، همه نوزادان تازه متولد شده در بریتانیا آزمایش خون معمولی برای غربالگری این بیماری دریافت می کنند. [152] به دلیل اینکه بسیاری از بزرگسالان در گروههای پرخطر نمیدانند ناقل هستند یا خیر، به زنان باردار و هر دو زوج در یک زوج غربالگری پیشنهاد میشود تا در صورت داشتن صفت سلول داسی شکل بتوانند مشاوره دریافت کنند. [153] علاوه بر این، اهداکنندگان خون از گروههای پرخطر نیز غربالگری میشوند تا تأیید شود که آیا ناقل هستند و آیا خون آنها به درستی فیلتر میشود. [154] اهداکنندگانی که مشخص میشود ناقل هستند، مطلع میشوند و خون آنها، در حالی که اغلب برای افراد همگروه قومی استفاده میشود، برای کسانی که به بیماری سلول داسی شکل نیاز دارند که نیاز به تزریق خون دارند، استفاده نمیشود. [155]
در عربستان سعودی ، حدود 4.2٪ از جمعیت دارای ویژگی سلول داسی شکل هستند و 0.26٪ مبتلا به بیماری سلول داسی شکل هستند. بیشترین شیوع در استان شرقی است که تقریباً 17 درصد جمعیت حامل این ژن و 1.2 درصد به بیماری سلول داسی شکل هستند. [156] در سال 2005، عربستان سعودی یک آزمایش اجباری قبل از ازدواج شامل الکتروفورز HB را معرفی کرد که هدف آن کاهش بروز SCD و تالاسمی بود . [157]
در بحرین ، مطالعهای که در سال 1998 منتشر شد و حدود 56000 نفر را در بیمارستانهای بحرین تحت پوشش قرار داد، نشان داد که 2٪ از نوزادان مبتلا به بیماری سلول داسی شکل هستند، 18٪ از افراد مورد بررسی دارای ویژگی سلول داسی شکل هستند و 24٪ ناقل جهش ژنی بودند که باعث ایجاد جهش در ژن میشود. بیماری [158] کشور غربالگری همه زنان باردار را در سال 1992 آغاز کرد و نوزادان تازه متولد شده در صورت ناقل بودن مادر شروع به آزمایش کردند. در سال 2004، قانونی تصویب شد که به موجب آن زوج هایی که قصد ازدواج دارند باید تحت مشاوره رایگان قبل از ازدواج قرار گیرند . این برنامه ها با کمپین های آموزش عمومی همراه بود. [159]
بیماری سلول داسی شکل در برخی از گروههای قومی در مرکز هند رایج است، [160] که شیوع آن از 9.4 تا 22.2 درصد در نواحی آندمیک مادیا پرادش ، راجستان و چاتیسگر متغیر است . [161] همچنین در میان مردم تارو نپال و هند بومی است . با این حال، آنها هفت برابر کمتر از مالاریا با وجود زندگی در یک منطقه آلوده به مالاریا. [162]
در جامائیکا ، 10 درصد از جمعیت حامل ژن سلول داسی هستند که آن را به شایع ترین اختلال ژنتیکی در کشور تبدیل می کند. [163]
اولین گزارش مدرن از بیماری سلول داسی شکل ممکن است در سال 1846 باشد، جایی که کالبد شکافی یک برده فراری اعدام شده مورد بحث قرار گرفت. یافته کلیدی عدم وجود طحال بود. [164] [165] بنا به گزارش، بردگان آفریقایی در ایالات متحده در برابر مالاریا مقاومت نشان دادند، اما مستعد ابتلا به زخم پا بودند. [165] ویژگیهای غیرطبیعی گلبولهای قرمز خون، که بعداً نام خود را به این بیماری دادند، برای اولین بار توسط ارنست ای. آیرونز (1877-1959)، کارآموز قلب و عروق شیکاگو و استاد پزشکی جیمز بی. هریک (1861-1861) توصیف شد. آیرونز در خون مردی به نام والتر کلمنت نوئل، دانشجوی سال اول دندانپزشکی 20 ساله از گرانادا، سلول های "داس شکل و درازی عجیب" را دید. نوئل در دسامبر 1904 به دلیل کم خونی در بیمارستان پرسبیتریان شیکاگو بستری شده بود. [18] [166] نوئل در طول سه سال بعد چندین بار به دلیل " روماتیسم عضلانی " و "حملات صفراوی" مجددا پذیرش شد، اما تحصیلات خود را به پایان رساند و به پایتخت گرانادا (سنت جورج) بازگشت تا دندانپزشکی کند . او در سال 1916 بر اثر ذات الریه درگذشت و در گورستان کاتولیک در Sauteurs در شمال گرانادا به خاک سپرده شد. [18] [19] مدت کوتاهی پس از گزارش هریک، مورد دیگری در نیمه ماهنامه پزشکی ویرجینیا با همین عنوان ظاهر شد، «گلولههای خونی قرمز دراز و داسیشکل عجیب در مورد کم خونی شدید». [ 167] این مقاله بر اساس یک بیمار بستری شده در بیمارستان دانشگاه ویرجینیا در 15 نوامبر 1910 است . [19] [169] مشکلات دوران کودکی مربوط به بیماری سلول داسی تا دهه 1930 گزارش نشد، علیرغم این واقعیت که این امر در جمعیت های آفریقایی-آمریکایی غیرمعمول نبوده است. [165]
لموئل دیگز ، پزشک ممفیس ، محقق پرکار بیماری سلول داسی، برای اولین بار در سال 1933 تمایز بین بیماری سلول داسی شکل و صفت را معرفی کرد، اگرچه تا سال 1949، ویژگی های ژنتیکی توسط جیمز وی. نیل و EA Beet مشخص نشده بود . [19] سال 1949 سالی بود که لینوس پاولینگ رفتار شیمیایی غیرعادی هموگلوبین S را توصیف کرد و این را به یک ناهنجاری در خود مولکول نسبت داد. [19] [170] تغییر مولکولی در HbS در سال 1956 توسط Vernon Ingram توصیف شد . [171] اواخر دهه 1940 و اوایل دهه 1950 درک بیشتری در رابطه بین مالاریا و بیماری سلول داسی شکل مشاهده شد. در سال 1954، معرفی الکتروفورز هموگلوبین امکان کشف زیرگروه های خاصی مانند بیماری HbSC را فراهم کرد. [19]
مطالعات تاریخ طبیعی در مقیاس بزرگ و مطالعات مداخله ای بیشتر در دهه 1970 و 1980 معرفی شد که منجر به استفاده گسترده از پیشگیری از عفونت های پنوموکوکی در میان سایر مداخلات شد. فیلم تلویزیونی بیل کازبی برنده جایزه امی در سال 1972، به همه دوستان من در ساحل ، داستان والدین یک کودک مبتلا به بیماری سلول داسی شکل را به تصویر می کشد. [172] دهه 1990 توسعه هیدروکسی کاربامید بود، و گزارشهایی از درمان از طریق پیوند مغز استخوان در سال 2007 ظاهر شد. [19]
برخی از متون قدیمی از آن به عنوان دریپانوسیتوز یاد می کنند. [173]
بیماری سلول داسی شکل اغلب به عنوان یک ناتوانی مورد بحث قرار می گیرد. [174] از تاریخ 15 سپتامبر 2017، اداره تامین اجتماعی ایالات متحده یک حکم تفسیری خط مشی صادر کرد که اطلاعات زمینه ای در مورد بیماری سلول داسی شکل و توضیحی در مورد نحوه ارزیابی این بیماری در طی فرآیند قضاوت برای ادعای ناتوانی توسط تامین اجتماعی ارائه می دهد. [175] [176]
در ایالات متحده، انگ هایی پیرامون SCD وجود دارد که افراد مبتلا به SCD را از دریافت مراقبت های لازم منصرف می کند. به گفته مؤسسه ملی قلب، ریه و خون، این انگها عمدتاً بر افرادی با اجداد آمریکایی آفریقایی تبار و آمریکای لاتین تأثیر می گذارد. [177] افراد مبتلا به SCD تأثیر انگ های این بیماری را بر جنبه های مختلف زندگی از جمله رفاه اجتماعی و روانی تجربه می کنند. مطالعات نشان داده است که افراد مبتلا به SCD اغلب احساس می کنند که باید تشخیص خود را مخفی نگه دارند تا از تبعیض در محل کار و همچنین در بین همسالان در روابط خود جلوگیری کنند. [178] در دهه 1960، دولت ایالات متحده از طرح هایی برای غربالگری در محل کار برای بیماری های ژنتیکی در تلاش برای محافظت از افراد مبتلا به SCD حمایت کرد. با انجام این غربالگری، در نظر گرفته شد که کارکنان در محیط هایی قرار نگیرند که به طور بالقوه می تواند مضر باشد و باعث ایجاد SCD شود. [179]
اوگاندا پنجمین بیماری سلول داسی شکل (SCD) در جهان است. [180] در اوگاندا ، ننگ اجتماعی برای مبتلایان به بیماری سلول داسی شکل وجود دارد، زیرا دانش عمومی در مورد این بیماری وجود ندارد. شکاف کلی در دانش در مورد بیماری سلول داسی شکل در میان نوجوانان و بزرگسالان جوان به دلیل پنهان کاری تایید شده فرهنگی در مورد این بیماری مشخص شده است. [180] در حالی که اکثر مردم به طور کلی در مورد این بیماری شنیده اند، بخش بزرگی از جمعیت در مورد نحوه تشخیص یا ارثی SCD اطلاعات نسبتا نادرستی دارند. کسانی که در مورد این بیماری مطلع شده اند از خانواده یا دوستانشان و نه از متخصصان بهداشت در مورد آن مطلع شده اند . عدم ارائه اطلاعات در مورد بیماری سلول داسی شکل به مردم منجر به ایجاد درک ضعیفی از علل بیماری، علائم و تکنیک های پیشگیری می شود. [181] تفاوتهای فیزیکی و اجتماعی که در مبتلایان به بیماری سلول داسی شکل، مانند یرقان، توقف رشد فیزیکی و تاخیر در بلوغ جنسی ایجاد میشود، همچنین میتواند آنها را به هدف قلدری، طرد و انگ تبدیل کند. [180]
داده های گردآوری شده در مورد بیماری سلول داسی شکل در اوگاندا از اوایل دهه 1970 به روز نشده است. کمبود داده ها به دلیل کمبود بودجه تحقیقاتی دولتی است، حتی اگر اوگاندایی ها روزانه از SCD می میرند. [182] داده ها نشان می دهد که فراوانی صفت بیماری سلول داسی شکل 20 درصد از جمعیت اوگاندا است. [182] این بدان معنی است که 66 میلیون نفر در معرض خطر ابتلا به یک فرزند مبتلا به بیماری سلول داسی قرار دارند. [182] همچنین تخمین زده می شود که حدود 25000 اوگاندایی هر ساله با SCD متولد می شوند و 80٪ از این افراد بیش از پنج سال عمر نمی کنند. [182] SCD همچنین 25٪ در نرخ مرگ و میر کودکان در اوگاندا نقش دارد. [182] مردم بامبا اوگاندا، واقع در جنوب غربی کشور، حامل 45 درصد از ژن هستند که بالاترین فراوانی صفت ثبت شده در جهان است. [182] کلینیک سلول داسی شکل در مولاگو تنها یک کلینیک بیماری سلول داسی شکل در کشور است و به طور متوسط روزانه 200 بیمار را ملاقات می کند. [182]
انگ اطراف این بیماری به ویژه در مناطقی از کشور که به آن مبتلا نیستند بد است. برای مثال، اوگانداییهای شرقی نسبت به اوگانداییهای غربی نسبت به این بیماری آگاهتر هستند، زیرا احتمال بیشتری وجود دارد که بر این باورند که بیماری سلول داسی به عنوان مجازاتی از جانب خدا یا جادوگری به وجود آمده است . [183] سایر تصورات نادرست در مورد SCD عبارتند از این باور که ناشی از عوامل محیطی است، اما در واقعیت، SCD یک بیماری ژنتیکی است. [184] در سرتاسر اوگاندا تلاش هایی برای رسیدگی به تصورات غلط اجتماعی در مورد این بیماری صورت گرفته است. در سال 2013، بنیاد نجات سلول داسی اوگاندا برای گسترش آگاهی در مورد بیماری سلول داسی شکل و مبارزه با انگ اجتماعی مرتبط با این بیماری تأسیس شد. [185] علاوه بر تلاشهای این سازمان، نیاز به گنجاندن آموزش بیماری سلول داسی در برنامههای آموزش سلامت جامعه از قبل وجود دارد تا انگ بیماری سلول داسی در اوگاندا کاهش یابد. [181]
انگ عمیقا ریشه دار SCD از جامعه باعث می شود که خانواده ها اغلب وضعیت بیمار اعضای خانواده خود را از ترس برچسب زدن، نفرین شدن یا کنار گذاشتن رویدادهای اجتماعی پنهان کنند. [186] گاهی اوقات در اوگاندا، زمانی که تایید می شود که یکی از اعضای خانواده به بیماری سلول داسی شکل مبتلا است، از روابط صمیمانه با همه اعضای خانواده اجتناب می شود. [186] انگ و انزوای اجتماعی که افراد مبتلا به بیماری سلول داسی شکل معمولاً تجربه میکنند، اغلب نتیجه تصورات غلط رایج است که افراد مبتلا به SCD نباید با افراد آزاد از این بیماری معاشرت کنند. این ذهنیت افراد مبتلا به SCD را از حق شرکت آزادانه در فعالیت های اجتماعی مانند دیگران می رباید [180] انگ مرتبط با SCD و انزوای اجتماعی در مدارس، به ویژه، می تواند زندگی را برای جوانانی که با بیماری سلول داسی شکل زندگی می کنند بسیار دشوار کند. [180] برای کودکان مدرسهای که با SCD زندگی میکنند، انگی که با آن مواجه میشوند میتواند منجر به طرد همسالان شود. [180] طرد همسالان مستلزم طرد شدن از گروهها یا اجتماعات اجتماعی است. اغلب باعث می شود فرد طرد شده دچار پریشانی عاطفی شود و ممکن است منجر به عملکرد ضعیف تحصیلی، اجتناب از مدرسه و شکست شغلی آنها در آینده شود. [180] این انزوای اجتماعی نیز احتمالاً تأثیر منفی بر افراد مبتلا به عزت نفس SCD و کیفیت کلی زندگی دارد. [180]
مادران کودکان مبتلا به بیماری سلول داسی شکل تمایل دارند مقادیر نامتناسبی از انگ از همسالان و اعضای خانواده خود دریافت کنند. این زنان اغلب برای تشخیص SCD توسط فرزندشان مورد سرزنش قرار می گیرند ، به خصوص اگر SCD در نسل های قبلی وجود نداشته باشد، به دلیل این سوء ظن که سلامت ضعیف کودک ممکن است به دلیل عدم اجرای اقدامات پیشگیرانه بهداشتی یا ترویج یک محیط سالم توسط مادر باشد. برای رشد فرزندش [184] تکیه بر نظریه های مربوط به عوامل محیطی برای مقصر دانستن مادر، نشان دهنده دانش ضعیف بسیاری از اوگاندا در مورد چگونگی به دست آوردن بیماری است، زیرا توسط ژنتیک تعیین می شود، نه محیط. [184] مادران کودکان مبتلا به بیماری سلول داسی شکل نیز اغلب با منابع بسیار محدودی برای محافظت از آینده خود در برابر انگ ابتلا به SCD باقی می مانند. [184] این عدم دسترسی به منابع ناشی از نقشهای فرعی آنها در ساختارهای خانوادگی و همچنین اختلاف طبقاتی است که مانع از توانایی بسیاری از مادران برای برآورده کردن هزینهها و مسئولیتهای اضافی مراقبت از کودک میشود. [184]
زنان مبتلا به SCD که باردار می شوند اغلب در اوگاندا با تبعیض و دلسردی شدید روبرو می شوند. این زنان اغلب توسط همسالان خود به عنوان افراد غیرمسئول برای بچه دار شدن در حالی که با بیماری سلول داسی شکل زندگی می کنند یا حتی درگیر رابطه جنسی در حین زندگی با SCD نامیده می شوند. بار صفت و بیماری سلول داسی شکل در مطالعه نظارت بر داسی اوگاندا (US3): مطالعه مقطعی انتقاد و قضاوت این زنان، نه تنها از سوی متخصصان مراقبت های بهداشتی، بلکه از سوی خانواده هایشان، اغلب باعث می شود که آنها احساس تنهایی، افسرده، مضطرب، شرم و با حمایت اجتماعی بسیار کمی داشته باشند . بار بیماری و صفت سلول داسی شکل در اوگاندا مطالعه نظارت بر داسی (US3): یک مطالعه مقطعی - سلامت جهانی Lancet اکثر زنان باردار مبتلا به SCD نیز مادران مجردی هستند زیرا معمولاً توسط شریک مرد خود که ادعا می کنند از شریک زندگی خود بی اطلاع هستند رها می شوند. وضعیت SCD. والدین ناآماده و نادرست کودکان مبتلا به بیماری سلول داسی شکل: زمان بازنگری در کمپین های آگاهی بخشی نه تنها باعث ناراحتی عاطفی این زنان می شود، بلکه این سطح پایین حمایت والدین می تواند با علائم افسردگی مرتبط باشد و به طور کلی کاهش یابد. کیفیت زندگی کودک پس از تولد. [187]
در سال 2021 مشخص شد که بسیاری از بیماران از مراجعه به بیمارستان ها می ترسند، این میزان ناآگاهی در بین کارکنان بود، بنابراین برای درمان خود در خارج از NHS، مسکن خریداری کردند. آنها اغلب برای مدت طولانی منتظر تسکین درد بودند و گاهی اوقات مشکوک به رفتار «مصرف مواد» بودند. تاخیر در درمان، عدم اطلاع تیم هماتولوژی بیمارستان و مدیریت ضعیف درد باعث مرگ و میر شده بود. کارکنان متخصص هماتولوژی ترجیح میدهند در بیمارستانهای آموزشی بزرگتر کار کنند، که منجر به کمبود تخصص در جاهای دیگر شد. [188] در سال 2021، NHS اولین درمان جدید خود را پس از 20 سال برای سلول داسی شکل آغاز کرد. این شامل استفاده از Crizanlizumab ، دارویی است که از طریق قطرهای تزریق خون داده میشود، که تعداد مراجعه بیماران به A&E را کاهش میدهد. این درمان از طریق مشاوران در هر یک از ده مرکز جدید راه اندازی شده در سراسر کشور قابل دسترسی است. [189] با این حال، در همان سال، یک گروه پارلمانی همه حزبی گزارشی درباره سلول داسی شکل و تالاسمی با عنوان «هیچکس گوش نمی دهد» تهیه کرد. [190] تا حدودی در پاسخ به این موضوع، در 19 ژوئن 2022، روز جهانی سلول داسی، NHS کمپینی به نام "آیا می توانید بگویید که سلول داسی است؟" راه اندازی کرد. این کمپین اهداف دوگانه ای داشت. یکی افزایش آگاهی در مورد علائم و نشانه های کلیدی اختلال خونی بود تا افراد به همان اندازه که نسبت به حمله قلبی یا سکته قریب الوقوع هوشیار هستند نسبت به علائم بحران سلول داسی شکل هوشیار باشند. هدف دوم، راه اندازی یک برنامه آموزشی جدید برای کمک به امدادگران، کارکنان حوادث و اورژانس، مراقبین و عموم مردم برای مراقبت موثر از مبتلایان در بحران بود. [191]
در حالی که پیوند خون بند ناف به طور بالقوه می تواند این بیماری را درمان کند، اهداکننده مناسب تنها در 10 درصد از افراد در دسترس است. [192] حدود 7 درصد از افراد نیز در نتیجه این روش می میرند و ممکن است بیماری پیوند در مقابل میزبان رخ دهد. [192]
بیماری هایی مانند بیماری سلول داسی که ممکن است فنوتیپ طبیعی یا عملکرد سلولی فرد در سلول های مبتلا به بیماری توسط یک نسخه طبیعی از ژن جهش یافته بازیابی شود، ممکن است کاندیدای خوبی برای درمان ژن درمانی باشد. خطرات و مزایای مربوط به ژن درمانی برای بیماری سلول داسی شکل شناخته شده نیست. [193]
در سال 2001، بیماری سلول داسی با استفاده از ژن درمانی با موفقیت در موش ها درمان شد . [194] [195] محققان از یک ناقل ویروسی برای تولید هموگلوبین جنینی (HbF) در موشها - که اساساً دارای همان نقصی هستند که باعث بیماری سلول داسی شکل انسانی میشود - استفاده کردند، که معمولاً یک فرد بلافاصله پس از تولد تولید آن متوقف میشود. در انسان، استفاده از هیدروکسی اوره برای تحریک تولید HbF به طور موقت علائم بیماری سلول داسی شکل را کاهش می دهد. محققان نشان دادند که این روش ژن درمانی راه دائمی تری برای افزایش تولید HbF درمانی است. [196]
آزمایشات بالینی فاز 1 ژن درمانی برای بیماری سلول داسی شکل در انسان در سال 2014 آغاز شد. کارآزمایی های بالینی ایمنی مغز استخوان اصلاح شده با ناقل لنتی ویروسی را برای بزرگسالان مبتلا به بیماری سلول داسی شکل شدید ارزیابی کردند. [197] [198] گزارش موردی برای اولین فرد تحت درمان در مارس 2017 منتشر شد و از آن زمان چند نفر دیگر تحت درمان قرار گرفتند. [199] [200]
پلتفرم های ویرایش ژن مانند CRISPR/Cas9 برای اصلاح جهش عامل بیماری در سلول های بنیادی خونساز گرفته شده از فرد مبتلا به این بیماری استفاده شده است. [201] در ژوئیه 2019 ابزار ویرایش ژن CRISPR برای ویرایش سلولهای مغز استخوان یک فرد مبتلا به SCD برای تقویت هموگلوبین جنین با مهار ژن BCL11A استفاده شد . [202] [203] تعدادی از محققان پیامدهای اخلاقی SCD را یکی از اولین کاربردهای بالقوه فناوری CRISPR، با توجه به سوء استفاده های تاریخی و بی توجهی جامعه آفریقایی آمریکایی توسط حوزه پزشکی در نظر گرفته اند. [204]
در سال 2017، دوازده کارآزمایی بالینی بر روی ژن درمانی برای درمان کم خونی سلول داسی متمرکز بود. از این 12 کارآزمایی، چهار مورد از آنها ژن HBB جهش یافته را با یک ژن سالم جایگزین کردند. سه کارآزمایی از Mozobil، دارویی که برای درمان انواع سرطان استفاده میشود، برای تعیین اینکه آیا افزایش سلولهای بنیادی میتواند برای ژندرمانی استفاده شود، استفاده کردند. یک کارآزمایی بر تجزیه و تحلیل نمونه های مغز استخوان بیماران مبتلا به کم خونی سلول داسی شکل متمرکز بود. آزمایش دیگری با استفاده از خون بند ناف نوزادان با و بدون کم خونی سلول داسی شکل برای توسعه ژن درمانی انجام شد. [205]
در نوامبر 2023، یک درمان ژنی با استفاده از ابزار ویرایش ژن CRISPR توسط تنظیم کننده های بریتانیا برای درمان بیماری سلول داسی شکل و همچنین برای اختلالات خونی بتا تالاسمی وابسته به انتقال خون تایید شد . [14] [125]
هیچ شواهد پزشکی قوی برای تعیین خطرات و مزایای بالقوه مربوط به درمان افراد مبتلا به بیماری سلول داسی شکل با پیوند سلول های بنیادی خونساز وجود ندارد. [206]
{{cite journal}}: CS1 maint: URL نامناسب ( پیوند )پنی سیلین پیشگیرانه دو بار در روز از اوایل دوران نوزادی شروع می شود و تا حداقل 5 سالگی ادامه می یابد.
... تیم ها گزارش می دهند که دو استراتژی برای رفع مستقیم سلول های خونی نادرست به طور چشمگیری سلامت تعداد انگشت شماری از افراد مبتلا به این بیماری های ژنتیکی را بهبود بخشیده است.
{{cite journal}}: CS1 maint: DOI از ژوئن 2024 غیرفعال است ( پیوند )