اسید بوتیریک ( / ˈ b j uː t ɪ r ɪ k / ؛ از یونانی باستان : βούτῡρον , به معنی "کره") که با نام سیستماتیک بوتانوئیک اسید نیز شناخته می شود، یک آلکیل کربوکسیلیک اسید با زنجیره مستقیم با فرمول شیمیایی CH 3 است. CH 2 CH 2 CO 2 H . این مایع روغنی و بی رنگ با بوی نامطبوع است . ایزوبوتیریک اسید (2-متیل پروپانوئیک اسید) یک ایزومر است . نمک ها و استرهای اسید بوتیریک به نام بوتیرات یا بوتانوات شناخته می شوند . اسید به طور گسترده در طبیعت وجود ندارد، اما استرهای آن گسترده است. این یک ماده شیمیایی رایج صنعتی [7] و یک جزء مهم در روده پستانداران است.
اسید بوتیریک اولین بار به شکل ناخالص در سال 1814 توسط شیمیدان فرانسوی میشل اوژن شورول مشاهده شد . در سال 1818، او آن را به اندازه کافی خالص کرده بود تا آن را مشخص کند. با این حال، شورول تحقیقات اولیه خود را در مورد اسید بوتیریک منتشر نکرد. در عوض، او یافته های خود را به صورت دست نویس نزد دبیر آکادمی علوم در پاریس، فرانسه سپرده بود. هانری براکونو ، شیمیدان فرانسوی، نیز در مورد ترکیب کره تحقیق می کرد و یافته های خود را منتشر می کرد و این منجر به اختلافاتی در مورد اولویت شد. در اوایل سال 1815، شورول ادعا کرد که ماده ای را که مسئول بوی کره است، پیدا کرده است. [8] تا سال 1817، او برخی از یافته های خود را در مورد خواص اسید بوتیریک منتشر کرد و آن را نام برد. [9] با این حال، تا سال 1823 بود که او خواص اسید بوتیریک را به تفصیل ارائه کرد. [10] نام اسید بوتیریک از βούτῡρον به معنای "کره" گرفته شده است، ماده ای که برای اولین بار در آن یافت شد. نام لاتین butyrum (یا buturum ) مشابه است.
تری گلیسیرید اسید بوتیریک 3 تا 4 درصد کره را تشکیل می دهد . هنگامی که کره فاسد می شود، اسید بوتیریک با هیدرولیز از گلیسرید آزاد می شود . [11] این یکی از زیر گروه اسیدهای چرب به نام اسیدهای چرب زنجیره کوتاه است . اسید بوتیریک یک اسید کربوکسیلیک معمولی است که با بازها واکنش می دهد و بر بسیاری از فلزات تأثیر می گذارد. [12] در چربی حیوانی و روغن های گیاهی ، شیر گاو ، شیر مادر ، کره ، پنیر پارمزان ، بوی بدن ، استفراغ و به عنوان محصول تخمیر بی هوازی (از جمله در روده بزرگ ) یافت می شود . [13] [14] طعمی شبیه کره و بوی نامطبوع دارد . پستانداران با توانایی تشخیص بوی خوب، مانند سگ ، می توانند آن را با 10 قسمت در میلیارد تشخیص دهند ، در حالی که انسان می تواند آن را فقط در غلظت های بالاتر از 10 قسمت در میلیون تشخیص دهد . در تولید مواد غذایی از آن به عنوان طعم دهنده استفاده می شود . [15]
در انسان، اسید بوتیریک یکی از دو آگونیست درون زا اولیه گیرنده 2 هیدروکسی کربوکسیلیک اسید انسانی ( HCA 2 )، یک گیرنده جفت شده با پروتئین G جفت شده با G i/o است . [16] [17]
اسید بوتیریک به عنوان اکتیل استر آن در ازگیل ( Pastinaca sativa ) [18] و در دانه درخت جینکو وجود دارد . [19]
در صنعت، اسید بوتیریک با هیدروفورمیلاسیون از پروپن و گاز سنتز تولید می شود و بوتیرآلدئید را تشکیل می دهد که به محصول نهایی اکسید می شود. [7]
می توان آن را با اشباع شدن با نمک هایی مانند کلرید کلسیم از محلول های آبی جدا کرد . نمک کلسیم، Ca(C 4 H 7 O 2 ) 2 · H 2 O ، در آب گرم کمتر از آب سرد حل می شود.
بوتیرات توسط چندین فرآیند تخمیر انجام شده توسط باکتری های بی هوازی اجباری تولید می شود . [20] این مسیر تخمیر توسط لویی پاستور در سال 1861 کشف شد. نمونه هایی از گونه های باکتری تولید کننده بوتیرات :
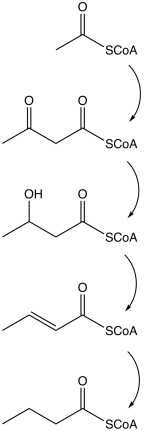
مسیر با تقسیم گلیکولیتیک گلوکز به دو مولکول پیروات آغاز می شود ، همانطور که در بیشتر موجودات اتفاق می افتد. پیرووات به استیل کوآنزیم A که توسط پیروات:فردوکسین اکسیدوردوکتاز کاتالیز می شود اکسید می شود . دو مولکول دی اکسید کربن ( CO 2 ) و دو مولکول هیدروژن ( H 2 ) به عنوان مواد زائد تشکیل می شوند. متعاقبا ATP در آخرین مرحله تخمیر تولید می شود. سه مولکول ATP برای هر مولکول گلوکز تولید می شود که بازدهی نسبتاً بالایی دارد. معادله متعادل برای این تخمیر است
سایر مسیرهای بوتیرات شامل احیای سوکسینات و عدم تناسب کروتونات است.
چندین گونه استون و n- بوتانول را در یک مسیر جایگزین تشکیل می دهند که با تخمیر بوتیرات شروع می شود. برخی از این گونه ها عبارتند از:
این باکتری ها همانطور که در بالا توضیح داده شد با تخمیر بوتیرات شروع می شوند، اما وقتی PH به زیر 5 می رسد، برای جلوگیری از کاهش بیشتر pH، به تولید بوتانول و استون تبدیل می شوند. برای هر مولکول استون دو مولکول بوتانول تشکیل می شود.
تغییر در مسیر پس از تشکیل استواستیل CoA رخ می دهد. سپس این واسطه دو مسیر ممکن را طی می کند:
برای مقاصد تجاری از گونه های کلستریدیوم ترجیحاً برای تولید اسید بوتیریک یا بوتانول استفاده می شود. رایج ترین گونه مورد استفاده برای پروبیوتیک ها کلستریدیوم بوتیریکوم است . [21]
بقایای الیاف بسیار قابل تخمیر، مانند نشاسته مقاوم ، سبوس جو دوسر ، پکتین و گوار توسط باکتری های روده بزرگ به اسیدهای چرب با زنجیره کوتاه (SCFA) از جمله بوتیرات تبدیل می شوند و SCFA بیشتری نسبت به الیاف کمتر قابل تخمیر مانند سلولز تولید می کنند . [14] [22] یک مطالعه نشان داد که نشاسته مقاوم به طور مداوم بوتیرات بیشتری نسبت به سایر انواع فیبر غذایی تولید می کند . [23] تولید SCFA از الیاف در حیوانات نشخوارکننده مانند گاو مسئول محتوای بوتیرات شیر و کره است. [13] [24]
فروکتان ها منبع دیگری از فیبرهای غذایی محلول پربیوتیک هستند که می توانند برای تولید بوتیرات هضم شوند. [25] آنها اغلب در فیبرهای محلول غذاهایی که دارای گوگرد بالایی هستند ، مانند آلیوم و سبزیجات چلیپایی یافت می شوند . منابع فروکتان ها عبارتند از گندم (اگرچه برخی از گونه های گندم مانند املا حاوی مقادیر کمتری هستند)، [26] چاودار ، جو ، پیاز ، سیر ، اورشلیم و کنگر کره زمین ، مارچوبه ، چغندر ، کاسنی ، برگ قاصدک ، تره سفید ، تره فرنگی پیاز بهاره ، کلم بروکلی ، کلم بروکسل ، کلم ، رازیانه ، و پری بیوتیک ها مانند فروکتولیگوساکاریدها ( FOS )، الیگو فروکتوز و اینولین . [27] [28]
اسید بوتیریک به عنوان یک اسید کربوکسیلیک معمولی واکنش نشان می دهد: می تواند مشتقات آمید ، استر ، انیدرید و کلرید را تشکیل دهد . [29] دومی، بوتیریل کلرید ، معمولاً به عنوان واسطه برای به دست آوردن بقیه استفاده می شود.
اسید بوتیریک در تهیه استرهای مختلف بوتیرات استفاده می شود. این ماده برای تولید سلولز استات بوتیرات (CAB) استفاده می شود که در طیف گسترده ای از ابزارها، رنگ ها و پوشش ها استفاده می شود و نسبت به استات سلولز در برابر تخریب مقاوم تر است . [30] CAB می تواند با قرار گرفتن در معرض گرما و رطوبت تخریب شود و اسید بوتیریک آزاد کند. [31]
استرهای با وزن مولکولی کم اسید بوتیریک، مانند متیل بوتیرات ، عمدتاً عطر یا طعم دلپذیری دارند. [7] در نتیجه، آنها به عنوان مواد افزودنی غذا و عطر استفاده می شوند. این یک طعم دهنده غذا در پایگاه داده FLAVIS اتحادیه اروپا (شماره 08.005) است.
به دلیل بوی قوی آن به عنوان افزودنی طعمه ماهیگیری نیز استفاده شده است. [32] بسیاری از طعمهای تجاری موجود در طعمههای کپور ( Cyprinus carpio ) از اسید بوتیریک به عنوان پایه استری استفاده میکنند. مشخص نیست که آیا ماهی توسط خود اسید بوتیریک جذب می شود یا مواد اضافه شده به آن. اسید بوتیریک یکی از معدود اسیدهای آلی بود که نشان داده شده است هم برای تنچ و هم برای تلخی خوش طعم است . [33] این ماده به عنوان یک بمب بدبو توسط انجمن حفاظت از چوپان دریایی برای مختل کردن خدمه صید نهنگ ژاپنی استفاده شده است . [34]
اسید بوتیریک (pK a 4.82) در pH فیزیولوژیکی کاملاً یونیزه می شود ، بنابراین آنیون آن ماده ای است که عمدتاً در سیستم های بیولوژیکی مرتبط است. این یکی از دو آگونیست درون زا اولیه گیرنده 2 هیدروکسی کربوکسیلیک اسید انسانی ( HCA 2 ، همچنین به عنوان GPR109A) شناخته می شود، یک گیرنده G i/o -coupled G protein-coupled (GPCR)، [16] [17]
مانند سایر اسیدهای چرب با زنجیره کوتاه (SCFAs)، بوتیرات آگونیست گیرنده های اسید چرب آزاد FFAR2 و FFAR3 است که به عنوان حسگرهای مواد مغذی عمل می کنند که کنترل هموستاتیک تعادل انرژی را تسهیل می کنند . با این حال، در میان گروه SCFA ها، فقط بوتیرات آگونیست HCA 2 است . [37] [38] [39] همچنین یک مهارکننده HDAC (به ویژه HDAC1، HDAC2، HDAC3، و HDAC8)، [35] [36] دارویی است که عملکرد آنزیمهای هیستون داستیلاز را مهار میکند و در نتیجه حالت استیله را مطلوب میکند. هیستون ها در سلول ها [39] استیلاسیون هیستون با کاهش جاذبه الکترواستاتیکی بین هیستون ها و DNA ، ساختار کروماتین را شل می کند . [39] به طور کلی، تصور میشود که عوامل رونویسی قادر به دسترسی به مناطقی که هیستونها به شدت با DNA مرتبط هستند (به عنوان مثال، غیر استیله، به عنوان مثال، هتروکروماتین) نخواهند بود. [ نیاز به نقل از پزشکی ] بنابراین، تصور میشود که اسید بوتیریک فعالیت رونویسی را در پروموتورها افزایش میدهد، [39] که معمولاً به دلیل فعالیت هیستون داستیلاز خاموش یا تنظیم میشوند.
بوتیراتی که در روده بزرگ از طریق تخمیر میکروبی فیبر غذایی تولید می شود، در درجه اول توسط کلونوسیت ها و کبد برای تولید ATP در طول متابولیسم انرژی جذب و متابولیزه می شود . با این حال، مقداری بوتیرات در کولون دیستال جذب می شود، که به ورید پورتال متصل نیست، در نتیجه امکان توزیع سیستمیک بوتیرات به سیستم های چندگانه از طریق سیستم گردش خون را فراهم می کند. [39] [40] بوتیرات که به گردش خون سیستمیک رسیده است میتواند به آسانی از سد خونی مغزی از طریق ناقلهای مونوکربوکسیلات (یعنی اعضای خاصی از گروه ناقل SLC16A ) عبور کند. [41] [42] سایر ناقلین که واسطه عبور بوتیرات از غشاهای لیپیدی هستند عبارتند از SLC5A8 (SMCT1)، SLC27A1 (FATP1) و SLC27A4 (FATP4). [35] [42]
اسید بوتیریک توسط لیگازهای XM مختلف انسانی (ACSM1، ACSM2B، ASCM3، ACSM4، ACSM5، و ACSM6) متابولیزه می شود که به عنوان لیگاز بوتیرات-CoA نیز شناخته می شود. [43] [44] متابولیت تولید شده توسط این واکنش بوتیریل-CoA است و به شرح زیر تولید می شود: [43]
بوتیرات به عنوان یک اسید چرب با زنجیره کوتاه ، توسط میتوکندری به عنوان منبع انرژی (یعنی آدنوزین تری فسفات یا ATP) از طریق متابولیسم اسیدهای چرب متابولیزه می شود . [39] به ویژه، منبع انرژی مهمی برای سلول های پوشش دهنده روده بزرگ پستانداران (کلونوسیت ها) است. [25] بدون بوتیرات، سلولهای کولون تحت اتوفاژی (یعنی خود هضم) قرار میگیرند و میمیرند. [45]
در انسان، تریبوتیرین پیش ساز بوتیرات ، که به طور طبیعی در کره وجود دارد، توسط تری اسیل گلیسرول لیپاز به دی بوتیرین و بوتیرات از طریق واکنش متابولیزه می شود: [46]
بوتیرات اثرات متعددی بر روی هموستاز انرژی و بیماری های مرتبط ( دیابت و چاقی )، التهاب و عملکرد سیستم ایمنی (مثلاً اثرات ضد میکروبی و ضد سرطانی بارز ) در انسان دارد. این اثرات از طریق متابولیسم آن توسط میتوکندری برای تولید ATP در طی متابولیسم اسیدهای چرب یا از طریق یک یا چند هدف آنزیمی اصلاح کننده هیستون (یعنی کلاس I هیستون داستیلازها ) و اهداف گیرنده جفت شده با پروتئین G (یعنی FFAR2 ، FFAR3 ، و HCA 2 ). [37] [47]
بوتیرات برای میزبانی هموستاز ایمنی ضروری است. [37] اگرچه نقش و اهمیت بوتیرات در روده به طور کامل شناخته نشده است، بسیاری از محققان استدلال میکنند که کاهش باکتریهای تولیدکننده بوتیرات در بیماران مبتلا به چندین شرایط واسکولیتی برای پاتوژنز این اختلالات ضروری است. کاهش بوتیرات در روده معمولاً به دلیل فقدان یا کاهش باکتریهای تولیدکننده بوتیرات (BPB) ایجاد میشود. این کاهش در BPB منجر به دیس بیوز میکروبی می شود . این با تنوع زیستی کم و کاهش اعضای اصلی تولید کننده بوتیرات مشخص می شود. بوتیرات یک متابولیت میکروبی ضروری با نقش حیاتی به عنوان تعدیل کننده عملکرد مناسب ایمنی در میزبان است. نشان داده شده است که کودکان فاقد BPB بیشتر مستعد ابتلا به بیماری های آلرژیک [48] و دیابت نوع 1 هستند. [49] بوتیرات همچنین در رژیم غذایی کم فیبر غذایی کاهش مییابد که میتواند باعث التهاب شود و اثرات نامطلوب دیگری داشته باشد تا جایی که این اسیدهای چرب با زنجیره کوتاه PPAR-γ را فعال میکنند . [50]
بوتیرات نقش کلیدی برای حفظ هموستاز ایمنی هم به صورت موضعی (در روده) و هم به صورت سیستمی (از طریق بوتیرات در گردش) دارد. نشان داده شده است که تمایز سلول های T تنظیمی را تقویت می کند . به طور خاص، بوتیرات در گردش باعث تولید سلولهای T تنظیمکننده خارج تیمی میشود. سطوح پایین بوتیرات در افراد انسانی می تواند به کاهش کنترل با واسطه سلول T نظارتی کمک کند، در نتیجه یک پاسخ ایمنی-پاتولوژیک قدرتمند سلول T را ترویج می کند. [51] از سوی دیگر، بوتیرات روده گزارش شده است که سیتوکین های پیش التهابی موضعی را مهار می کند. بنابراین فقدان یا کاهش این BPB در روده می تواند کمک احتمالی در پاسخ التهابی بیش از حد فعال باشد. بوتیرات موجود در روده همچنین از یکپارچگی سد اپیتلیال روده محافظت می کند. بنابراین کاهش سطح بوتیرات منجر به یک سد اپیتلیال روده ای آسیب دیده یا ناکارآمد می شود. [52] کاهش بوتیرات نیز با تکثیر کلستریدیوئید دیفیسیل همراه است . برعکس، یک رژیم غذایی با فیبر بالا منجر به غلظت اسید بوتیریک بالاتر و مهار رشد C. difficile می شود . [53]
در یک مطالعه تحقیقاتی در سال 2013 که توسط Furusawa و همکاران انجام شد، مشخص شد که بوتیرات مشتق شده از میکروب در القای تمایز سلولهای T تنظیمکننده کولون در موشها ضروری است. این اهمیت زیادی دارد و احتمالاً به پاتوژنز و واسکولیت مرتبط با بسیاری از بیماریهای التهابی مرتبط است، زیرا سلولهای T تنظیمی نقش مرکزی در سرکوب پاسخهای التهابی و آلرژیک دارند. [54] در چندین مطالعه تحقیقاتی، نشان داده شده است که بوتیرات باعث تمایز سلول های T تنظیمی در شرایط آزمایشگاهی و درون تنی می شود. [55] ظرفیت ضد التهابی بوتیرات به طور گسترده توسط بسیاری از مطالعات مورد تجزیه و تحلیل و حمایت قرار گرفته است. مشخص شده است که بوتیرات تولید شده توسط میکروارگانیسمها تولید سلولهای T تنظیمی را تسریع میکند، اگرچه مکانیسم خاصی که توسط آن انجام میدهد نامشخص است. [56] اخیراً نشان داده شده است که بوتیرات نقش اساسی و مستقیمی در تعدیل بیان ژن سلولهای T سیتوتوکسیک دارد. [57] بوتیرات همچنین دارای اثر ضد التهابی بر نوتروفیل ها است و مهاجرت آنها را به سمت زخم ها کاهش می دهد. این اثر از طریق گیرنده HCA 1 انجام می شود . [58]
در میکروبیومهای روده که در کلاس پستانداران یافت میشوند، همه چیزخواران و گیاهخواران دارای جوامع باکتریایی تولیدکننده بوتیرات هستند که تحت سلطه مسیر کوآ ترانسفراز بوتیریل-CoA:استات است، در حالی که گوشتخواران دارای جوامع باکتریایی تولیدکننده بوتیرات هستند که مسیر بوتیرات کیناز بر آنها غالب است. [59]
بوی اسید بوتیریک که از فولیکول های چربی همه پستانداران خارج می شود، به عنوان یک سیگنال روی کنه عمل می کند.
اثرات بوتیرات بر روی سیستم ایمنی از طریق مهار هیستون داستیلازهای کلاس I و فعال سازی اهداف گیرنده جفت شده با پروتئین G آن انجام می شود : HCA 2 (GPR109A)، FFAR2 (GPR43) و FFAR3 (GPR41). [38] [60] در میان اسیدهای چرب با زنجیره کوتاه ، بوتیرات قویترین پروموتر سلولهای T تنظیمکننده روده در شرایط آزمایشگاهی و تنها در میان گروهی است که لیگاند HCA 2 است . [38] نشان داده شده است که یک واسطه مهم پاسخ التهابی کولون است. دارای پتانسیل پیشگیرانه و درمانی برای مقابله با کولیت اولسراتیو ناشی از التهاب و سرطان کولورکتال است .
بوتیرات خواص ضد میکروبی را در انسان ایجاد کرده است که از طریق پپتید ضد میکروبی LL-37 ایجاد می شود که از طریق مهار HDAC روی هیستون H3 ایجاد می کند. [60] [61] [62] در شرایط آزمایشگاهی، بوتیرات بیان ژن FOXP3 ( تنظیمکننده رونویسی Tregs ) را افزایش میدهد و سلولهای T تنظیمکننده کولون (Tregs) را از طریق مهار کلاس I هیستون داستیلازها تقویت میکند . [38] [60] از طریق این اقدامات، بیان اینترلوکین 10 ، یک سایتوکین ضد التهابی را افزایش می دهد . [60] [38] بوتیرات همچنین با مهار مسیرهای سیگنالینگ IFN-γ - STAT1 ، که تا حدی از طریق مهار هیستون داستیلاز انجام می شود، التهاب روده بزرگ را سرکوب می کند . در حالی که سیگنال دهی گذرا IFN-γ به طور کلی با پاسخ ایمنی طبیعی میزبان همراه است ، سیگنالینگ مزمن IFN-γ اغلب با التهاب مزمن همراه است. نشان داده شده است که بوتیرات فعالیت HDAC1 را که به پروموتر ژن Fas در سلولهای T متصل میشود، مهار میکند و در نتیجه پروموتر Fas افزایش مییابد و گیرنده Fas روی سطح سلول T تنظیم میشود. [63]
مشابه سایر آگونیست های HCA 2 مورد مطالعه، بوتیرات همچنین اثرات ضد التهابی مشخصی را در بافت های مختلف از جمله مغز، دستگاه گوارش، پوست و بافت عروقی ایجاد می کند . [64] [65] [66] اتصال بوتیرات در FFAR3 باعث آزاد شدن نوروپپتید Y می شود و هموستاز عملکردی مخاط روده بزرگ و سیستم ایمنی روده را ارتقا می دهد. [67]
نشان داده شده است که بوتیرات یک واسطه حیاتی برای پاسخ التهابی کولون است. این ماده مسئول حدود 70 درصد انرژی از کلونوسیت ها است که یک SCFA حیاتی در هموستاز کولون است . [68] بوتیرات دارای پتانسیل پیشگیرانه و درمانی برای مقابله با کولیت اولسراتیو با واسطه التهاب (UC) و سرطان کولورکتال است . [69] اثرات متفاوتی در سلولهای سالم و سرطانی ایجاد میکند: این به «پارادوکس بوتیرات» معروف است. به ویژه، بوتیرات سلول های تومور روده بزرگ را مهار می کند و تکثیر سلول های اپیتلیال کولون سالم را تحریک می کند. [70] [71] توضیح اینکه چرا بوتیرات منبع انرژی برای کلونوسیتهای طبیعی است و باعث القای آپوپتوز در سلولهای سرطانی کولون میشود، اثر Warburg در سلولهای سرطانی است که منجر به متابولیزه نشدن بوتیرات به درستی میشود. این پدیده منجر به تجمع بوتیرات در هسته می شود که به عنوان یک مهار کننده هیستون داستیلاز (HDAC) عمل می کند. [72] یک مکانیسم زیربنایی عملکرد بوتیرات در سرکوب التهاب کولون، مهار مسیرهای سیگنالینگ IFN-γ / STAT1 است . نشان داده شده است که بوتیرات فعالیت HDAC1 را که به پروموتر ژن Fas در سلولهای T متصل میشود ، مهار میکند و در نتیجه پروموتر Fas افزایش مییابد و گیرنده Fas روی سطح سلول T تنظیم میشود. بنابراین پیشنهاد می شود که بوتیرات آپوپتوز سلول های T را در بافت کولون افزایش می دهد و در نتیجه منبع التهاب (تولید IFN-γ) را از بین می برد. [73] بوتیرات با غیرفعال کردن فعالیت فاکتور رونویسی Sp1 و کاهش بیان ژن فاکتور رشد اندوتلیال عروقی، رگزایی را مهار می کند . [74]
به طور خلاصه، تولید اسیدهای چرب فرار مانند بوتیرات از الیاف قابل تخمیر ممکن است به نقش فیبر غذایی در سرطان روده بزرگ کمک کند. اسیدهای چرب با زنجیره کوتاه ، که شامل اسید بوتیریک میشود، توسط باکتریهای مفید روده بزرگ ( پروبیوتیکها ) که از آن تغذیه میکنند یا پروبیوتیکها را تخمیر میکنند، که محصولات گیاهی حاوی فیبر غذایی هستند، تولید میشوند . این اسیدهای چرب با زنجیره کوتاه با افزایش تولید انرژی به کلونوسیت ها کمک می کنند و ممکن است با مهار تکثیر سلولی در برابر سرطان روده بزرگ محافظت کنند. [22]
برعکس، برخی از محققان به دنبال حذف بوتیرات و در نظر گرفتن آن یک محرک بالقوه سرطان بوده اند. [75] مطالعات روی موشها نشان میدهد که باعث تغییر سلولهای اپیتلیال کولون با کمبود MSH2 میشود . [76]
با توجه به اهمیت بوتیرات به عنوان یک تنظیم کننده التهاب و کمک کننده سیستم ایمنی، کاهش بوتیرات می تواند یک عامل کلیدی موثر بر پاتوژنز بسیاری از شرایط واسکولیتی باشد. بنابراین حفظ سطوح سالم بوتیرات در روده ضروری است. پیوند میکروبیوتای مدفوع (برای بازگرداندن BPB و همزیستی در روده) می تواند با پر کردن سطوح بوتیرات موثر باشد. در این درمان، یک فرد سالم مدفوع خود را اهدا می کند تا به فرد مبتلا به دیس بیوز پیوند شود. یک گزینه درمانی کم تهاجمی، تجویز بوتیرات - به عنوان مکمل های خوراکی یا تنقیه - است که نشان داده شده است در خاتمه علائم التهاب با حداقل تا بدون عوارض جانبی بسیار موثر است. در مطالعه ای که در آن بیماران مبتلا به کولیت اولسراتیو با تنقیه بوتیرات تحت درمان قرار گرفتند، التهاب به طور قابل توجهی کاهش یافت و خونریزی به طور کامل پس از تهیه بوتیرات متوقف شد. [77]
اسید بوتیریک یک HDAC استمهارکننده ای که برای HDAC های کلاس I در انسان انتخابی است. [35] HDAC ها آنزیم های اصلاح کننده هیستون هستند که می توانند باعث دی استیلاسیون هیستون و سرکوب بیان ژن شوند. HDAC ها تنظیم کننده های مهم تشکیل سیناپسی، شکل پذیری سیناپسی و تشکیل حافظه بلند مدت هستند . HDACهای کلاس I در میانجیگری در ایجاد اعتیاد نقش دارند . [78] [79] [80] اسید بوتیریک و سایر مهارکنندههای HDAC در تحقیقات پیش بالینی برای ارزیابی اثرات رونویسی، عصبی و رفتاری مهار HDAC در حیوانات معتاد به مواد مخدر استفاده شدهاند. [80] [81] [82]
یون بوتیرات یا بوتانوات ، C3H7COO- ، باز مزدوج اسید بوتیریک است . این شکلی است که در سیستم های بیولوژیکی در pH فیزیولوژیکی یافت می شود . یک ترکیب بوتیریک (یا بوتانوئیک) یک نمک کربوکسیلات یا استر اسید بوتیریک است.
این مقاله شامل متنی از یک نشریه است که اکنون در مالکیت عمومی است : Chisholm, Hugh , ed. (1911). "اسید بوتیریک". دایره المعارف بریتانیکا (ویرایش یازدهم). انتشارات دانشگاه کمبریج
اسیدهای چرب با زنجیره کوتاه (SCFAs) مانند استات، بوتیرات و پروپیونات که توسط تخمیر میکروبی روده فیبر غذایی تولید می شوند، به عنوان منابع انرژی میزبان ضروری شناخته می شوند و به عنوان مولکول های انتقال سیگنال از طریق گیرنده های جفت شده با پروتئین G عمل می کنند. (FFAR2، FFAR3، OLFR78، GPR109A) و به عنوان تنظیم کننده های اپی ژنتیکی بیان ژن با مهار هیستون داستیلاز (HDAC). شواهد اخیر نشان می دهد که فیبر غذایی و SCFA های مشتق شده از میکروبی روده اثرات مفید متعددی بر متابولیسم انرژی میزبان نه تنها از طریق بهبود محیط روده، بلکه با تأثیر مستقیم بر بافت های مختلف محیطی میزبان اعمال می کنند.
وریدهای راست روده میانی و تحتانی قسمت تحتانی رکتوم را تخلیه می کنند و خون وریدی به ورید اجوف تحتانی باز می گردد. بنابراین، داروهای جذب شده در سیستم دوم ترجیحاً به گردش خون سیستمیک تحویل داده می شود، کبد را دور می زند و از متابولیسم عبور اول جلوگیری می کند.
سایر مطالعات in vivo در آزمایشگاههای ما نشان داد که چندین ترکیب از جمله استات، پروپیونات، بوتیرات، اسید بنزوئیک، اسید سالیسیلیک، اسید نیکوتین و برخی از آنتیبیوتیکهای β-لاکتام ممکن است توسط MCT در BBB منتقل شوند.
21
... جذب اسید والپروئیک در حضور اسیدهای چرب با زنجیره متوسط مانند هگزانوات، اکتانوات و دکانوات کاهش یافت، اما نه پروپیونات یا بوتیرات، که نشان می دهد والپروئیک اسید از طریق یک سیستم انتقال برای محیط به مغز جذب می شود. - اسیدهای چرب زنجیره ای، نه اسیدهای چرب با زنجیره کوتاه.
انتقال دهنده های مونوکربوکسیلات (MCTs) به عنوان واسطه انتقال مونوکربوکسیلات های زنجیره کوتاه مانند لاکتات، پیروات و بوتیرات شناخته شده اند. ... MCT1 و MCT4 همچنین با انتقال اسیدهای چرب با زنجیره کوتاه مانند استات و فورمات که سپس در آستروسیت ها متابولیزه می شوند، مرتبط بوده اند [78]. ... SLC5A8 در بافت طبیعی کولون بیان می شود و به عنوان یک سرکوب کننده تومور در کولون انسان عمل می کند و این ژن در کارسینوم کولون رخ می دهد. این ناقل در جذب متمرکز بوتیرات و پیروات تولید شده به عنوان محصول تخمیر توسط باکتری های کولون نقش دارد.
{{cite encyclopedia}}: |website=نادیده گرفته شد ( کمک )