اسید نیتریک یک ترکیب معدنی با فرمول H N O 3 است . این یک اسید معدنی بسیار خورنده است . [6] این ترکیب بی رنگ است، اما نمونه ها به مرور زمان به دلیل تجزیه به اکسیدهای نیتروژن، رنگ زردی پیدا می کنند . بیشتر اسید نیتریک موجود در بازار دارای غلظت 68 درصد در آب است. هنگامی که محلول حاوی بیش از 86٪ HNO 3 باشد ، به آن اسید نیتریک دود گفته می شود . بسته به مقدار دی اکسید نیتروژن موجود، اسید نیتریک دوددار بیشتر به عنوان اسید نیتریک دوددار قرمز در غلظت های بالاتر از 86٪ یا اسید نیتریک دوددار سفید در غلظت های بالاتر از 95٪ مشخص می شود.
اسید نیتریک معرف اولیه ای است که برای نیتراسیون استفاده می شود - افزودن یک گروه نیترو ، به طور معمول به یک مولکول آلی . در حالی که برخی از ترکیبات نیترو حاصل ، مواد منفجره حساس به شوک و حرارت هستند ، برخی از آنها به اندازه کافی پایدار هستند که در مهمات و تخریب استفاده شوند، در حالی که برخی دیگر هنوز پایدارتر هستند و به عنوان رنگ های مصنوعی و دارو استفاده می شوند (مثلا مترونیدازول ). اسید نیتریک نیز معمولا به عنوان یک عامل اکسید کننده قوی استفاده می شود .
اعتقاد بر این است که کشف اسیدهای معدنی مانند اسید نیتریک به کیمیاگری قرن سیزدهم اروپا برمی گردد . [7] دیدگاه مرسوم این است که اسید نیتریک برای اولین بار در شبه گیبر De invente veritatis ("درباره کشف حقیقت"، پس از حدود 1300 ) توصیف شد. [8]
با این حال، به گفته اریک جان هولمیارد و احمد ی.الحسن ، اسید نیتریک در آثار قبلی عربی مانند صندوق الحکمه منسوب به جابر بن حیان (قرن هشتم) یا تعویض الحاکم منسوب به خلیفه فاطمی الحکیم بعمر الله (985-1021). [9]
دستور العمل در صندوق الحکمه منسوب به جابر چنین ترجمه شده است: [10] [11]
پنج قسمت از گلهای خالص نیتر ، سه قسمت ویتریول قبرس و دو قسمت زاج یمن را بردارید . آن ها را به طور جداگانه به خوبی پودر کنید تا مانند گرد و غبار شوند و سپس آن ها را در فلاسک قرار دهید. دومی را با یک فیبر کف دست وصل کنید و یک گیرنده شیشه ای را به آن وصل کنید. سپس دستگاه را برعکس کرده و قسمت بالایی (یعنی فلاسک حاوی مخلوط) را با آتش ملایم گرم کنید. در اثر حرارت، روغنی مانند کره گاو به پایین سرازیر خواهد شد.
اسید نیتریک همچنین در آثار پس از 1300 یافت می شود که به دروغ به آلبرت کبیر و رامون لول (هر دو قرن سیزدهم) نسبت داده شده است. این آثار تقطیر مخلوطی حاوی نیتر و ویتریول سبز را توصیف می کنند که آن را "eau forte" (آکوا فورتیس) می نامند. [12] [13] [14]
در قرن هفدهم، یوهان رودولف گلابر فرآیندی را برای بدست آوردن اسید نیتریک با تقطیر نیترات پتاسیم با اسید سولفوریک ابداع کرد. در سال 1776 آنتوان لاووازیه از کار جوزف پریستلی استناد کرد تا به این نکته اشاره کند که می توان آن را از اکسید نیتریک (که او آن را "هوای نیتروژن" می نامد)، "ترکیب با حجم تقریباً مساوی از خالص ترین قسمت هوای معمولی و با مقدار قابل توجهی تبدیل کرد. مقدار آب." [15] [a] در سال 1785 هنری کاوندیش ترکیب دقیق آن را تعیین کرد و نشان داد که می توان آن را با عبور جریانی از جرقه های الکتریکی از هوای مرطوب سنتز کرد . [12] در سال 1806، هامفری دیوی نتایج آزمایشهای گسترده الکترولیز آب مقطر را گزارش کرد که به این نتیجه رسید که اسید نیتریک در آند از گاز نیتروژن اتمسفر محلول تولید میشود. او از یک باتری ولتاژ بالا و الکترودهای غیر واکنشی و مخروطهایی مانند مخروطهای الکترود طلایی استفاده کرد که بهعنوان رگهایی که توسط آزبست مرطوب پل میشوند، دو برابر میشوند. [16]
تولید صنعتی اسید نیتریک از هوای اتمسفر در سال 1905 با فرآیند Birkeland-Eyde که به نام فرآیند قوس نیز شناخته می شود، آغاز شد. [17] این فرآیند مبتنی بر اکسیداسیون نیتروژن اتمسفر توسط اکسیژن اتمسفر به اکسید نیتریک با قوس الکتریکی با دمای بسیار بالا است. بازده تا حدود 4-5٪ اکسید نیتریک در 3000 درجه سانتیگراد و کمتر در دماهای پایین تر به دست آمد. [17] [18] اکسید نیتریک خنک شد و توسط اکسیژن اتمسفر باقیمانده به دی اکسید نیتروژن اکسید شد و متعاقباً در آب در یک سری از ستونها یا برجهای جذب ستون پرشده برای تولید اسید نیتریک رقیق جذب شد. اولین برج ها دی اکسید نیتروژن را از طریق آب و قطعات غیر واکنشی کوارتز حباب زدند. حدود 20 درصد از اکسیدهای نیتروژن تولید شده بدون واکنش باقی ماندند، بنابراین برج های نهایی حاوی محلول قلیایی برای خنثی کردن بقیه بودند. [19] این فرآیند بسیار انرژی بر بود و زمانی که آمونیاک ارزان در دسترس قرار گرفت، به سرعت توسط فرآیند استوالد جابجا شد.
یکی دیگر از روش های اولیه تولید توسط مهندس فرانسوی آلبرت نودون در حدود سال 1913 اختراع شد. روش او اسید نیتریک را از الکترولیز نیترات کلسیم تبدیل شده توسط باکتری ها از مواد نیتروژن دار در باتلاق های ذغال سنگ نارس تولید کرد. یک گلدان سفالی که توسط سنگ آهک احاطه شده بود در ذغال سنگ نارس فرو رفته و با الوارهای قیر خورده روی آن قرار داده شد تا محفظه ای برای آند کربنی ایجاد شود که در اطراف آن اسید نیتریک تشکیل می شود. اسید نیتریک از یک لوله سفالی [20] که تا ته دیگ فرو رفته بود، خارج می شد . آب تازه از طریق یک لوله سفالی دیگر به سمت بالا پمپ می شد تا جایگزین مایع خارج شده شود. فضای داخلی پر از کک بود . کاتدهای چدن در ذغال سنگ نارس اطراف آن فرو رفته بودند. مقاومت حدود 3 اهم بر متر مکعب و برق عرضه شده حدود 10 ولت بود. تولید از یک کانسار 800 تن در سال بود. [20] [21]
هنگامی که فرآیند هابر برای تولید کارآمد آمونیاک در سال 1913 معرفی شد، تولید اسید نیتریک از آمونیاک با استفاده از فرآیند Ostwald بر تولید از فرآیند Birkeland-Eyde پیشی گرفت. این روش تولید هنوز هم مورد استفاده قرار می گیرد.
اسید نیتریک موجود در بازار یک آزئوتروپ با آب با غلظت 68% HNO3 است . این محلول دارای دمای جوش 120.5 درجه سانتیگراد (249 درجه فارنهایت) در 1 اتمسفر است. به نام "اسید نیتریک غلیظ" شناخته می شود. آزئوتروپ اسید نیتریک و آب یک مایع بی رنگ در دمای اتاق است.
دو هیدرات جامد شناخته شده اند: مونوهیدرات HNO 3 · H 2 O یا نیترات اکسونیوم [H 3 O] + [NO 3 ] - و تری هیدرات HNO 3 · 3H 2 O .
مقیاس چگالی قدیمیتر گاهی دیده میشود، با اسید نیتریک غلیظ که با نام 42 Baumé مشخص شده است . [22]

اسید نیتریک در معرض تجزیه حرارتی یا سبک است و به همین دلیل اغلب در بطری های شیشه ای قهوه ای ذخیره می شود:
این واکنش ممکن است منجر به تغییرات غیر قابل چشم پوشی در فشار بخار بالای مایع شود زیرا اکسیدهای نیتروژن تولید شده به طور جزئی یا کامل در اسید حل می شوند.
دی اکسید نیتروژن ( NO 2 ) و / یا تتروکسید دی نیتروژن ( N 2 O 4 ) به صورت محلول در اسید نیتریک باقی می ماند و آن را در دماهای بالاتر زرد یا حتی قرمز رنگ می کند. در حالی که اسید خالص هنگام قرار گرفتن در معرض هوا بخارهای سفید رنگی از خود خارج می کند، اسید با دی اکسید نیتروژن محلول بخارات قهوه ای مایل به قرمز تولید می کند که منجر به نام های رایج "اسید نیتریک بخاردار قرمز" و "اسید نیتریک دوددار سفید" می شود. اکسیدهای نیتروژن ( NOx ) در اسید نیتریک محلول هستند.
اسید نیتریک دوددار تجاری دارای 98 درصد HNO 3 و چگالی آن 1.50 گرم بر سانتی متر مکعب است . این درجه اغلب در صنعت مواد منفجره استفاده می شود. به اندازه اسید بی آب فرار و خورنده نیست و غلظت تقریبی آن 21.4 M است.
اسید نیتریک گازدار قرمز یا RFNA حاوی مقادیر قابل توجهی دی اکسید نیتروژن محلول ( NO 2 ) است که محلول را با رنگ قهوه ای مایل به قرمز باقی می گذارد. به دلیل دی اکسید نیتروژن محلول، چگالی اسید نیتریک دوددار قرمز کمتر در 1.490 گرم بر سانتی متر مکعب است .
یک اسید نیتریک بخاردار مهار شده ، یا اسید نیتریک بخاردار سفید (IWFNA)، یا اسید نیتریک بخاردار مهار شده قرمز (IRFNA)، میتواند با افزودن 0.6 تا 0.7 درصد هیدروژن فلوراید (HF) ساخته شود. این فلوراید برای مقاومت در برابر خوردگی در مخازن فلزی اضافه می شود. فلوراید یک لایه فلوراید فلزی ایجاد می کند که از فلز محافظت می کند.
اسید نیتریک دود سفید، اسید نیتریک خالص یا WFNA، بسیار نزدیک به اسید نیتریک بی آب است. این به صورت اسید نیتریک 99.9٪ با روش یا حدود 24 مولار در دسترس است . یکی از مشخصات اسید نیتریک دود سفید این است که حداکثر 2٪ آب و حداکثر 0.5٪ NO 2 محلول دارد . اسید نیتریک بی آب یک مایع بی رنگ و با ویسکوزیته کم (متحرک) با چگالی 1.512-3 گرم بر سانتی متر مکعب است که در دمای 42- درجه سانتی گراد (44- درجه فارنهایت) جامد می شود و کریستال های سفید تشکیل می دهد. [ نیازمند منبع ] ویسکوزیته دینامیکی آن در شرایط استاندارد 0.76 cP است. [23] همانطور که به NO 2 و آب تجزیه می شود، رنگ زردی به دست می آورد. در 83 درجه سانتیگراد (181 درجه فارنهایت) می جوشد. معمولاً در یک بطری شیشهای کهربایی نشکن با دو برابر فضای سر ذخیره میشود تا فشار ایجاد شود، اما حتی با وجود این اقدامات احتیاطی، بطری باید ماهیانه تخلیه شود تا فشار کاهش یابد.
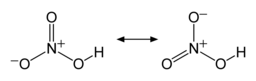
دو پیوند انتهایی N-O تقریباً معادل و نسبتاً کوتاه هستند، در 1.20 و 1.21 Å. [24] این را می توان با نظریه های تشدید توضیح داد . دو شکل اصلی متعارف برخی از ویژگی های پیوند دوگانه را در این دو پیوند نشان می دهند که باعث می شود آنها کوتاهتر از پیوندهای منفرد N–O باشند . سومین پیوند N-O دراز است زیرا اتم O آن به اتم H پیوند دارد، [25] [26] با طول پیوند 1.41 Å در فاز گاز. [24] مولکول کمی صاف است ( صفحه های NO 2 و NOH 2 درجه از یکدیگر متمایل شده اند) و چرخش محدودی در اطراف پیوند منفرد N-OH وجود دارد. [6] [27]
اسید نیتریک به طور معمول در دمای محیط به عنوان یک اسید قوی در نظر گرفته می شود. در مورد مقدار ثابت تفکیک اسید اختلاف نظر وجود دارد، اگرچه مقدار p K a معمولاً کمتر از 1- گزارش می شود. این بدان معنی است که اسید نیتریک در محلول رقیق شده به جز در محلول های بسیار اسیدی کاملاً تجزیه می شود. مقدار p K a در دمای 250 درجه سانتیگراد به 1 افزایش می یابد. [28]
اسید نیتریک می تواند به عنوان یک پایه با توجه به اسیدی مانند اسید سولفوریک عمل کند :
یون نیترونیوم ، [NO 2 ] + ، معرف فعال در واکنش های نیتراسیون آروماتیک است . از آنجایی که اسید نیتریک دارای هر دو خاصیت اسیدی و بازی است، می تواند تحت یک واکنش اتوپروتولیز، مشابه خود یونیزاسیون آب قرار گیرد :
اسید نیتریک با اکثر فلزات واکنش می دهد، اما جزئیات به غلظت اسید و ماهیت فلز بستگی دارد. اسید نیتریک رقیق در واکنش با اکثر فلزات مانند یک اسید معمولی رفتار می کند . منیزیم ، منگنز و روی H2 را آزاد می کنند :
اسید نیتریک می تواند فلزات غیر فعال مانند مس و نقره را اکسید کند . با این فلزات غیر فعال یا کمتر الکترومثبت، محصولات به دما و غلظت اسید بستگی دارند. به عنوان مثال، مس با اسید نیتریک رقیق در دمای محیط با استوکیومتری 3:8 واکنش می دهد:
اکسید نیتریک تولید شده ممکن است با اکسیژن اتمسفر واکنش داده و دی اکسید نیتروژن تولید کند . با اسید نیتریک غلیظ تر، دی اکسید نیتروژن مستقیماً در یک واکنش با استوکیومتری 1:4 تولید می شود:
پس از واکنش با اسید نیتریک، اکثر فلزات نیترات های مربوطه را تولید می کنند . برخی از فلزات و فلزات اکسید می دهند . به عنوان مثال، Sn ، As ، Sb ، و Ti به ترتیب به SnO 2 ، As 2 O 5 ، Sb 2 O 5 و TiO 2 اکسید می شوند . [29]
برخی از فلزات گرانبها ، مانند طلای خالص و فلزات گروه پلاتین، با اسید نیتریک واکنش نمی دهند، اگرچه طلای خالص با آبی رژیا ، مخلوطی از اسید نیتریک غلیظ و اسید هیدروکلریک ، واکنش نشان می دهد . با این حال، برخی از فلزات کمتر نجیب ( نقره ، مس ، ...) موجود در برخی از آلیاژهای طلای نسبتاً فقیر مانند طلای رنگی می توانند به راحتی توسط اسید نیتریک اکسید و حل شوند و منجر به تغییر رنگ سطح آلیاژ طلا شود. اسید نیتریک به عنوان وسیله ای ارزان در جواهر فروشی ها برای شناسایی سریع آلیاژهای کم طلا (کمتر از 14 قیراط ) و ارزیابی سریع خلوص طلا استفاده می شود.
به عنوان یک عامل اکسید کننده قوی، اسید نیتریک با بسیاری از ترکیبات غیرفلزی واکنش می دهد، گاهی اوقات به صورت انفجاری. بسته به غلظت اسید، دما و عامل کاهنده درگیر، محصولات نهایی می توانند متغیر باشند. واکنش با تمام فلزات به جز سری فلزات نجیب و آلیاژهای خاص صورت می گیرد . به عنوان یک قاعده کلی، واکنشهای اکسیدکننده عمدتاً با اسید غلیظ رخ میدهد و به تشکیل دی اکسید نیتروژن ( NO 2 ) کمک میکند. با این حال، خواص اکسید کننده قوی اسید نیتریک ماهیت ترمودینامیکی دارد، اما گاهی اوقات واکنش های اکسیداسیون آن از نظر جنبشی نامطلوب است. وجود مقادیر کم اسید نیتروژن ( HNO 2 ) سرعت واکنش را به شدت افزایش می دهد. [29]
اگرچه کروم (Cr)، آهن (Fe) و آلومینیوم (Al) به آسانی در اسید نیتریک رقیق حل می شوند، اسید غلیظ یک لایه اکسید فلزی را تشکیل می دهد که از قسمت عمده فلز در برابر اکسیداسیون بیشتر محافظت می کند. تشکیل این لایه محافظ را غیرفعال سازی می نامند . [29] غلظت غیرفعال سازی معمولی از 20٪ تا 50٪ حجمی متغیر است. [30] [ نیاز به نقل قول کامل ] فلزاتی که توسط اسید نیتریک غلیظ غیرفعال می شوند عبارتند از آهن ، کبالت ، کروم ، نیکل و آلومینیوم . [29]
به عنوان یک اسید اکسید کننده قوی ، اسید نیتریک با بسیاری از مواد آلی واکنش می دهد و واکنش ها ممکن است انفجاری باشد. گروه هیدروکسیل معمولاً یک هیدروژن را از مولکول آلی جدا می کند تا آب را تشکیل دهد و گروه نیترو باقی مانده جای هیدروژن را می گیرد. نیتراسیون ترکیبات آلی با اسید نیتریک روش اصلی سنتز بسیاری از مواد منفجره رایج مانند نیتروگلیسیرین و تری نیتروتولوئن (TNT) است. از آنجایی که بسیاری از محصولات جانبی کمتر پایدار امکان پذیر است، این واکنش ها باید به دقت کنترل شوند و محصولات جانبی حذف شوند تا محصول مورد نظر جدا شود.
واکنش با عناصر غیرفلزی، به استثنای نیتروژن، اکسیژن، گازهای نجیب ، سیلیکون و هالوژن به غیر از ید، معمولاً آنها را به بالاترین حالت اکسیداسیون خود به عنوان اسید با تشکیل دی اکسید نیتروژن برای اسید غلیظ و اکسید نیتریک برای رقیق شدن اکسید می کند. اسید
اسید نیتریک غلیظ I2 ، P4 و S8 را به ترتیب به HIO3 ، H3PO4 و H2SO4 اکسید می کند . [29] اگرچه با گرافیت و کربن آمورف واکنش می دهد، اما با الماس واکنش نمی دهد. می تواند الماس را از گرافیت که اکسید می کند جدا کند. [31]
اسید نیتریک با پروتئین ها واکنش می دهد و محصولات نیترات دار زرد را تشکیل می دهد. این واکنش به عنوان واکنش زانتوپروتئیک شناخته می شود . این آزمایش با افزودن اسید نیتریک غلیظ به ماده مورد آزمایش و سپس حرارت دادن مخلوط انجام می شود. اگر پروتئین هایی که حاوی اسیدهای آمینه با حلقه های معطر هستند وجود داشته باشد، مخلوط زرد می شود. با افزودن پایه ای مانند آمونیاک ، رنگ نارنجی می شود. این تغییرات رنگی ناشی از حلقه های معطر نیتراتی در پروتئین است. [32] [33] اسید زانتوپروتئیک زمانی تشکیل میشود که اسید با سلولهای اپیتلیال تماس پیدا کند . تغییرات رنگ پوست محلی مربوطه نشان دهنده اقدامات احتیاطی ناکافی هنگام استفاده از اسید نیتریک است.
تولید اسید نیتریک صنعتی از فرآیند Ostwald استفاده می کند . فرآیندهای ترکیبی استوالد و هابر بسیار کارآمد هستند و فقط به هوا و گاز طبیعی نیاز دارند . [34]
نوآوری فنی فرآیند Ostwald شرایط مناسبی است که در آن آمونیاک بی آب به جای دی نیتروژن ( N2 ) به اکسید نیتریک (NO) می سوزد . [34] [35] سپس اکسید نیتریک، اغلب با اکسیژن اتمسفر ، به دی اکسید نیتروژن ( NO 2 ) اکسید می شود:
سپس دی اکسید در آب با اسید نیتریک و مواد اولیه اکسید نیتریک نامتناسب می شود:
واکنش خالص حداکثر اکسیداسیون آمونیاک است:
اکسیدهای نیتروژن محلول یا از بین میروند (در مورد اسید نیتریک بخاردار سفید) یا در محلول باقی میمانند تا اسید نیتریک بخاردار قرمز را تشکیل دهند .
محلول های اسید نیتریک درجه تجاری معمولاً بین 52 تا 68 درصد اسید نیتریک بر حسب جرم هستند که حداکثر غلظت قابل تقطیر است . کم آبی بیشتر تا 98 درصد را می توان با H 2 SO 4 غلیظ به دست آورد . [34] [36] از نظر تاریخی، غلظتهای اسید بالاتر نیز با حل کردن دی اکسید نیتروژن اضافی در اسید تولید میشد، اما آخرین کارخانه در ایالات متحده استفاده از این فرآیند را در سال 2012 متوقف کرد. [36]
اخیراً وسایل الکتروشیمیایی برای تولید اسید بی آب از مواد اولیه اسید نیتریک غلیظ ساخته شده است. [37]
سنتز اسید نیتریک در مقیاس آزمایشگاهی فراوان است. بیشتر آنها از تکنیک های صنعتی الهام می گیرند.
طیف گسترده ای از نمک های نیترات با اسید سولفوریک (H2SO4 ) متاتز می شوند - به عنوان مثال، نیترات سدیم :
تقطیر در نقطه جوش 83 درجه سانتیگراد اسید نیتریک، باقیمانده جامد فلز-نمک را جدا می کند. [26] محلول اسیدی حاصل 68.5% آزئوتروپ است و میتواند بیشتر (مانند صنعت) با اسید سولفوریک یا نیترات منیزیم تغلیظ شود . [36]
روش دیگر، تجزیه حرارتی نیترات مس (II) دی اکسید نیتروژن و گازهای اکسیژن می دهد. اینها سپس از طریق آب یا پراکسید هیدروژن [38] مانند فرآیند استوالد عبور داده می شوند:

عمده ترین کاربرد صنعتی اسید نیتریک برای تولید کود است . اسید نیتریک با آمونیاک خنثی می شود و نیترات آمونیوم می دهد . این برنامه 75 تا 80 درصد از 26 میلیون تن تولید سالانه (1987) را مصرف می کند. کاربردهای اصلی دیگر برای تولید مواد منفجره، پیش سازهای نایلون و ترکیبات آلی ویژه است. [39]
در سنتز آلی ، صنعتی و غیره، گروه نیترو یک گروه عملکردی همه کاره است . مخلوطی از اسیدهای نیتریک و سولفوریک یک جایگزین نیترو را با جایگزینی معطر الکتروفیل به ترکیبات معطر مختلف وارد می کند . بسیاری از مواد منفجره مانند TNT به این ترتیب تهیه می شوند:
اسید سولفوریک غلیظ یا اولئوم آب اضافی را جذب می کند.
گروه نیترو را می توان کاهش داد تا یک گروه آمین به دست آورد که امکان سنتز ترکیبات آنیلین از نیتروبنزن های مختلف را فراهم می کند :
پیش ساز نایلون ، اسید آدیپیک ، در مقیاس بزرگ با اکسیداسیون «روغن KA» - مخلوطی از سیکلوهگزانون و سیکلوهگزانول - با اسید نیتریک تولید می شود. [39]
اسید نیتریک به اشکال مختلف به عنوان اکسید کننده در موشک های سوخت مایع استفاده شده است . این اشکال شامل اسید نیتریک بخاردار قرمز، اسید نیتریک بخاردار سفید، مخلوط با اسید سولفوریک و این اشکال با بازدارنده HF است. [40] IRFNA ( اسید نیتریک گازدار قرمز مهار شده ) یکی از سه جزء سوخت مایع برای موشک BOMARC بود . [41]
از اسید نیتریک می توان برای تبدیل فلزات به اشکال اکسید شده مانند تبدیل فلز مس به نیترات مس استفاده کرد . همچنین می توان از آن در ترکیب با اسید هیدروکلریک به عنوان آبزیان برای حل کردن فلزات نجیب مانند طلا (به عنوان اسید کلرواوریک ) استفاده کرد. این نمک ها را می توان برای خالص سازی طلا و سایر فلزات با خلوص بیش از 99.9٪ با فرآیندهای تبلور مجدد و رسوب انتخابی استفاده کرد . توانایی آن در حل انتخابی فلزات خاص یا حلال بودن بسیاری از نمک های فلزی، آن را در فرآیندهای جداسازی طلا مفید می کند.
در آنالیز عنصری توسط ICP-MS ، ICP-AES ، GFAA، و Flame AA، اسید نیتریک رقیق (0.5-5.0٪) به عنوان یک ترکیب ماتریکس برای تعیین آثار فلزی در محلول ها استفاده می شود. [42] اسید درجه فلز ردیابی فوق خالص برای چنین تعیینی مورد نیاز است، زیرا مقادیر کمی از یون های فلزی می تواند بر نتیجه تجزیه و تحلیل تأثیر بگذارد.
همچنین معمولاً در فرآیند هضم نمونههای آب کدر، نمونههای لجن، نمونههای جامد و همچنین انواع دیگر نمونههای منحصربهفرد که نیاز به آنالیز عنصری از طریق ICP-MS ، ICP-OES ، ICP-AES ، GFAA و طیفسنجی جذب اتمی شعله دارند، استفاده میشود. . معمولاً این هضم ها از محلول 50 درصدی HNO 3 خریداری شده مخلوط با آب نوع 1 DI استفاده می کنند.
در الکتروشیمی ، اسید نیتریک به عنوان یک عامل دوپینگ شیمیایی برای نیمه هادی های آلی و در فرآیندهای خالص سازی برای نانولوله های کربنی خام استفاده می شود .
در غلظت کم (تقریباً 10٪)، اسید نیتریک اغلب برای پیری مصنوعی کاج و افرا استفاده می شود . رنگ تولید شده خاکستری مایل به طلایی است که بسیار شبیه به چوب بسیار قدیمی مومی یا روغنی ( پرونده چوب ) است. [43]
از اثرات خورنده اسید نیتریک برای برخی از کاربردهای خاص، مانند اچ کردن در چاپ، ترشی فولاد ضد زنگ یا تمیز کردن ویفرهای سیلیکونی در الکترونیک استفاده می شود. [44]
محلولی از اسید نیتریک، آب و الکل، نیتال ، برای حکاکی فلزات به منظور آشکار ساختن ریزساختار استفاده می شود. ISO 14104 یکی از استانداردهایی است که این روش شناخته شده را شرح می دهد. [45]
اسید نیتریک یا در ترکیب با اسید هیدروکلریک یا به تنهایی برای تمیز کردن لغزش های پوشش شیشه ای و لام های شیشه ای برای کاربردهای میکروسکوپی پیشرفته استفاده می شود. [46] همچنین برای تمیز کردن شیشه قبل از نقرهکاری هنگام ساخت آینههای نقره استفاده میشود. [47]
مخلوطهای آبی موجود در بازار از اسید نیتریک 5 تا 30 درصد و اسید فسفریک 15 تا 40 درصد معمولاً برای تمیز کردن مواد غذایی و تجهیزات لبنی عمدتاً برای حذف ترکیبات کلسیم و منیزیم رسوبشده (یا رسوبشده از جریان فرآیند یا ناشی از استفاده از آب سخت) استفاده میشوند. در طول تولید و تمیز کردن). محتوای اسید فسفریک به غیرفعال کردن آلیاژهای آهنی در برابر خوردگی توسط اسید نیتریک رقیق کمک می کند. [ نیازمند منبع ]
اسید نیتریک را می توان به عنوان یک آزمایش نقطه ای برای آلکالوئیدهایی مانند LSD استفاده کرد که بسته به آلکالوئید رنگ های متنوعی را ارائه می دهد. [48]
اسید نیتریک نقش کلیدی در PUREX و سایر روشهای بازفرآوری سوخت هستهای دارد ، جایی که میتواند بسیاری از اکتینیدهای مختلف را حل کند . نیترات های به دست آمده به کمپلکس های مختلفی تبدیل می شوند که می توانند واکنش داده و به صورت انتخابی استخراج شوند تا فلزات از یکدیگر جدا شوند.
اسید نیتریک یک اسید خورنده و یک عامل اکسید کننده قوی است . خطر اصلی ناشی از آن سوختگی های شیمیایی است، زیرا هیدرولیز اسیدی با پروتئین ها ( آمید ) و چربی ها ( استر ) انجام می دهد که در نتیجه بافت های زنده (مانند پوست و گوشت ) را تجزیه می کند. اسید نیتریک غلیظ پوست انسان را به دلیل واکنش آن با کراتین زرد می کند . این لکه های زرد وقتی خنثی می شوند نارنجی می شوند. [49] اثرات سیستمیک بعید است، و این ماده یک سرطانزا یا جهشزا در نظر گرفته نمیشود. [50]
درمان استاندارد کمک های اولیه برای ریختن اسید روی پوست، مانند سایر عوامل خورنده، آبیاری با مقدار زیادی آب است. شستشو حداقل 10 تا 15 دقیقه ادامه می یابد تا بافت اطراف محل سوختگی اسیدی خنک شود و از آسیب ثانویه جلوگیری شود. لباس های آلوده بلافاصله برداشته می شوند و پوست زیر آن کاملا شسته می شود.
اسید نیتریک به عنوان یک عامل اکسید کننده قوی، می تواند به شدت با بسیاری از ترکیبات واکنش نشان دهد.
اسید نیتریک یکی از رایج ترین انواع اسید مورد استفاده در حملات اسیدی است . [51]