ایزوتوپ ها گونه های هسته ای متمایز (یا نوکلیدها ) از یک عنصر شیمیایی هستند . آنها دارای عدد اتمی یکسان (تعداد پروتون در هسته خود ) و موقعیت در جدول تناوبی هستند (و از این رو به عنصر شیمیایی یکسانی تعلق دارند)، اما تعداد نوکلئون های مختلف ( اعداد جرمی ) به دلیل تعداد نوترون های مختلف در هسته آنها متفاوت است. در حالی که تمام ایزوتوپ های یک عنصر مشخص دارای خواص شیمیایی مشابهی هستند، اما دارای جرم اتمی و خواص فیزیکی متفاوتی هستند . [1]
اصطلاح ایزوتوپ از ریشه یونانی isos (ἴσος «برابر») و topos (τόπος «مکان») به معنای «همان مکان» گرفته شده است. بنابراین، معنای پشت نام این است که ایزوتوپهای مختلف یک عنصر واحد موقعیت یکسانی را در جدول تناوبی اشغال میکنند . [2] توسط دکتر و نویسنده اسکاتلندی مارگارت تاد در پیشنهادی در سال 1913 به فردریک سودی شیمیدان بریتانیایی که این اصطلاح را رایج کرد، ابداع شد . [3]
تعداد پروتون های درون هسته اتم را عدد اتمی آن می نامند و برابر با تعداد الکترون های اتم خنثی (غیر یونیزه) است. هر عدد اتمی یک عنصر خاص را مشخص می کند، اما ایزوتوپ را مشخص نمی کند. یک اتم از یک عنصر معین ممکن است دامنه وسیعی در تعداد نوترون های خود داشته باشد . تعداد نوکلئونها (اعم از پروتون و نوترون) در هسته، عدد جرمی اتم است و هر ایزوتوپ از یک عنصر معین دارای عدد جرمی متفاوتی است.
برای مثال، کربن-12 ، کربن-13 و کربن-14 سه ایزوتوپ عنصر کربن با اعداد جرمی 12، 13 و 14 هستند. عدد اتمی کربن 6 است، یعنی هر اتم کربن دارای 6 پروتون است به طوری که اعداد نوترونی این ایزوتوپ ها به ترتیب 6، 7 و 8 است.
نوکلید گونه ای از اتم با تعداد مشخصی پروتون و نوترون در هسته است ، برای مثال کربن-13 با 6 پروتون و 7 نوترون. مفهوم نوکلید (اشاره به گونههای هستهای منفرد) بر ویژگیهای هستهای بر خواص شیمیایی تأکید میکند، در حالی که مفهوم ایزوتوپ (گروهبندی همه اتمهای هر عنصر) بر شیمیایی بر هستهای تأکید دارد. عدد نوترون تا حد زیادی بر خواص هسته ای تأثیر می گذارد، اما تأثیر آن بر خواص شیمیایی برای اکثر عناصر ناچیز است. حتی برای سبکترین عناصر، که نسبت عدد نوترون به عدد اتمی آنها بین ایزوتوپها بیشترین تغییر را دارد، معمولاً فقط یک اثر کوچک دارد، اگرچه در برخی شرایط مهم است (برای هیدروژن، سبکترین عنصر، اثر ایزوتوپ به اندازهای بزرگ است که روی زیستشناسی تأثیر بگذارد. به شدت). اصطلاح ایزوتوپ ها ( در اصل عناصر ایزوتوپی [4]، اکنون گاهی اوقات هسته های ایزوتوپی [5] ) به معنای مقایسه است (مانند مترادف ها یا ایزومرها ). به عنوان مثال، نوکلیدها12
6سی
،13
6سی
،14
6سی
ایزوتوپ هستند (نوکلئیدهایی با عدد اتمی یکسان اما اعداد جرمی متفاوت [6] )، اما40
18آر
،40
19ک
،40
20حدود
ایزوبارها هستند (نوکلئیدهایی با عدد جرمی یکسان [7] ). با این حال، ایزوتوپ اصطلاح قدیمیتری است و بنابراین بهتر از نوکلید شناخته میشود و هنوز هم گاهی اوقات در زمینههایی استفاده میشود که نوکلید ممکن است مناسبتر باشد، مانند فناوری هستهای و پزشکی هستهای .
یک ایزوتوپ و/یا نوکلید با نام عنصر خاص مشخص می شود (این عدد اتمی را نشان می دهد) و سپس یک خط فاصله و عدد جرمی (مانند هلیوم-3 ، هلیوم-4 ، کربن-12 ، کربن-14 ، اورانیوم-) مشخص می شود. 235 و اورانیوم 239 ). [8] هنگامی که از یک نماد شیمیایی استفاده می شود، به عنوان مثال "C" برای کربن، نماد استاندارد (اکنون به عنوان "نشان AZE" شناخته می شود زیرا A عدد جرمی ، Z عدد اتمی و E برای عنصر است ) برای نشان دادن عدد جرمی است. (تعداد نوکلئون ها) با یک رونوشت در سمت چپ بالای نماد شیمیایی و برای نشان دادن عدد اتمی با یک زیرنویس در سمت چپ پایین (مثلاً3
2او
،4
2او
،12
6سی
،14
6سی
،235
92U
، و239
92U
). [9] از آنجایی که عدد اتمی با نماد عنصر داده می شود، معمول است که فقط عدد جرمی را در بالانویس ذکر کنیم و زیرنویس عدد اتمی را کنار بگذاریم (مثلاً3
او
،4
او
،12
سی
،14
سی
،235
U
، و239
U
). برای مثال، حرف m (برای فراپایدار) بعد از عدد جرمی اضافه میشود تا یک ایزومر هستهای ، یک حالت هستهای متقابل یا با انرژی برانگیخته (برخلاف حالت پایه با کمترین انرژی )، نشان دهد.180 متر
73تا
( تانتالوم-180 متر ).
تلفظ رایج نماد AZE با نحوه نوشتن آن متفاوت است:4
2او
معمولاً به جای چهار-دو هلیوم به صورت هلیوم چهار تلفظ می شود و235
92U
به عنوان اورانیوم دو و سی و پنج (انگلیسی آمریکایی) یا اورانیوم-دو-سه-پنج (بریتانیایی) به جای اورانیوم 235-92.
برخی از ایزوتوپ ها/نوکلیدها رادیواکتیو هستند و بنابراین به آنها رادیو ایزوتوپ یا رادیونوکلئید می گویند ، در حالی که برخی دیگر هرگز به صورت رادیواکتیو تجزیه نشده اند و به عنوان ایزوتوپ های پایدار یا هسته های پایدار شناخته می شوند . به عنوان مثال،14
سی
شکل رادیواکتیو کربن است، در حالی که12
سی
و13
سی
ایزوتوپ های پایدار هستند. حدود 339 هسته طبیعی روی زمین وجود دارد، [10] که از این تعداد 286 هسته اولیه هستند ، به این معنی که آنها از زمان شکل گیری منظومه شمسی وجود داشته اند .
هسته های اولیه شامل 35 هسته با نیمه عمر بسیار طولانی (بیش از 100 میلیون سال) و 251 هسته هستند که به طور رسمی به عنوان " نوکلیدهای پایدار " در نظر گرفته می شوند، [10] زیرا مشاهده نشده است که تجزیه شوند. در بیشتر موارد، به دلایل واضح، اگر عنصری ایزوتوپ های پایدار داشته باشد، آن ایزوتوپ ها در فراوانی عنصری موجود در زمین و در منظومه شمسی غالب هستند. با این حال، در مورد سه عنصر ( تلوریم ، ایندیم و رنیم )، فراوانترین ایزوتوپ موجود در طبیعت در واقع یک (یا دو) ایزوتوپ رادیویی با عمر بسیار طولانی از عنصر است، علیرغم اینکه این عناصر دارای یک یا چند عنصر پایدار هستند. ایزوتوپ ها
تئوری پیشبینی میکند که بسیاری از هستههای به ظاهر «پایدار» رادیواکتیو هستند و نیمه عمر بسیار طولانی دارند (کاهش احتمال فروپاشی پروتون ، که همه هستهها را در نهایت ناپایدار میکند). برخی از نوکلیدهای پایدار در تئوری از نظر انرژی نسبت به سایر اشکال شناخته شده فروپاشی، مانند واپاشی آلفا یا فروپاشی مضاعف بتا، حساس هستند، اما هنوز هیچ محصول فروپاشی مشاهده نشده است، و بنابراین گفته میشود که این ایزوتوپها از نظر مشاهده پایدار هستند. نیمه عمر پیش بینی شده برای این هسته ها اغلب بسیار بیشتر از سن تخمینی جهان است، و در واقع، 31 رادیونوکلئید شناخته شده (به هسته اولیه مراجعه کنید ) با نیمه عمر طولانی تر از سن جهان وجود دارد.
با افزودن هستههای رادیواکتیو که بهطور مصنوعی ایجاد شدهاند، در حال حاضر 3339 هستهی شناخته شده وجود دارد . [11] اینها شامل 905 هسته هستند که یا پایدار هستند یا نیمه عمر آنها بیش از 60 دقیقه است. برای جزئیات بیشتر به لیست نوکلیدها مراجعه کنید .
وجود ایزوتوپ ها برای اولین بار در سال 1913 توسط رادیو شیمیدان فردریک سودی ، بر اساس مطالعات زنجیره های تجزیه رادیواکتیو که حدود 40 گونه مختلف را به عنوان عناصر رادیواکتیو (یعنی عناصر رادیواکتیو) بین اورانیوم و سرب نشان می داد ، پیشنهاد شد ، اگرچه جدول تناوبی فقط 11 مورد را مجاز می دانست. عناصر بین سرب و اورانیوم شامل [12] [13] [14]
چندین تلاش برای جداسازی شیمیایی این عناصر رادیویی جدید شکست خورده بود. [15] برای مثال، سودی در سال 1910 نشان داده بود که جداسازی مزوتوریوم (که بعداً 228 Ra بود )، رادیوم ( 226 Ra، طولانیترین ایزوتوپ) و توریم X ( 224 Ra) غیرممکن است. [16] تلاش برای قرار دادن عناصر رادیویی در جدول تناوبی باعث شد سودی و کازیمیرز فاجانها به طور مستقل قانون جابجایی رادیواکتیو خود را در سال 1913 پیشنهاد کنند، به این معنی که واپاشی آلفا عنصری را در دو نقطه سمت چپ در جدول تناوبی تولید می کند، در حالی که انتشار واپاشی بتا. یک عنصر را یک جا به سمت راست تولید کرد. [17] [18] [19] [20] سادی تشخیص داد که انتشار یک ذره آلفا و به دنبال آن دو ذره بتا منجر به تشکیل عنصری شد که از نظر شیمیایی مشابه عنصر اولیه بود، اما با جرم چهار واحد سبکتر و با خواص رادیواکتیو متفاوت. .
سودی پیشنهاد کرد که چندین نوع اتم (که از نظر خواص رادیواکتیو متفاوت هستند) می توانند یک مکان را در جدول اشغال کنند. [14] برای مثال، تجزیه آلفا اورانیوم-235 توریم-231 را تشکیل می دهد، در حالی که واپاشی بتا اکتینیم-230 توریم-230 را تشکیل می دهد. [15] اصطلاح "ایزوتوپ"، یونانی به معنای "در همان مکان"، [14] توسط مارگارت تاد ، پزشک اسکاتلندی و دوست خانوادگی، در طی مکالمه ای که در آن ایده های خود را برای او توضیح داد، به سودی پیشنهاد شد . [16] [21] [22] [23] [24] [25] او در سال 1921 جایزه نوبل شیمی را تا حدی برای کار خود در مورد ایزوتوپ ها دریافت کرد. [26]

در سال 1914 ریچاردز تغییراتی را بین وزن اتمی سرب از منابع معدنی مختلف یافت که به تغییرات در ترکیب ایزوتوپی به دلیل منشأهای مختلف رادیواکتیو نسبت داده می شد. [15] [26]
اولین شواهد برای ایزوتوپ های متعدد یک عنصر پایدار (غیر رادیواکتیو) توسط جی جی تامسون در سال 1912 به عنوان بخشی از کاوش او در ترکیب پرتوهای کانال (یون های مثبت) یافت شد. [27] تامسون جریانهای یونهای نئون را از طریق میدانهای مغناطیسی و الکتریکی موازی هدایت کرد، انحراف آنها را با قرار دادن یک صفحه عکاسی در مسیرشان اندازهگیری کرد و نسبت جرم به بار آنها را با استفاده از روشی محاسبه کرد که به روش سهمی تامسون معروف شد. هر جریان یک تکه درخشان بر روی صفحه در نقطه ای که برخورد می کند ایجاد می کند. تامسون دو تکه سهموی مجزا از نور را روی صفحه عکاسی مشاهده کرد (تصویر را ببینید)، که دو گونه از هستهها را با نسبت جرم به بار متفاوت پیشنهاد میکرد. او نوشت: «بنابراین، فکر میکنم، نمیتوان شک داشت که آنچه که نئون نامیده میشود یک گاز ساده نیست، بلکه مخلوطی از دو گاز است که وزن اتمی یکی حدود 20 و دیگری حدود 22 است. گاز سنگینتر همیشه بسیار کمنورتر از گاز سبکتر است، بنابراین احتمالاً گاز سنگینتر تنها درصد کمی از مخلوط را تشکیل میدهد. [28]
FW Aston متعاقباً با استفاده از طیفنگار جرمی چندین ایزوتوپ پایدار برای عناصر متعدد کشف کرد . در سال 1919 استون نئون را با وضوح کافی مورد مطالعه قرار داد تا نشان دهد که دو جرم ایزوتوپی بسیار نزدیک به اعداد صحیح 20 و 22 هستند و هیچ کدام برابر با جرم مولی (20.2) گاز نئون نیستند. این مثالی از قانون اعداد کامل استون برای جرم های ایزوتوپی است که بیان می کند که انحرافات بزرگ جرم مولی عنصری از اعداد صحیح در درجه اول به دلیل این واقعیت است که عنصر مخلوطی از ایزوتوپ ها است. استون به طور مشابه در سال 1920 نشان داد که جرم مولی کلر (35.45) میانگین وزنی جرم تقریباً یکپارچه برای دو ایزوتوپ 35 Cl و 37 Cl است. [29] [30]
پس از کشف نوترون توسط جیمز چادویک در سال 1932، [31] علت اصلی وجود ایزوتوپها مشخص شد، یعنی هستههای ایزوتوپهای مختلف برای یک عنصر معین، تعداد نوترونهای متفاوتی دارند، البته تعداد آنها یکسان است. از پروتون ها
یک اتم خنثی به اندازه پروتون ها الکترون دارد. بنابراین ایزوتوپهای مختلف یک عنصر معین، همگی دارای تعداد یکسانی الکترون هستند و ساختار الکترونیکی مشابهی دارند. از آنجایی که رفتار شیمیایی یک اتم تا حد زیادی توسط ساختار الکترونیکی آن تعیین می شود، ایزوتوپ های مختلف رفتار شیمیایی تقریباً یکسانی از خود نشان می دهند.
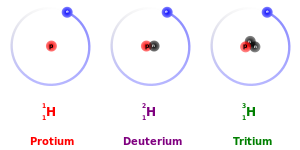
استثنای اصلی در این مورد، اثر ایزوتوپ جنبشی است : ایزوتوپهای سنگینتر به دلیل جرمهای بزرگتر، نسبت به ایزوتوپهای سبکتر همان عنصر، تمایل دارند تا حدودی کندتر واکنش نشان دهند. این بیشتر برای پروتیوم مشخص است (1
اچ
، دوتریوم (2
اچ
و تریتیوم (3
اچ
) زیرا جرم دوتریوم دو برابر پروتیوم و تریتیوم سه برابر جرم پروتیوم است. [32] این تفاوتهای جرمی نیز با تغییر مرکز ثقل ( جرم کاهشیافته ) سیستمهای اتمی، بر رفتار پیوندهای شیمیایی مربوطه تأثیر میگذارد. با این حال، برای عناصر سنگینتر، تفاوت جرم نسبی بین ایزوتوپها بسیار کمتر است، به طوری که اثرات اختلاف جرم در شیمی معمولاً ناچیز است. (عناصر سنگین همچنین دارای نوترون های نسبتاً بیشتری نسبت به عناصر سبک تر هستند، بنابراین نسبت جرم هسته ای به جرم الکترونیکی جمعی کمی بیشتر است.) همچنین یک اثر ایزوتوپ تعادلی وجود دارد .

به طور مشابه، دو مولکول که فقط در ایزوتوپهای اتمهایشان ( ایزوتوپولوگها ) متفاوت هستند، ساختارهای الکترونیکی یکسانی دارند و بنابراین خواص فیزیکی و شیمیایی تقریباً غیرقابل تشخیص هستند (دوتریوم و تریتیوم استثناهای اصلی هستند). حالت های ارتعاشی یک مولکول با شکل آن و جرم اتم های تشکیل دهنده آن تعیین می شود. بنابراین ایزوتوپولوگ های مختلف مجموعه های مختلفی از حالت های ارتعاشی دارند. از آنجایی که حالتهای ارتعاشی به مولکول اجازه میدهد فوتونهای انرژیهای متناظر را جذب کند، ایزوتوپولوژیکها خواص نوری متفاوتی در محدوده مادون قرمز دارند .
هستههای اتمی شامل پروتونها و نوترونهایی است که توسط نیروی قوی باقیمانده به هم متصل شدهاند . از آنجایی که پروتون ها دارای بار مثبت هستند، یکدیگر را دفع می کنند. نوترون ها که از نظر الکتریکی خنثی هستند، هسته را از دو طریق تثبیت می کنند. حضور همزمان آنها پروتون ها را اندکی از هم دور می کند و دافعه الکترواستاتیکی بین پروتون ها را کاهش می دهد و آنها نیروی هسته ای جذابی را بر روی یکدیگر و روی پروتون ها اعمال می کنند. به همین دلیل، یک یا چند نوترون برای اتصال دو یا چند پروتون به یک هسته ضروری است. با افزایش تعداد پروتونها، نسبت نوترونها به پروتونها نیز افزایش مییابد که برای اطمینان از یک هسته پایدار ضروری است (نمودار سمت راست را ببینید). برای مثال، اگرچه نسبت نوترون:پروتون از3
2او
1:2 است، نسبت نوترون به پروتون از238
92U
بزرگتر از 3:2 است. تعدادی از عناصر سبکتر دارای نوکلیدهای پایدار با نسبت 1:1 ( Z = N ) هستند. نوکلید40
20حدود
(کلسیم-40) از نظر مشاهداتی سنگین ترین هسته پایدار با تعداد نوترون و پروتون یکسان است. تمام هسته های پایدار سنگین تر از کلسیم 40 حاوی نوترون بیشتری نسبت به پروتون هستند.
از 80 عنصر دارای ایزوتوپ پایدار، بیشترین تعداد ایزوتوپ پایدار مشاهده شده برای هر عنصر ده عدد است (برای عنصر قلع ). هیچ عنصری نه یا هشت ایزوتوپ پایدار ندارد. پنج عنصر دارای هفت ایزوتوپ پایدار، هشت عنصر دارای شش ایزوتوپ پایدار، ده عنصر دارای پنج ایزوتوپ پایدار، نه عنصر دارای چهار ایزوتوپ پایدار، پنج عنصر دارای سه ایزوتوپ پایدار، 16 دارای دو ایزوتوپ پایدار (شمارش180 متر
73تا
به عنوان پایدار)، و 26 عنصر تنها یک ایزوتوپ پایدار دارند (از این میان، 19 عنصر به اصطلاح عناصر تک هستهای هستند که دارای یک ایزوتوپ پایدار اولیه هستند که بر وزن اتمی عنصر طبیعی با دقت بالا تسلط دارد و تثبیت میکند؛ 3 عنصر تک هستهای رادیواکتیو. نیز رخ دهد). [33] در مجموع، 251 هسته وجود دارد که تجزیه و تحلیل آنها مشاهده نشده است. برای 80 عنصری که یک یا چند ایزوتوپ پایدار دارند، میانگین تعداد ایزوتوپ های پایدار 251/80 ≈ 3.14 ایزوتوپ در هر عنصر است.
نسبت پروتون به نوترون تنها عامل موثر بر پایداری هسته ای نیست. همچنین به زوج بودن یا عجیب بودن عدد اتمی Z ، عدد نوترونی N و در نتیجه مجموع آنها، عدد جرمی A بستگی دارد . عجیب بودن هر دو Z و N تمایل به کاهش انرژی اتصال هسته ای دارد و باعث می شود هسته های فرد معمولاً پایدارتر شوند. این تفاوت قابل توجه انرژی اتصال هسته ای بین هسته های همسایه، به ویژه ایزوبارهای فرد A ، پیامدهای مهمی دارد: ایزوتوپ های ناپایدار با تعداد غیربهینه نوترون یا پروتون در اثر واپاشی بتا (از جمله انتشار پوزیترون )، جذب الکترون ، یا سایر واپاشی های کمتر رایج تجزیه می شوند. حالت هایی مانند شکافت خود به خود و فروپاشی خوشه ای .
بیشتر هسته های پایدار، زوج-پروتون-زوفر-نوترون هستند که در آن همه اعداد Z ، N و A زوج هستند. نوکلیدهای فرد- A پایدار (تقریباً به طور مساوی) به نوکلیدهای فرد-پروتون-زوتر-نوترون و زوج-پروتون-فرد نوترون تقسیم می شوند. نوکلیدهای فرد-پروتون-فرد-نوترون پایدار کمترین موارد را دارند.
146 هستههای زوج پروتون و نوترون (EE) حدود 58 درصد از تمام هستههای پایدار را تشکیل میدهند و همگی به دلیل جفت شدن دارای اسپین صفر هستند. همچنین 24 هسته اولیه با عمر طولانی حتی یکنواخت وجود دارد. در نتیجه، هر یک از 41 عنصر زوج از 2 تا 82 دارای حداقل یک ایزوتوپ پایدار است و بیشتر این عناصر دارای چندین ایزوتوپ اولیه هستند. نیمی از این عناصر زوج دارای شش یا بیشتر ایزوتوپ پایدار هستند. پایداری بسیار زیاد هلیوم 4 به دلیل جفت شدن دو پروتون و 2 نوترون از هر گونه هسته ای حاوی پنج (5
2او
،5
3لی
) یا هشت (8
4باشد
) نوکلئون هایی که به اندازه کافی وجود دارند تا به عنوان سکویی برای تجمع عناصر سنگین تر از طریق همجوشی هسته ای در ستارگان عمل کنند (به فرآیند آلفای سه گانه مراجعه کنید ).
فقط پنج هسته پایدار دارای تعداد فرد پروتون و تعداد فرد نوترون هستند. چهار هسته اول «فرد-فرد» در هستههای کم جرم اتفاق میافتند، که تغییر پروتون به نوترون یا برعکس، منجر به نسبت پروتون به نوترون بسیار کجرو میشود .2
1اچ
،6
3لی
،10
5ب
، و14
7ن
; چرخش 1، 1، 3، 1). تنها هسته دیگر کاملاً «پایدار» فرد و فرد،180 متر
73تا
(چرخش 9)، گمان می رود که نادرترین هسته از 251 هسته پایدار باشد، و تنها ایزومر هسته ای اولیه است که علیرغم تلاش های آزمایشی هنوز مشاهده نشده است که فروپاشی کند. [34]
بسیاری از رادیونوکلئیدهای عجیب و غریب (مانند حالت پایه تانتالیوم-180) با نیمه عمر نسبتاً کوتاه شناخته شده اند. معمولاً، آنها به ایزوبارهای یکنواخت نزدیک خود که دارای پروتون های جفت و نوترون های جفتی هستند، بتا واپاشی می کنند. از 9 هسته اولیه عجیب و غریب (پنج پایدار و چهار رادیواکتیو با نیمه عمر طولانی)، فقط14
7ن
رایج ترین ایزوتوپ یک عنصر مشترک است. این مورد به این دلیل است که بخشی از چرخه CNO است . نوکلیدها6
3لی
و10
5ب
ایزوتوپ های اقلیتی از عناصر هستند که خود در مقایسه با سایر عناصر سبک کمیاب هستند، در حالی که شش ایزوتوپ دیگر تنها درصد کمی از فراوانی طبیعی عناصر آنها را تشکیل می دهند.
53 هسته پایدار دارای تعداد پروتون زوج و تعداد فرد نوترون هستند. آنها در مقایسه با ایزوتوپ های زوج که حدوداً 3 برابر تعدادشان هستند، در اقلیت هستند. از میان 41 عنصر زوج Z که دارای یک هسته پایدار هستند، تنها دو عنصر (آرگون و سریم) هیچ هسته پایدار زوج و فرد ندارند. یک عنصر (قلع) دارای سه عنصر است. 24 عنصر وجود دارد که دارای یک هسته زوج و فرد و 13 عنصر دارای دو هسته زوج و فرد هستند. از 35 رادیونوکلئید اولیه، چهار هسته زوج و فرد وجود دارد (جدول سمت راست را ببینید)، از جمله هسته شکافت پذیر . 235
92U
. به دلیل تعداد نوترونهای فرد، هستههای زوج و فرد به دلیل انرژی ناشی از اثرات جفت شدن نوترون، سطح مقطع جذب نوترون بزرگی دارند . این هستههای نوترون فرد-پروتون زوج پایدار معمولاً به دلیل فراوانی در طبیعت غیرمعمول هستند، عموماً به این دلیل که برای تشکیل و ورود به فراوانی اولیه، باید از گرفتن نوترونها فرار کرده و ایزوتوپهای زوج و زوج پایدار دیگر را در طول هر دو s- به وجود آورند. فرآیند و فرآیند r جذب نوترون، در طول سنتز هسته در ستارگان . فقط به همین دلیل195
78Pt
و9
4باشد
به طور طبیعی فراوان ترین ایزوتوپ های عنصر خود هستند.
48 نوکلیدهای فرد - پروتون - زوج - نوترون پایدار که توسط نوترونهای جفت آنها تثبیت شدهاند، بیشتر ایزوتوپهای پایدار عناصر با اعداد فرد را تشکیل میدهند. تعداد بسیار کمی از نوکلیدهای فرد-پروتون-فرد-نوترون شامل بقیه هستند. 41 عنصر با اعداد فرد با Z = 1 تا 81 وجود دارد که 39 عنصر دارای ایزوتوپ های پایدار ( تکنسیوم ) هستند.
43تی سی
) و پرومتیم (
61بعد از ظهر
) هیچ ایزوتوپ پایدار ندارند). از این 39 عنصر Z فرد ، 30 عنصر (شامل هیدروژن-1 که 0 نوترون آن زوج است ) دارای یک ایزوتوپ زوج و فرد پایدار و 9 عنصر: کلر (
17Cl
، پتاسیم (
19ک
، مس (
29مس
، گالیم (
31گا
، برم (
35برادر
، نقره ای (
47Ag
، آنتیموان (
51Sb
ایریدیوم (
77Ir
و تالیم (
81Tl
، هر کدام دو ایزوتوپ پایدار زوج و فرد دارند. در مجموع 30 + 2(9) = 48 ایزوتوپ زوج و فرد پایدار است.
همچنین پنج ایزوتوپ زوج و فرد رادیواکتیو با عمر طولانی اولیه وجود دارد.87
37Rb
،115
49در
،187
75Re
،151
63Eu
، و209
83بی
. دو مورد آخر اخیراً مشخص شد که پوسیدگی دارند و نیمه عمر آنها بیشتر از 10 18 سال است.
اکتینیدهای با عدد نوترون فرد معمولاً شکافت پذیر هستند (با نوترون های حرارتی )، در حالی که آنهایی که عدد نوترون زوج دارند معمولاً شکافت پذیر نیستند، اگرچه با نوترون های سریع قابل شکافت هستند . همه هستههای فرد و فرد از نظر مشاهدهی پایدار دارای اسپین عدد صحیح غیرصفر هستند. این به این دلیل است که نوترون جفت نشده و پروتون جفت نشده نیروی هستهای بیشتری نسبت به یکدیگر دارند، در صورتی که اسپینهایشان در یک راستا باشند (با تولید یک اسپین کل حداقل 1 واحد)، به جای ضد تراز. برای ساده ترین مورد این رفتار هسته ای دوتریوم را ببینید .
فقط195
78Pt
،9
4باشد
، و14
7ن
دارای عدد نوترون فرد هستند و به طور طبیعی فراوان ترین ایزوتوپ عنصر خود هستند.
عناصر یا از یک نوکلید ( عناصر تک هسته ای ) یا از بیش از یک ایزوتوپ طبیعی تشکیل شده اند. ایزوتوپ های ناپایدار (رادیواکتیو) یا اولیه هستند یا پسا اولیه. ایزوتوپهای اولیه محصولی از نوکلئوسنتز ستارهای یا نوع دیگری از سنتز هستهای مانند پوسته شدن پرتوهای کیهانی بودند ، و تا به امروز باقی ماندهاند، زیرا سرعت فروپاشی آنها بسیار کند است (مانند اورانیوم-238 و پتاسیم-40 ). ایزوتوپهای پسا اولیه توسط بمباران پرتوهای کیهانی بهعنوان هستههای کیهانی (مثلاً تریتیوم ، کربن-14 )، یا با فروپاشی یک ایزوتوپ اولیه رادیواکتیو به یک دختر هستهای پرتوزا (مانند اورانیوم به رادیوم ) ایجاد شدند. چند ایزوتوپ به طور طبیعی بهعنوان هستههای هستهزا ، توسط برخی واکنشهای هستهای طبیعی دیگر ، مانند زمانی که نوترونهای حاصل از شکافت هستهای طبیعی توسط اتم دیگری جذب میشوند، سنتز میشوند.
همانطور که در بالا توضیح داده شد، تنها 80 عنصر دارای ایزوتوپ پایدار هستند و 26 مورد از آنها فقط یک ایزوتوپ پایدار دارند. بنابراین، حدود دو سوم عناصر پایدار به طور طبیعی در روی زمین در چندین ایزوتوپ پایدار وجود دارند که بیشترین تعداد ایزوتوپ های پایدار برای یک عنصر ده ایزوتوپ است، برای قلع .
50Sn
). حدود 94 عنصر به طور طبیعی روی زمین یافت می شود (تا شامل پلوتونیوم )، اگرچه برخی از آنها فقط در مقادیر بسیار کوچک مانند پلوتونیوم 244 شناسایی می شوند . دانشمندان تخمین می زنند که عناصری که به طور طبیعی روی زمین وجود دارند (برخی فقط به عنوان ایزوتوپ های رادیویی) در مجموع 339 ایزوتوپ ( نوکلید ) وجود دارند. [35] تنها 251 مورد از این هستههای طبیعی پایدار هستند، به این معنا که تا کنون هرگز مشاهده نشدهاند که فروپاشی کنند. 35 هسته اولیه دیگر (در مجموع 286 هسته اولیه) رادیواکتیو با نیمه عمر شناخته شده هستند، اما نیمه عمر آنها بیش از 100 میلیون سال است که به آنها اجازه می دهد از ابتدای منظومه شمسی وجود داشته باشند. برای جزئیات بیشتر به لیست نوکلیدها مراجعه کنید .
تمام هسته های پایدار شناخته شده به طور طبیعی روی زمین وجود دارند. سایر هسته های طبیعی رادیواکتیو هستند اما به دلیل نیمه عمر نسبتاً طولانی آنها یا به دلیل سایر روش های تولید طبیعی مداوم در زمین رخ می دهند. اینها شامل هستههای کیهانزایی فوقالذکر ، هستههای هستهزا ، و هر هسته پرتوزایی که در اثر فروپاشی مداوم یک هسته رادیواکتیو اولیه، مانند رادون و رادیوم از اورانیوم، تشکیل شدهاند، میشوند.
حدود 3000 هسته رادیواکتیو اضافی که در طبیعت یافت نمی شود در راکتورهای هسته ای و در شتاب دهنده های ذرات ایجاد شده است. بسیاری از هستههای کوتاهمدت که به طور طبیعی روی زمین یافت نمیشوند نیز با تجزیه و تحلیل طیفسنجی مشاهده شدهاند که به طور طبیعی در ستارگان یا ابرنواخترها ایجاد میشوند . به عنوان مثال آلومینیوم-26 است که به طور طبیعی در زمین یافت نمی شود اما در مقیاس نجومی به وفور یافت می شود.
جرمهای اتمی جدولبندی شده عناصر، میانگینهایی هستند که وجود ایزوتوپهای متعدد با جرمهای متفاوت را نشان میدهند. قبل از کشف ایزوتوپ ها، مقادیر غیرصحیح جرم اتمی که به طور تجربی تعیین شده بودند، دانشمندان را گیج می کرد. به عنوان مثال، یک نمونه کلر حاوی 75.8 درصد کلر 35 و 24.2 درصد کلر 37 است که میانگین جرم اتمی آن 35.5 واحد جرم اتمی است .
طبق نظریه عمومی پذیرفته شده کیهان شناسی ، تنها ایزوتوپ های هیدروژن و هلیوم، آثاری از برخی ایزوتوپ های لیتیوم و بریلیم، و شاید مقداری بور، در انفجار بزرگ ایجاد شدند ، در حالی که تمام هسته های دیگر بعداً در ستارگان و ابرنواخترها و در فعل و انفعالات بین ذرات پرانرژی مانند پرتوهای کیهانی و هسته های تولید شده قبلی. ( برای جزئیات فرآیندهای مختلفی که تصور می شود مسئول تولید ایزوتوپ هستند، به هسته سنتز مراجعه کنید .) فراوانی مربوط به ایزوتوپ ها روی زمین ناشی از مقادیر تشکیل شده توسط این فرآیندها، گسترش آنها در کهکشان، و نرخ فروپاشی ایزوتوپ هایی است که ناپایدار هستند. پس از ادغام اولیه منظومه شمسی ، ایزوتوپ ها بر اساس جرم دوباره توزیع شدند و ترکیب ایزوتوپی عناصر از سیاره ای به سیاره دیگر کمی متفاوت است. این گاهی اوقات ردیابی منشا شهاب سنگ ها را ممکن می کند .
جرم اتمی ( mr ) یک ایزوتوپ (نوکلید) عمدتاً با عدد جرمی آن (یعنی تعداد نوکلئونهای موجود در هسته آن) تعیین میشود. اصلاحات جزئی به دلیل انرژی اتصال هسته (نگاه کنید به نقص جرم )، تفاوت جزئی در جرم بین پروتون و نوترون، و جرم الکترون های مرتبط با اتم است، دومی به این دلیل که نسبت الکترون به نوکلئون در بین ایزوتوپ ها متفاوت است.
عدد جرمی یک کمیت بدون بعد است . از سوی دیگر، جرم اتمی با استفاده از واحد جرم اتمی بر اساس جرم اتم کربن 12 اندازه گیری می شود. با نمادهای "u" (برای واحد جرم اتمی یکپارچه) یا "Da" (برای دالتون ) نشان داده می شود .
جرم اتمی ایزوتوپ های طبیعی یک عنصر، وزن اتمی استاندارد عنصر را تعیین می کند. هنگامی که عنصر حاوی ایزوتوپ های N باشد ، عبارت زیر برای میانگین جرم اتمی اعمال می شود :
که در آن m 1 , m 2 , ..., m N جرم اتمی هر ایزوتوپ مجزا هستند و x 1 , ..., x N فراوانی نسبی این ایزوتوپ ها هستند.
چندین برنامه کاربردی وجود دارد که بر روی خواص ایزوتوپ های مختلف یک عنصر خاص سرمایه گذاری می کند. جداسازی ایزوتوپ ها یک چالش تکنولوژیکی مهم است، به ویژه با عناصر سنگین مانند اورانیوم یا پلوتونیوم. عناصر سبک تر مانند لیتیوم، کربن، نیتروژن و اکسیژن معمولاً با انتشار گاز ترکیبات خود مانند CO و NO از هم جدا می شوند. جداسازی هیدروژن و دوتریوم غیرعادی است زیرا بر اساس خواص شیمیایی است تا فیزیکی، به عنوان مثال در فرآیند سولفید Girdler . ایزوتوپهای اورانیوم به صورت عمده توسط انتشار گاز، سانتریفیوژ گاز، جداسازی یونیزاسیون لیزری و (در پروژه منهتن ) توسط نوعی طیفسنجی جرمی تولید جدا شدهاند .
بنابراین، عناصر شیمیایی یکسان - یا ایزوتوپ ها، همانطور که برای اولین بار در این نامه به طبیعت نام بردم، زیرا آنها همان مکان را در جدول تناوبی اشغال می کنند ...
ص 208: تا سال 1913 ما از عبارت "عناصر رادیویی از نظر شیمیایی غیرقابل تفکیک" استفاده می کردیم و در آن زمان کلمه ایزوتوپ در یک بحث در اتاق نشیمن با دکتر مارگارت تاد در خانه پدر همسر سودی، سر
جورج پیشنهاد شد.
بیلبی