در بیوشیمی ، ایزوآنزیم ها (همچنین به عنوان ایزوآنزیم ها یا به طور کلی به عنوان اشکال متعدد آنزیم شناخته می شوند ) آنزیم هایی هستند که در توالی اسید آمینه متفاوت هستند اما واکنش شیمیایی یکسانی را کاتالیز می کنند. ایزوآنزیم ها معمولاً پارامترهای جنبشی متفاوتی دارند (مثلاً مقادیر مختلف KM ) ، یا به طور متفاوتی تنظیم می شوند. آنها به تنظیم دقیق متابولیسم اجازه می دهند تا نیازهای خاص یک بافت خاص یا مرحله رشد را برآورده کند.
در بسیاری از موارد، ایزوآنزیم ها توسط ژن های همولوگ که در طول زمان از هم جدا شده اند کدگذاری می شوند. به بیان دقیق، آنزیمهایی با توالیهای اسید آمینه مختلف که واکنش یکسانی را کاتالیز میکنند، اگر توسط ژنهای مختلف کدگذاری شوند، ایزوآنزیم هستند، یا اگر توسط آللهای مختلف یک ژن کدگذاری شوند، آلوزیم هستند . این دو اصطلاح اغلب به جای هم استفاده می شوند.
ایزوآنزیم ها برای اولین بار توسط RL Hunter و Clement Markert (1957) توصیف شدند که آنها را به عنوان انواع مختلفی از یک آنزیم با عملکردهای یکسان و موجود در یک فرد تعریف کردند . [1] این تعریف شامل (1) گونههای آنزیمی است که محصول ژنهای مختلف هستند و بنابراین مکانهای مختلفی را نشان میدهند (که به عنوان ایزوآنزیم توصیف میشوند ) و (2) آنزیمهایی که محصول آللهای مختلف یک ژن هستند (به عنوان آلوزیم توصیف میشوند ). [2]
ایزوآنزیم ها معمولاً نتیجه تکرار ژن هستند ، اما می توانند از پلی پلوئیدیزه شدن یا هیبریداسیون اسید نوکلئیک نیز ایجاد شوند . در طول زمان تکامل، اگر عملکرد نوع جدید با نوع اصلی یکسان باقی بماند ، احتمالاً یکی از آنها با تجمع جهشها از بین میرود و منجر به ایجاد یک شبه ژن میشود . با این حال، اگر جهشها فوراً از عملکرد آنزیم جلوگیری نکنند، بلکه درعوض عملکرد یا الگوی بیان آن را تغییر دهند ، آنگاه این دو نوع ممکن است هر دو مورد علاقه انتخاب طبیعی قرار گیرند و برای عملکردهای مختلف تخصصی شوند. [3] به عنوان مثال، آنها ممکن است در مراحل مختلف رشد یا در بافت های مختلف بیان شوند. [4]
آلوزیمها ممکن است از جهشهای نقطهای یا از رویدادهای درج-حذف ( indel ) که روی توالی کدکننده ژن تأثیر میگذارند، ایجاد شوند. مانند هر جهش جدید دیگری، سه چیز ممکن است برای یک آلوزیم جدید رخ دهد:
نمونه ای از ایزوآنزیم گلوکوکیناز است ، گونه ای از هگزوکیناز که توسط گلوکز 6-فسفات مهار نمی شود . ویژگیهای تنظیمی متفاوت و تمایل کمتر آن به گلوکز (در مقایسه با سایر هگزوکینازها)، به آن اجازه میدهد تا عملکردهای مختلفی را در سلولهای اندامهای خاص انجام دهد، مانند کنترل ترشح انسولین توسط سلولهای بتا پانکراس یا شروع سنتز گلیکوژن توسط سلولهای کبدی . . هر دوی این فرآیندها فقط باید زمانی اتفاق بیفتند که گلوکز فراوان باشد.
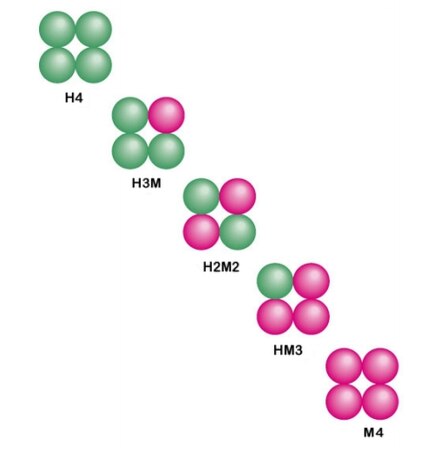

1.) آنزیم لاکتات دهیدروژناز یک تترامر ساخته شده از دو زیر واحد مختلف، فرم H و فرم M است. اینها بسته به بافت در ترکیبات مختلف ترکیب می شوند: [7]
2.) ایزوآنزیم های کراتین فسفوکیناز: [7] کراتین کیناز (CK) یا کراتین فسفوکیناز (CPK) تبدیل فسفو کراتین به کراتین را کاتالیز می کند.
CPK در 3 ایزوآنزیم وجود دارد. هر ایزوآنزیم دایمری از 2 زیرواحد M (عضله)، B (مغز) یا هر دو است [7]
3.) ایزوآنزیم های آلکالین فسفاتاز: [7] شش ایزوآنزیم شناسایی شده است. آنزیم یک مونومر است، ایزوآنزیم ها به دلیل تفاوت در محتوای کربوهیدرات (باقی مانده اسید سیالیک) است. مهم ترین ایزوآنزیم های ALP عبارتند از α1 -ALP ، α2 - ALP حساس به حرارت، α2 - ALP پایدار در برابر حرارت، pre-β ALP و γ-ALP. افزایش ALP حساس به گرما α2 نشان دهنده هپاتیت است در حالی که pre-β ALP نشان دهنده بیماری های استخوانی است.
ایزوآنزیم ها (و آلوزیم ها) انواعی از همان آنزیم هستند. مگر اینکه آنها از نظر خواص بیوشیمیایی یکسان باشند، به عنوان مثال سوبستراها و سینتیک آنزیم آنها، ممکن است با یک سنجش بیوشیمیایی قابل تشخیص باشند . با این حال، چنین تفاوت هایی معمولاً ظریف هستند، به ویژه بین آلوزیم هایی که اغلب انواع خنثی هستند . این ظرافت قابل انتظار است، زیرا دو آنزیم که به طور قابل توجهی در عملکردشان متفاوت هستند، بعید است که به عنوان ایزوآنزیم شناسایی شده باشند .
در حالی که ایزوآنزیم ها ممکن است از نظر عملکرد تقریباً یکسان باشند، ممکن است از راه های دیگر متفاوت باشند. به طور خاص، جایگزینهای اسید آمینه که بار الکتریکی آنزیم را تغییر میدهند، توسط الکتروفورز ژل شناسایی میشوند و این اساس استفاده از ایزوآنزیمها به عنوان نشانگرهای مولکولی را تشکیل میدهد . برای شناسایی ایزوآنزیمها، از آسیاب کردن بافت حیوانی یا گیاهی با بافر استخراج، عصاره پروتئین خام ساخته میشود و اجزای عصاره بر حسب بار آن توسط الکتروفورز ژل جدا میشوند. از لحاظ تاریخی، این کار معمولاً با استفاده از ژل های ساخته شده از نشاسته سیب زمینی انجام می شود ، اما ژل های آکریل آمید وضوح بهتری ارائه می دهند.
تمام پروتئین های بافت در ژل وجود دارد، بنابراین آنزیم های فردی باید با استفاده از روشی که عملکرد آنها را به یک واکنش رنگ آمیزی مرتبط می کند، شناسایی شوند. برای مثال، تشخیص میتواند بر اساس رسوب موضعی رنگهای شاخص محلول مانند نمکهای تترازولیوم باشد که با کاهش آنها توسط کوفاکتورهایی مانند NAD یا NADP که در مناطق فعالیت آنزیم ایجاد میشوند، نامحلول میشوند. این روش سنجش مستلزم آن است که آنزیمها پس از جداسازی همچنان عملکردی داشته باشند ( الکتروفورز ژل بومی )، و بزرگترین چالش را برای استفاده از ایزوآنزیمها به عنوان یک تکنیک آزمایشگاهی فراهم میکند.
ایزوآنزیم ها در سینتیک متفاوت هستند ( آنها مقادیر KM و V max متفاوتی دارند ).
ژنتیک جمعیت اساساً مطالعه علل و اثرات تغییرات ژنتیکی در داخل و بین جمعیت ها است و در گذشته ایزوآنزیم ها از جمله پرکاربردترین نشانگرهای مولکولی برای این منظور بوده اند. اگرچه اکنون آنها تا حد زیادی با رویکردهای مبتنی بر DNA آموزنده تر جایگزین شده اند (مانند توالی یابی مستقیم DNA ، پلی مورفیسم های تک نوکلئوتیدی و ریزماهواره ها )، آنها هنوز جزو سریع ترین و ارزان ترین سیستم های نشانگر برای توسعه هستند و (از سال 2005 [به روز رسانی]) به عنوان یک سیستم عالی باقی می مانند. انتخاب برای پروژه هایی که فقط نیاز به شناسایی سطوح پایین تنوع ژنتیکی دارند، به عنوان مثال، کمی سازی سیستم های جفت گیری .