اتم ها ذرات اساسی عناصر شیمیایی هستند . یک اتم از هسته ای از پروتون ها و به طور کلی نوترون ها تشکیل شده است که توسط گروهی از الکترون ها به صورت الکترومغناطیسی محصور شده است . عناصر شیمیایی با تعداد پروتون هایی که در اتم هایشان هستند از یکدیگر متمایز می شوند. به عنوان مثال، هر اتمی که حاوی 11 پروتون باشد سدیم است و هر اتمی که حاوی 29 پروتون باشد مس است . اتم هایی با تعداد پروتون یکسان اما تعداد نوترون متفاوت، ایزوتوپ های یک عنصر نامیده می شوند.
اتم ها بسیار کوچک هستند، معمولاً حدود 100 پیکومتر عرض دارند. عرض یک موی انسان حدود یک میلیون اتم کربن است. اتمها کوچکتر از کوتاهترین طول موج نور مرئی هستند، به این معنی که انسان نمیتواند اتمها را با میکروسکوپهای معمولی ببیند. آنها آنقدر کوچک هستند که پیش بینی دقیق رفتار آنها با استفاده از فیزیک کلاسیک به دلیل اثرات کوانتومی امکان پذیر نیست .
بیش از 99.94 درصد از جرم اتم در هسته است. پروتون ها دارای بار الکتریکی مثبت و نوترون ها بدون بار هستند، بنابراین هسته دارای بار مثبت است. الکترون ها دارای بار منفی هستند و این بار مخالف همان چیزی است که آنها را به هسته متصل می کند. اگر تعداد پروتونها و الکترونها به طور معمول برابر باشند، آنگاه اتم در کل از نظر الکتریکی خنثی است. اگر یک اتم دارای الکترون های بیشتری نسبت به پروتون ها باشد، بار کلی آن منفی است و یون منفی (یا آنیون) نامیده می شود. برعکس، اگر پروتون آن بیشتر از الکترون باشد، بار مثبت دارد و یون مثبت (یا کاتیون) نامیده می شود.
الکترون های یک اتم توسط نیروی الکترومغناطیسی به سمت پروتون های هسته اتم جذب می شوند . پروتون ها و نوترون های هسته توسط نیروی هسته ای به یکدیگر جذب می شوند . این نیرو معمولاً قویتر از نیروی الکترومغناطیسی است که پروتونهای دارای بار مثبت را از یکدیگر دفع میکند. تحت شرایط خاص، نیروی الکترومغناطیسی دفع کننده قوی تر از نیروی هسته ای می شود. در این حالت هسته شکافته شده و عناصر مختلفی از خود به جای می گذارد . این یک شکل از فروپاشی هسته ای است .
اتم ها می توانند با پیوندهای شیمیایی به یک یا چند اتم دیگر بچسبند و ترکیبات شیمیایی مانند مولکول ها یا کریستال ها را تشکیل دهند . توانایی اتم ها برای اتصال و جدا شدن از یکدیگر مسئول بیشتر تغییرات فیزیکی مشاهده شده در طبیعت است. شیمی علمی است که این تغییرات را مطالعه می کند.
این ایده اولیه که ماده از ذرات ریز تقسیم ناپذیر تشکیل شده است، یک ایده قدیمی است که در بسیاری از فرهنگ های باستانی ظاهر شده است. کلمه اتم از کلمه یونانی باستان atomos گرفته شده است ، [a] که به معنای "قابل برش" است. اما این ایده باستانی به جای استدلال علمی مبتنی بر استدلال فلسفی بود. نظریه اتمی مدرن مبتنی بر این مفاهیم قدیمی نیست. [1] [2] در اوایل قرن 19، دانشمند جان دالتون شواهدی پیدا کرد که ماده واقعاً از واحدهای مجزا تشکیل شده است، و بنابراین کلمه اتم را برای آن واحدها به کار برد. [3]

در اوایل دهه 1800، جان دالتون دادههای تجربی جمعآوریشده توسط او و دیگر دانشمندان را گردآوری کرد و الگویی را کشف کرد که اکنون به نام « قانون نسبتهای چندگانه » شناخته میشود. او متوجه شد که در هر گروهی از ترکیبات شیمیایی که همگی حاوی دو عنصر شیمیایی خاص هستند، مقدار عنصر A در هر اندازه عنصر B در این ترکیبات با نسبتهای اعداد کوچک کوچک متفاوت است. این الگو نشان میدهد که هر عنصر با عناصر دیگر در مضرب یک واحد وزن ترکیب میشود و هر عنصر دارای یک واحد وزن منحصر به فرد است. دالتون تصمیم گرفت این واحدها را «اتم» بنامد. [4]
به عنوان مثال، دو نوع اکسید قلع وجود دارد : یکی پودر خاکستری است که 88.1٪ قلع و 11.9٪ اکسیژن است، و دیگری پودر سفید است که 78.7٪ قلع و 21.3٪ اکسیژن است. با تنظیم این ارقام، در پودر خاکستری به ازای هر 100 گرم قلع حدود 13.5 گرم اکسیژن و در پودر سفید به ازای هر 100 گرم قلع حدود 27 گرم اکسیژن وجود دارد. 13.5 و 27 نسبت 1:2 را تشکیل می دهند. دالتون نتیجه گرفت که در اکسید خاکستری به ازای هر اتم قلع یک اتم اکسیژن و در اکسید سفید به ازای هر اتم قلع دو اتم اکسیژن ( SnO و SnO 2 ) وجود دارد . [5] [6]
دالتون همچنین اکسیدهای آهن را تجزیه و تحلیل کرد . یک نوع اکسید آهن وجود دارد که یک پودر سیاه است که 78.1٪ آهن و 21.9٪ اکسیژن است. و اکسید آهن دیگری وجود دارد که یک پودر قرمز است که 70.4 درصد آهن و 29.6 درصد اکسیژن است. با تنظیم این ارقام، در پودر سیاه به ازای هر 100 گرم آهن حدود 28 گرم اکسیژن و در پودر قرمز به ازای هر 100 گرم آهن حدود 42 گرم اکسیژن وجود دارد. 28 و 42 نسبت 2:3 را تشکیل می دهند. دالتون نتیجه گرفت که در این اکسیدها، به ازای هر دو اتم آهن، به ترتیب دو یا سه اتم اکسیژن وجود دارد ( Fe 2 O 2 و Fe 2 O 3 ). [ب] [7] [8]
به عنوان مثال نهایی: اکسید نیتروژن 63.3 درصد نیتروژن و 36.7 درصد اکسیژن، اکسید نیتریک 44.05 درصد نیتروژن و 55.95 درصد اکسیژن و دی اکسید نیتروژن 29.5 درصد نیتروژن و 70.5 درصد اکسیژن است. با تنظیم این ارقام، در اکسید نیتروژن به ازای هر 140 گرم نیتروژن 80 گرم اکسیژن، در اکسید نیتریک به ازای هر 140 گرم نیتروژن حدود 160 گرم اکسیژن و در دی اکسید نیتروژن به ازای هر 140 گرم، 320 گرم اکسیژن وجود دارد. گرم نیتروژن 80، 160 و 320 نسبت 1:2:4 را تشکیل می دهند. فرمول های مربوط به این اکسیدها N 2 O , NO و NO 2 هستند . [9] [10]
در سال 1897، جی جی تامسون کشف کرد که پرتوهای کاتدی شکلی از نور نیستند، بلکه از ذرات با بار منفی ساخته شدهاند، زیرا میتوانند توسط میدانهای الکتریکی و مغناطیسی منحرف شوند. [11] او اندازه گیری کرد که این ذرات حداقل هزار بار سبک تر از هیدروژن (سبک ترین اتم) هستند. [12] او این ذرات جدید را ذرات نامید ، اما بعداً آنها به الکترون تغییر نام دادند زیرا این ذرات حامل الکتریسیته هستند. [13] تامسون همچنین نشان داد که الکترون ها با ذرات منتشر شده توسط مواد فوتوالکتریک و رادیواکتیو یکسان هستند. [14] تامسون توضیح داد که جریان الکتریکی عبور الکترونها از یک اتم به اتم دیگر است و وقتی جریانی وجود نداشت، الکترونها خود را در اتمها قرار میدهند. این به نوبه خود به این معنی بود که اتم ها آن طور که دانشمندان فکر می کردند تقسیم ناپذیر نیستند. اتم از الکترون هایی تشکیل شده بود که بار منفی آنها توسط منبعی از بار مثبت متعادل می شد تا یک اتم خنثی الکتریکی ایجاد شود. تامسون توضیح داد که یون ها باید اتم هایی باشند که دارای الکترون اضافی یا کمبود باشند. [15]
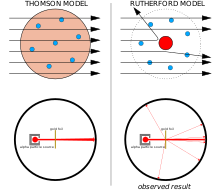
الکترونهای اتم منطقاً باید با مقدار متناسبی از بار مثبت متعادل میشدند، اما تامسون نمیدانست این بار مثبت از کجا آمده است، بنابراین او به طور آزمایشی پیشنهاد کرد که این بار مثبت در همه جای اتم وجود دارد، اتم در اتم است. شکل یک کره به دنبال این، او تصور کرد که موازنه نیروهای الکترواستاتیک الکترون ها را در سراسر کره به شیوه ای کم و بیش یکنواخت توزیع می کند. [16] مدل تامسون عموماً به عنوان مدل پودینگ آلو شناخته می شود ، اگرچه نه تامسون و نه همکارانش از این قیاس استفاده نکردند. [17] مدل تامسون ناقص بود و قادر به پیشبینی سایر ویژگیهای عناصر مانند طیفهای نشر و ظرفیتها نبود . به زودی با کشف هسته اتم منسوخ شد .
بین سالهای 1908 و 1913، ارنست رادرفورد و همکارانش ، هانس گایگر و ارنست مارسدن، مجموعهای از آزمایشها را انجام دادند که در آن فویلهای نازک فلز را با پرتوی از ذرات آلفا بمباران کردند . آنها این کار را برای اندازه گیری الگوهای پراکندگی ذرات آلفا انجام دادند. آنها تعداد کمی از ذرات آلفا را مشاهده کردند که با زوایای بیشتر از 90 درجه منحرف می شدند. با توجه به مدل تامسون اتم که بارهای آن برای تولید میدان الکتریکی به اندازه کافی قوی بسیار پراکنده بودند، این نباید ممکن می شد. انحرافات باید همه ناچیز باشد. رادرفورد پیشنهاد کرد که بار مثبت اتم همراه با بیشتر جرم اتم در یک هسته کوچک در مرکز اتم متمرکز شده است. فقط چنین غلظت شدیدی از بار مثبت، که توسط جرم زیاد آن لنگر انداخته و از بار منفی جدا شده است، می تواند میدان الکتریکی ایجاد کند که می تواند ذرات آلفا را به شدت منحرف کند. [18]

یک مشکل در مکانیک کلاسیک این است که یک ذره باردار شتابدهنده تابش الکترومغناطیسی میتابد و باعث میشود که ذره انرژی جنبشی را از دست بدهد. حرکت دایرهای شتاب محسوب میشود، به این معنی که الکترونی که به دور یک بار مرکزی میچرخد، با کاهش سرعت باید به سمت هسته پایین بیاید. در سال 1913، فیزیکدان نیلز بور مدل جدیدی را پیشنهاد کرد که در آن فرض میشد الکترونهای یک اتم به دور هسته میچرخند، اما فقط میتوانستند این کار را در مجموعهای محدود از مدارها انجام دهند، و میتوانستند بین این مدارها فقط در تغییرات گسسته انرژی پرش کنند. جذب یا تابش یک فوتون [19] این کوانتیزاسیون برای توضیح اینکه چرا مدارهای الکترونها پایدار هستند و چرا عناصر تابش الکترومغناطیسی را در طیفهای مجزا جذب و ساطع میکنند، استفاده شد. [20] مدل بور فقط میتوانست طیف گسیل هیدروژن را پیشبینی کند، نه اتمهایی با بیش از یک الکترون.
در سال 1815، ویلیام پروت مشاهده کرد که وزن اتمی بسیاری از عناصر مضرب وزن اتمی هیدروژن است، که در واقع برای همه آنها اگر ایزوتوپ ها را در نظر بگیریم صادق است. در سال 1898، جی جی تامسون دریافت که بار مثبت یک یون هیدروژن برابر با بار منفی یک الکترون است و این ذرات در آن زمان کوچکترین ذرات باردار شناخته شده بودند. [21] تامسون بعداً دریافت که بار مثبت در یک اتم مضرب مثبت بار منفی یک الکترون است. [22] در سال 1913، هنری موزلی کشف کرد که فرکانس انتشار پرتو ایکس از یک اتم برانگیخته تابعی ریاضی از عدد اتمی آن و بار هستهای هیدروژن است. در سال 1917 رادرفورد گاز نیتروژن را با ذرات آلفا بمباران کرد و یون های هیدروژن را که از گاز ساطع می شود را شناسایی کرد و به این نتیجه رسید که آنها از برخورد ذرات آلفا و شکافتن اتم های نیتروژن تولید می شوند. [23]
این مشاهدات رادرفورد را به این نتیجه رساند که هسته هیدروژن یک ذره منفرد با بار مثبت برابر با بار منفی الکترون است. [24] او این ذره را در سال 1920 " پروتن " نامید . [25] عدد اتمی یک عنصر ، که به عنوان موقعیت عنصر در جدول تناوبی تعریف شده است ، همچنین تعداد پروتون هایی است که در هسته خود دارد. وزن اتمی هر عنصر از عدد پروتون آن بیشتر است، بنابراین رادرفورد فرض کرد که وزن اضافی توسط ذرات ناشناخته بدون بار الکتریکی و جرمی برابر با پروتون حمل می شود.
در سال 1928، والتر بوته مشاهده کرد که بریلیوم هنگام بمباران با ذرات آلفا، تابش بسیار نافذ و خنثی الکتریکی از خود ساطع می کند. بعدها کشف شد که این تشعشعات می تواند اتم های هیدروژن را از موم پارافین خارج کند . در ابتدا تصور می شد که این تابش گامای پرانرژی است ، زیرا تابش گاما تأثیر مشابهی بر الکترون های فلزات دارد، اما جیمز چادویک دریافت که اثر یونیزاسیون آنقدر قوی است که به دلیل تابش الکترومغناطیسی باشد، تا زمانی که انرژی و تکانه وجود داشته باشد. در تعامل حفظ شدند. در سال 1932، چادویک عناصر مختلفی مانند هیدروژن و نیتروژن را در معرض "تابش بریلیوم" مرموز قرار داد و با اندازه گیری انرژی ذرات باردار در حال پس زدن، نتیجه گرفت که تابش در واقع از ذرات خنثی الکتریکی تشکیل شده است که نمی توانند بدون جرم باشند. مانند پرتو گاما، اما در عوض باید جرمی مشابه جرم پروتون داشته باشند. چادویک اکنون این ذرات را نوترون های رادرفورد می داند. [26]

در سال 1925، ورنر هایزنبرگ اولین فرمول ریاضی ثابت مکانیک کوانتومی ( مکانیک ماتریس ) را منتشر کرد. [27] یک سال قبل، لویی دو بروگلی پیشنهاد کرده بود که همه ذرات تا حدی مانند امواج رفتار می کنند، [28] و در سال 1926 اروین شرودینگر از این ایده برای توسعه معادله شرودینگر استفاده کرد، که الکترون ها را به عنوان شکل موج های سه بعدی به جای نقاط توصیف می کند. در فضا [29] نتیجه استفاده از شکل موج برای توصیف ذرات این است که از نظر ریاضی بدست آوردن مقادیر دقیق برای موقعیت و تکانه یک ذره در یک نقطه زمانی معین غیرممکن است. این به عنوان اصل عدم قطعیت شناخته شد ، که توسط ورنر هایزنبرگ در سال 1927 فرموله شد. [27] در این مفهوم، برای دقت معین در اندازهگیری یک موقعیت، تنها میتوان محدودهای از مقادیر احتمالی برای تکانه به دست آورد، و بالعکس. [30] بنابراین، مدل سیارهای اتم به نفع مدلی که مناطق مداری اتمی را در اطراف هسته که در آن الکترون معین به احتمال زیاد یافت میشود، توصیف میکرد، کنار گذاشته شد. [31] [32] این مدل قادر به توضیح مشاهدات رفتار اتمی بود که مدلهای قبلی نمیتوانستند، مانند الگوهای ساختاری و طیفی خاص اتمهای بزرگتر از هیدروژن.
اگرچه کلمه اتم در اصل به ذره ای اشاره می کند که نمی توان آن را به ذرات کوچکتر تقسیم کرد، اما در کاربرد علمی مدرن اتم از ذرات مختلف زیر اتمی تشکیل شده است . ذرات تشکیل دهنده یک اتم الکترون ، پروتون و نوترون هستند .
الکترون با چهار مرتبه قدر در بین این ذرات کم جرم ترین است9.11 × 10-31 کیلوگرم ، با بار الکتریکی منفی و اندازه ای که برای اندازه گیری با استفاده از تکنیک های موجود بسیار کوچک است . [33] تا زمان کشف جرم نوترینو ، سبکترین ذره با جرم سکون مثبت اندازهگیری شده بود. در شرایط معمولی، الکترون ها به وسیله جاذبه ایجاد شده از بارهای الکتریکی مخالف به هسته با بار مثبت متصل می شوند. اگر یک اتم دارای تعداد الکترون های بیشتر یا کمتر از عدد اتمی خود باشد، در کل به ترتیب دارای بار منفی یا مثبت می شود. اتم باردار را یون می نامند . الکترون ها از اواخر قرن نوزدهم شناخته شده اند، بیشتر به لطف جی جی تامسون . برای جزئیات بیشتر به تاریخچه فیزیک زیراتمی مراجعه کنید .
پروتون ها دارای بار مثبت و جرم هستند1.6726 × 10-27 کیلوگرم . تعداد پروتون های یک اتم را عدد اتمی آن می گویند . ارنست رادرفورد (1919) مشاهده کرد که نیتروژن تحت بمباران ذره آلفا، آنچه را که به نظر می رسد هسته های هیدروژن است، بیرون می زند. در سال 1920 او پذیرفته بود که هسته هیدروژن یک ذره مجزا در اتم است و آن را پروتون نامید .
نوترون ها بار الکتریکی ندارند و جرم دارند1.6749 × 10-27 کیلوگرم . [34] [35] نوترونها سنگینترین از سه ذره تشکیلدهنده هستند، اما جرم آنها را میتوان با انرژی اتصال هستهای کاهش داد . نوترونها و پروتونها (که در مجموع به عنوان نوکلئون شناخته میشوند ) دارای ابعاد قابل مقایسه هستند.2.5 × 10-15 متر - اگرچه "سطح" این ذرات کاملاً مشخص نیست. [36] نوترون در سال 1932 توسط فیزیکدان انگلیسی جیمز چادویک کشف شد .
در مدل استاندارد فیزیک، الکترونها واقعاً ذرات بنیادی بدون ساختار داخلی هستند، در حالی که پروتونها و نوترونها ذرات ترکیبی هستند که از ذرات بنیادی به نام کوارک تشکیل شدهاند . دو نوع کوارک در اتم ها وجود دارد که هر کدام دارای بار الکتریکی کسری هستند. پروتون ها از دو کوارک بالا (هر کدام با بار + ) تشکیل شده اند2/3 ) و یک کوارک پایین (با بار − ).1/3) . نوترون ها از یک کوارک بالا و دو کوارک پایین تشکیل شده اند. این تمایز به دلیل تفاوت جرم و بار بین دو ذره است. [37] [38]
کوارک ها توسط برهمکنش قوی (یا نیروی قوی) که توسط گلوئون ها واسطه می شود، کنار هم نگه داشته می شوند . پروتونها و نوترونها به نوبهی خود توسط نیروی هستهای در هسته به یکدیگر متصل میشوند ، که باقیماندهای از نیروی قوی است که تا حدودی ویژگیهای برد متفاوتی دارد (برای اطلاعات بیشتر به مقاله در مورد نیروی هستهای مراجعه کنید). گلوئون عضوی از خانواده بوزونهای گیج است که ذرات بنیادی هستند که میانجی نیروهای فیزیکی هستند. [37] [38]

همه پروتون ها و نوترون های متصل در یک اتم یک هسته اتمی کوچک را تشکیل می دهند و در مجموع به آنها نوکلئون می گویند . شعاع یک هسته تقریباً برابر با فمتومتر است که تعداد کل نوکلئونها در آن است. [39] این بسیار کوچکتر از شعاع اتم است که در حد 105 fm است . نوکلئون ها توسط یک پتانسیل جذاب با برد کوتاه به نام نیروی قوی باقیمانده به یکدیگر متصل می شوند . در فواصل کمتر از 2.5 fm این نیرو بسیار قوی تر از نیروی الکترواستاتیکی است که باعث می شود پروتون های دارای بار مثبت یکدیگر را دفع کنند. [40]
اتم های یک عنصر دارای تعداد پروتون یکسانی هستند که به آن عدد اتمی می گویند . در درون یک عنصر، تعداد نوترونها ممکن است متفاوت باشد که ایزوتوپ آن عنصر را تعیین میکند. تعداد کل پروتون ها و نوترون ها هسته را تعیین می کند . تعداد نوترونها نسبت به پروتونها، پایداری هسته را تعیین میکند و ایزوتوپهای خاصی در معرض واپاشی رادیواکتیو قرار میگیرند . [41]
پروتون، الکترون و نوترون به عنوان فرمیون طبقه بندی می شوند . فرمیون ها از اصل طرد پائولی پیروی می کنند که فرمیون های یکسان مانند چندین پروتون را از اشغال یک حالت کوانتومی به طور همزمان منع می کند. بنابراین، هر پروتون در هسته باید یک حالت کوانتومی متفاوت از همه پروتونهای دیگر داشته باشد، و همین امر در مورد همه نوترونهای هسته و همه الکترونهای ابر الکترونی صدق میکند. [42]
هستهای که تعداد پروتونهای متفاوتی نسبت به نوترونها دارد، میتواند به طور بالقوه از طریق واپاشی رادیواکتیو که باعث میشود تعداد پروتونها و نوترونها به هم نزدیکتر شود، به حالت انرژی پایینتری سقوط کند. در نتیجه، اتمهایی با تعداد پروتونها و نوترونها در برابر فروپاشی پایدارتر هستند، اما با افزایش عدد اتمی، دفع متقابل پروتونها به نسبت فزایندهای از نوترونها برای حفظ پایداری هسته نیاز دارد. [42]
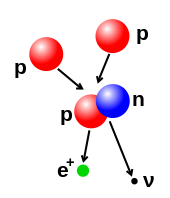
تعداد پروتونها و نوترونها در هسته اتم را میتوان تغییر داد، اگرچه این به دلیل نیروی قوی میتواند به انرژیهای بسیار بالایی نیاز داشته باشد. همجوشی هستهای زمانی اتفاق میافتد که چندین ذره اتمی به هم میپیوندند و هسته سنگینتری را تشکیل میدهند، مثلاً از طریق برخورد پرانرژی دو هسته. برای مثال، در هستهی خورشید، پروتونها به انرژیهای 3 تا 10 کو نیاز دارند تا بر دافعه متقابل خود - سد کولن - غلبه کنند و در یک هسته با هم ترکیب شوند. [43] شکافت هسته ای فرآیند مخالف است و باعث می شود یک هسته به دو هسته کوچکتر تقسیم شود - معمولاً از طریق واپاشی رادیواکتیو. هسته همچنین می تواند از طریق بمباران توسط ذرات زیراتمی یا فوتون های پرانرژی اصلاح شود. اگر این باعث تغییر تعداد پروتون های یک هسته شود، اتم به یک عنصر شیمیایی متفاوت تبدیل می شود. [44] [45]
اگر جرم هسته متعاقب یک واکنش همجوشی کمتر از مجموع جرم ذرات جداگانه باشد، اختلاف بین این دو مقدار می تواند به عنوان یک نوع انرژی قابل استفاده (مانند پرتو گاما یا انرژی جنبشی) منتشر شود. از یک ذره بتا )، همانطور که توسط فرمول هم ارزی جرم-انرژی آلبرت انیشتین ، e=mc 2 توضیح داده شده است ، که در آن m کاهش جرم و c سرعت نور است . این کسری بخشی از انرژی اتصال هسته جدید است و از دست دادن غیرقابل بازیافت انرژی است که باعث می شود ذرات ذوب شده در حالتی با هم باقی بمانند که نیاز به جدا شدن این انرژی دارد. [46]
همجوشی دو هستهای که هستههای بزرگتر با اعداد اتمی کمتر از آهن و نیکل ایجاد میکنند - تعداد نوکلئونهای کل حدود 60 - معمولاً یک فرآیند گرمازا است که انرژی بیشتری از آنچه برای جمع کردن آنها لازم است آزاد میکند. [47] این فرآیند آزادسازی انرژی است که همجوشی هسته ای در ستارگان را به واکنشی خودپایدار تبدیل می کند. برای هسته های سنگین تر، انرژی اتصال در هر نوکلئون شروع به کاهش می کند. این بدان معناست که فرآیند همجوشی که هستهای با عدد اتمی بالاتر از حدود 26 و عدد جرمی بالاتر از حدود 60 تولید میکند، یک فرآیند گرماگیر است . بنابراین، هستههای پرجرمتر نمیتوانند تحت یک واکنش همجوشی تولید انرژی قرار بگیرند که بتواند تعادل هیدرواستاتیکی یک ستاره را حفظ کند. [42]

الکترون های یک اتم توسط نیروی الکترومغناطیسی به سمت پروتون های هسته جذب می شوند . این نیرو، الکترونها را درون یک چاه پتانسیل الکترواستاتیکی که هسته کوچکتر را احاطه کرده است، متصل میکند، به این معنی که یک منبع خارجی انرژی برای فرار الکترون مورد نیاز است. هر چه الکترون به هسته نزدیکتر باشد، نیروی جاذبه بیشتر است. از این رو الکترون هایی که در نزدیکی مرکز چاه پتانسیل بسته می شوند، برای فرار به انرژی بیشتری نسبت به الکترون هایی که در جدایی های بیشتر هستند، نیاز دارند.
الکترونها مانند سایر ذرات دارای خواص ذره و موج هستند . ابر الکترونی ناحیه ای در داخل چاه پتانسیل است که در آن هر الکترون نوعی موج ایستاده سه بعدی را تشکیل می دهد - شکل موجی که نسبت به هسته حرکت نمی کند. این رفتار توسط یک اوربیتال اتمی تعریف می شود ، یک تابع ریاضی که احتمال اینکه یک الکترون به نظر می رسد در یک مکان خاص در هنگام اندازه گیری موقعیت آن قرار دارد، مشخص می شود. [48] تنها مجموعهای مجزا (یا کوانتیزهشده) از این اوربیتالها در اطراف هسته وجود دارد، زیرا سایر الگوهای موجی ممکن به سرعت به شکل پایدارتری تجزیه میشوند. [49] اوربیتال ها می توانند یک یا چند ساختار حلقه یا گره داشته باشند و از نظر اندازه، شکل و جهت با یکدیگر متفاوت باشند. [50]

هر اوربیتال اتمی مربوط به سطح انرژی خاصی از الکترون است. الکترون می تواند با جذب یک فوتون با انرژی کافی برای تقویت آن به حالت کوانتومی جدید، حالت خود را به سطح انرژی بالاتر تغییر دهد. به همین ترتیب، از طریق گسیل خود به خود ، یک الکترون در حالت انرژی بالاتر می تواند به حالت انرژی پایین تر سقوط کند در حالی که انرژی اضافی را به صورت فوتون تابش می کند. این مقادیر مشخصه انرژی، که با تفاوت در انرژی های حالت های کوانتومی تعریف می شوند، مسئول خطوط طیفی اتمی هستند . [49]
مقدار انرژی لازم برای حذف یا اضافه کردن یک الکترون - انرژی اتصال الکترون - بسیار کمتر از انرژی اتصال نوکلئون ها است . به عنوان مثال، برای جدا کردن یک الکترون حالت پایه از یک اتم هیدروژن تنها به 13.6 eV نیاز دارد، در مقایسه با 2.23 میلیون eV برای شکافتن یک هسته دوتریوم . [52] اگر اتم ها دارای تعداد مساوی پروتون و الکترون باشند، از نظر الکتریکی خنثی هستند . اتم هایی که دارای کمبود یا مازاد الکترون هستند یون نامیده می شوند . الکترون هایی که دورترین فاصله از هسته را دارند ممکن است به سایر اتم های نزدیک منتقل شوند یا بین اتم ها به اشتراک گذاشته شوند. با این مکانیسم، اتم ها می توانند به مولکول ها و انواع دیگر ترکیبات شیمیایی مانند بلورهای شبکه یونی و کووالانسی پیوند بخورند . [53]
طبق تعریف، هر دو اتم با تعداد پروتون یکسان در هسته خود به یک عنصر شیمیایی تعلق دارند . اتم هایی با تعداد پروتون مساوی اما تعداد نوترون متفاوت ، ایزوتوپ های متفاوت یک عنصر هستند. به عنوان مثال، تمام اتم های هیدروژن دقیقاً یک پروتون را می پذیرند، اما ایزوتوپ ها بدون نوترون ( هیدروژن-1 ، تا حد زیادی رایج ترین شکل، [54] که پروتیوم نیز نامیده می شود)، یک نوترون ( دوتریوم )، دو نوترون ( تریتیوم ) و بیشتر وجود دارند . از دو نوترون عناصر شناخته شده مجموعه ای از اعداد اتمی را تشکیل می دهند، از عنصر تک پروتونی هیدروژن تا عنصر 118 پروتونی اوگانسون . [55] همه ایزوتوپ های شناخته شده عناصر با اعداد اتمی بیشتر از 82 رادیواکتیو هستند، اگرچه رادیواکتیویته عنصر 83 ( بیسموت ) آنقدر ناچیز است که عملاً ناچیز است. [56] [57]
حدود 339 هسته به طور طبیعی بر روی زمین وجود دارد ، [58] که 251 (حدود 74٪) از بین رفتن مشاهده نشده است، و به عنوان " ایزوتوپ های پایدار " نامیده می شود. تنها 90 هسته از نظر تئوری پایدار هستند ، در حالی که 161 هسته دیگر (که مجموع آنها را به 251 می رساند) مشاهده نشده است که تجزیه شوند، حتی اگر در تئوری این امر از نظر انرژی ممکن است. اینها همچنین به طور رسمی به عنوان "پایدار" طبقه بندی می شوند. 35 هسته رادیواکتیو دیگر نیمه عمری بیش از 100 میلیون سال دارند و به اندازه ای طولانی هستند که از زمان تولد منظومه شمسی وجود داشته اند . این مجموعه 286 هسته ای به عنوان هسته اولیه شناخته می شود . در نهایت، ۵۳ هستهی کوتاهمدت اضافی بهطور طبیعی بهعنوان فرآوردههای فرزند فروپاشی هسته اولیه (مانند رادیوم از اورانیوم )، یا بهعنوان محصولات فرآیندهای انرژی طبیعی روی زمین، مانند بمباران پرتوهای کیهانی (مثلاً کربن) شناخته شدهاند. -14). [59] [یادداشت 1]
برای 80 عنصر شیمیایی، حداقل یک ایزوتوپ پایدار وجود دارد. به عنوان یک قاعده، فقط تعداد انگشت شماری ایزوتوپ پایدار برای هر یک از این عناصر وجود دارد که میانگین آن 3.1 ایزوتوپ پایدار در هر عنصر است. بیست و شش « عنصر تک ایزوتوپی » تنها یک ایزوتوپ پایدار دارند، در حالی که بیشترین تعداد ایزوتوپ پایدار مشاهده شده برای هر عنصر، ده ایزوتوپ برای عنصر قلع است . عناصر 43 ، 61 و همه عناصر با شماره 83 یا بالاتر هیچ ایزوتوپ پایداری ندارند. [60] : 1-12
پایداری ایزوتوپها تحت تأثیر نسبت پروتونها به نوترونها و همچنین وجود «اعداد جادویی» نوترونها یا پروتونهایی است که پوستههای کوانتومی بسته و پر شده را نشان میدهند. این پوسته های کوانتومی با مجموعه ای از سطوح انرژی در مدل پوسته هسته مطابقت دارند. پوسته های پر شده، مانند پوسته پر از 50 پروتون برای قلع، پایداری غیرعادی را به هسته می بخشد. از 251 هسته پایدار شناخته شده، تنها چهار عدد دارای تعداد فرد پروتون و تعداد فرد نوترون هستند: هیدروژن-2 ( دوتریوم )، لیتیوم-6 ، بور-10 و نیتروژن-14 . ( تانتالوم-180 متر عجیب و غریب و از نظر مشاهده پایدار است، اما پیش بینی می شود که با نیمه عمر بسیار طولانی تجزیه می شود.) همچنین، تنها چهار هسته رادیواکتیو عجیب و غریب که به طور طبیعی وجود دارند، نیمه عمر بیش از یک میلیارد سال دارند: پتاسیم- 40 ، وانادیوم-50 ، لانتانیم-138 ، و لوتیتیم-176 . بیشتر هستههای فرد و فرد نسبت به واپاشی بتا بسیار ناپایدار هستند ، زیرا فرآوردههای فروپاشی زوج و زوج هستند و بنابراین به دلیل اثرات جفت شدن هستهای قویتر هستند . [61]
اکثریت بزرگ جرم یک اتم از پروتون ها و نوترون های تشکیل دهنده آن می آید. تعداد کل این ذرات (به نام "نوکلئون") در یک اتم معین، عدد جرمی نامیده می شود . این یک عدد صحیح مثبت و بدون بعد (به جای داشتن بعد جرم) است، زیرا یک شمارش را بیان می کند. نمونه ای از استفاده از عدد جرمی "کربن-12" است که دارای 12 نوکلئون (شش پروتون و شش نوترون) است.
جرم واقعی یک اتم در حالت سکون اغلب بر حسب دالتون (Da) بیان می شود که واحد جرم اتمی یکپارچه (u) نیز نامیده می شود. این واحد به عنوان دوازدهم جرم یک اتم خنثی آزاد کربن 12 تعریف می شود که تقریباً برابر است با1.66 × 10-27 کیلوگرم . [62] هیدروژن-1 (سبک ترین ایزوتوپ هیدروژن که همچنین هسته ای با کمترین جرم است) دارای وزن اتمی 1.007825 Da است. [63] مقدار این عدد جرم اتمی نامیده می شود . جرم اتمی یک اتم تقریباً برابر است (در 1%) با عدد جرمی آن ضربدر واحد جرم اتمی (مثلاً جرم نیتروژن-14 تقریباً 14 Da است)، اما این عدد دقیقاً یک عدد صحیح نخواهد بود به جز ( طبق تعریف) در مورد کربن 12. [64] سنگین ترین اتم پایدار سرب-208 است، [56] با جرم6521 207.976 دا . [65]
از آنجایی که حتی سنگین ترین اتم ها برای کار مستقیم خیلی سبک هستند، شیمیدان ها در عوض از واحد مول استفاده می کنند . یک مول از اتم های هر عنصر همیشه تعداد اتم های یکسانی دارد (حدود6.022 × 10 23 ). این عدد طوری انتخاب شد که اگر جرم اتمی یک عنصر 1 u باشد، جرم یک مول از اتم های آن عنصر نزدیک به یک گرم باشد. به دلیل تعریف واحد جرم اتمی یکپارچه ، هر اتم کربن 12 دارای جرم اتمی دقیقاً 12 Da است و بنابراین یک مول اتم کربن 12 دقیقاً 0.012 کیلوگرم وزن دارد. [62]
اتم ها فاقد یک مرز بیرونی کاملاً مشخص هستند، بنابراین ابعاد آنها معمولاً بر حسب شعاع اتمی توصیف می شود . این اندازه گیری فاصله ای است که ابر الکترونی از هسته تا آن امتداد دارد. [66] این فرض را بر این میگذارد که اتم یک شکل کروی دارد که فقط برای اتمهای موجود در خلاء یا فضای آزاد رعایت میشود. شعاع اتمی ممکن است از فواصل بین دو هسته به دست آید که این دو اتم در یک پیوند شیمیایی به هم متصل شوند . شعاع با موقعیت یک اتم در نمودار اتمی، نوع پیوند شیمیایی، تعداد اتمهای همسایه ( عدد هماهنگی ) و خاصیت مکانیکی کوانتومی به نام اسپین تغییر میکند . [67] در جدول تناوبی عناصر، اندازه اتم هنگام حرکت به پایین ستونها افزایش مییابد، اما هنگام حرکت در ردیفها (از چپ به راست) کاهش مییابد. [68] در نتیجه، کوچکترین اتم هلیم با شعاع 32 pm است ، در حالی که یکی از بزرگترین اتم ها سزیم در 225 pm است. [69]
هنگامی که در معرض نیروهای خارجی، مانند میدان های الکتریکی ، شکل اتم ممکن است از تقارن کروی منحرف شود . همانطور که با ملاحظات نظری گروهی نشان داده شده است، تغییر شکل به بزرگی میدان و نوع مداری الکترونهای لایه بیرونی بستگی دارد . انحرافات کروی ممکن است به عنوان مثال در کریستال ها ، جایی که میدان های کریستالی-الکتریکی بزرگ ممکن است در سایت های شبکه با تقارن کم رخ دهند، ایجاد شود . [70] [71] تغییر شکلهای بیضوی قابل توجهی برای یونهای گوگرد [72] و یونهای کالکوژن [73] در ترکیبات نوع پیریت نشان داده شده است .
ابعاد اتمی هزاران بار کوچکتر از طول موج نور (400 تا 700 نانومتر ) است، بنابراین نمی توان آنها را با استفاده از میکروسکوپ نوری مشاهده کرد ، اگرچه اتم های جداگانه را می توان با استفاده از میکروسکوپ تونل زنی روبشی مشاهده کرد . برای تجسم ریز بودن اتم، در نظر بگیرید که عرض یک موی معمولی انسان حدود 1 میلیون اتم کربن است. [74] یک قطره آب حاوی حدود 2 سیستیلیون (2 × 10 21 ) اتم های اکسیژن و دو برابر تعداد اتم های هیدروژن. [75] الماس تک قیراط با جرم2 × 10-4 کیلوگرم حاوی حدود 10 سکتیلیون (1022 ) اتم کربن است . [نکته 2] اگر یک سیب به اندازه زمین بزرگنمایی شود، اتمهای موجود در سیب تقریباً به اندازه سیب اصلی خواهند بود. [76]

هر عنصر دارای یک یا چند ایزوتوپ است که دارای هستههای ناپایدار هستند که در معرض واپاشی رادیواکتیو هستند و باعث میشوند هسته ذرات یا تشعشعات الکترومغناطیسی ساطع کند. رادیواکتیویته زمانی رخ می دهد که شعاع یک هسته در مقایسه با شعاع نیروی قوی، که فقط در فواصل حدود 1 fm عمل می کند، بزرگ باشد. [77]
رایج ترین اشکال تجزیه رادیواکتیو عبارتند از: [78] [79]
سایر انواع نادرتر فروپاشی رادیواکتیو شامل بیرون راندن نوترون ها یا پروتون ها یا خوشه های نوکلئون از یک هسته یا بیش از یک ذره بتا است . یک آنالوگ گسیل گاما که به هستههای برانگیخته اجازه میدهد به روشی متفاوت انرژی خود را از دست بدهند، تبدیل داخلی است - فرآیندی که الکترونهایی با سرعت بالا تولید میکند که پرتوهای بتا نیستند و به دنبال آن فوتونهایی با انرژی بالا تولید میکند که پرتو گاما نیستند. چند هسته بزرگ به دو یا چند قطعه باردار با جرمهای مختلف به اضافه چندین نوترون منفجر میشوند، در یک فروپاشی به نام شکافت هستهای خود به خودی .
هر ایزوتوپ رادیواکتیو یک دوره زمانی واپاشی مشخص دارد - نیمه عمر - که با مقدار زمان لازم برای تجزیه نیمی از نمونه تعیین می شود. این یک فرآیند واپاشی نمایی است که به طور پیوسته نسبت ایزوتوپ باقی مانده را تا 50 درصد در هر نیمه عمر کاهش می دهد. بنابراین پس از گذشت دو نیمه عمر، تنها 25 درصد ایزوتوپ موجود است و غیره. [77]
ذرات بنیادی دارای خاصیت مکانیکی کوانتومی ذاتی هستند که به عنوان اسپین شناخته می شود . این مشابه با تکانه زاویه ای جسمی است که به دور مرکز جرم خود می چرخد ، اگرچه به طور دقیق اعتقاد بر این است که این ذرات نقطه مانند هستند و نمی توان گفت که در حال چرخش هستند. اسپین در واحدهای ثابت پلانک کاهش یافته (ħ) اندازهگیری میشود که الکترونها ، پروتونها و نوترونها همگی دارای اسپین 1⁄2 ç یا «اسپین -1⁄2 » هستند . در یک اتم، الکترونهایی که در اطراف هسته حرکت میکنند ، علاوه بر اسپین، دارای تکانه زاویهای مداری هستند ، در حالی که خود هسته به دلیل اسپین هستهایاش دارای تکانه زاویهای است. [80]
میدان مغناطیسی تولید شده توسط یک اتم - گشتاور مغناطیسی آن - توسط این اشکال مختلف تکانه زاویه ای تعیین می شود، درست همانطور که یک جسم باردار دوار به طور کلاسیک یک میدان مغناطیسی تولید می کند، اما بیشترین سهم از اسپین الکترون حاصل می شود. به دلیل ماهیت الکترونها برای اطاعت از اصل طرد پائولی ، که در آن هیچ دو الکترونی در یک حالت کوانتومی یافت نمیشوند ، الکترونهای مقید با یکدیگر جفت میشوند، به طوری که یک عضو از هر جفت در حالت اسپین بالا و دیگری در برعکس، حالت چرخش به پایین. بنابراین این اسپینها یکدیگر را خنثی میکنند و گشتاور دوقطبی مغناطیسی کل را در برخی اتمها با تعداد زوج الکترون به صفر میرسانند. [81]
در عناصر فرومغناطیسی مانند آهن، کبالت و نیکل، تعداد فرد الکترون منجر به یک الکترون جفت نشده و یک گشتاور مغناطیسی کلی می شود. اوربیتالهای اتمهای همسایه با هم همپوشانی دارند و وقتی اسپینهای الکترونهای جفتنشده با یکدیگر همسو میشوند، حالت انرژی پایینتری به دست میآید، فرآیندی خود به خودی که به عنوان برهمکنش تبادلی شناخته میشود . هنگامی که گشتاورهای مغناطیسی اتم های فرومغناطیسی در یک ردیف قرار می گیرند، ماده می تواند یک میدان ماکروسکوپی قابل اندازه گیری ایجاد کند. مواد پارامغناطیس دارای اتم هایی با گشتاورهای مغناطیسی هستند که وقتی میدان مغناطیسی وجود ندارد، در جهت های تصادفی صف می کشند، اما گشتاورهای مغناطیسی تک تک اتم ها در حضور میدان در یک ردیف قرار می گیرند. [81] [82]
هسته یک اتم وقتی دارای اعداد زوج نوترون و پروتون باشد، اسپین نخواهد داشت، اما برای سایر موارد اعداد فرد، هسته ممکن است دارای اسپین باشد. معمولاً هستههای دارای اسپین به دلیل تعادل حرارتی در جهات تصادفی قرار میگیرند ، اما برای عناصر خاصی (مانند زنون-129 ) میتوان بخش قابلتوجهی از حالتهای اسپین هستهای را قطبی کرد به طوری که آنها در یک جهت در یک راستا قرار گیرند. هیپرپولاریزاسیون نامیده می شود . این کاربردهای مهمی در تصویربرداری رزونانس مغناطیسی دارد . [83] [84]
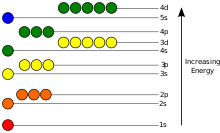
انرژی پتانسیل یک الکترون در یک اتم نسبت به زمانی که فاصله از هسته تا بی نهایت می رود منفی است . وابستگی آن به موقعیت الکترون به کمترین مقدار در داخل هسته می رسد ، تقریباً نسبت معکوس با فاصله. در مدل مکانیکی کوانتومی، یک الکترون محدود میتواند تنها مجموعهای از حالتها را در مرکز هسته اشغال کند و هر حالت مربوط به یک سطح انرژی خاص است . برای توضیح نظری معادله شرودینگر مستقل از زمان را ببینید . سطح انرژی را می توان با مقدار انرژی مورد نیاز برای جدا کردن الکترون از اتم اندازه گیری کرد و معمولاً بر حسب واحد الکترون ولت (eV) داده می شود. پایینترین حالت انرژی یک الکترون محدود را حالت پایه، یعنی حالت ساکن نامیده میشود ، در حالی که انتقال الکترون به سطح بالاتر منجر به حالت برانگیخته میشود. [85] انرژی الکترون همراه با n افزایش می یابد زیرا فاصله (متوسط) تا هسته افزایش می یابد. وابستگی انرژی به ℓ نه توسط پتانسیل الکترواستاتیکی هسته، بلکه توسط برهمکنش بین الکترون ها ایجاد می شود.
برای انتقال یک الکترون بین دو حالت مختلف ، مثلاً حالت پایه به حالت اول برانگیخته ، باید فوتونی را با انرژی منطبق با اختلاف انرژی پتانسیل آن سطوح جذب یا ساطع کند، طبق مدل نیلز بور ، دقیقاً چه چیزی می تواند باشد. با معادله شرودینگر محاسبه می شود . الکترون ها بین اوربیتال ها به شکل ذره ای می پرند. به عنوان مثال، اگر یک فوتون به الکترون ها برخورد کند، تنها یک الکترون در پاسخ به فوتون حالت ها را تغییر می دهد. خواص الکترون را ببینید .
انرژی فوتون ساطع شده متناسب با فرکانس آن است ، بنابراین این سطوح انرژی خاص به صورت نوارهای مجزا در طیف الکترومغناطیسی ظاهر می شوند . [86] هر عنصر دارای یک طیف مشخصه است که می تواند به بار هسته ای، لایه های فرعی پر شده توسط الکترون ها، برهمکنش های الکترومغناطیسی بین الکترون ها و عوامل دیگر بستگی داشته باشد. [87]

هنگامی که طیف پیوسته ای از انرژی از یک گاز یا پلاسما عبور می کند، برخی از فوتون ها توسط اتم ها جذب می شوند و باعث می شوند الکترون ها سطح انرژی خود را تغییر دهند. آن دسته از الکترونهای برانگیختهای که به اتم خود متصل میمانند، بهطور خود به خود این انرژی را بهعنوان فوتون ساطع میکنند و در یک جهت تصادفی حرکت میکنند و بنابراین به سطوح انرژی پایینتر برمیگردند. بنابراین اتمها مانند فیلتری عمل میکنند که یک سری نوارهای جذب تیره را در خروجی انرژی تشکیل میدهد. (ناظری که اتمها را از منظرهای میبیند که طیف پیوسته در پسزمینه را شامل نمیشود، در عوض یک سری خطوط نشری از فوتونهای ساطع شده توسط اتمها را میبیند.) اندازهگیریهای طیفسنجی قدرت و عرض خطوط طیفی اتمی ترکیب را امکانپذیر میسازد. و خواص فیزیکی یک ماده باید تعیین شود. [88]
بررسی دقیق خطوط طیفی نشان میدهد که برخی از آنها شکافتن ساختار ظریفی را نشان میدهند . این به دلیل جفت شدن اسپین-مدار ، که برهمکنشی بین اسپین و حرکت بیرونی ترین الکترون است، رخ می دهد. [89] هنگامی که یک اتم در یک میدان مغناطیسی خارجی قرار دارد، خطوط طیفی به سه یا چند جزء تقسیم میشوند. پدیده ای به نام اثر زیمن . این ناشی از برهمکنش میدان مغناطیسی با گشتاور مغناطیسی اتم و الکترون های آن است. برخی از اتمها میتوانند پیکربندیهای الکترونی متعددی با سطح انرژی یکسان داشته باشند، که بنابراین به صورت یک خط طیفی منفرد ظاهر میشوند. برهمکنش میدان مغناطیسی با اتم این پیکربندیهای الکترونی را به سطوح انرژی کمی متفاوت منتقل میکند و در نتیجه خطوط طیفی متعددی ایجاد میشود. [90] حضور یک میدان الکتریکی خارجی میتواند باعث شکافتن و جابجایی قابل مقایسه خطوط طیفی با اصلاح سطوح انرژی الکترون شود، پدیدهای که اثر استارک نامیده میشود . [91]
اگر یک الکترون مقید در حالت برانگیخته باشد، یک فوتون در حال تعامل با انرژی مناسب میتواند باعث گسیل تحریکشده یک فوتون با سطح انرژی منطبق شود. برای اینکه این اتفاق بیفتد، الکترون باید به حالت انرژی پایینتری بیفتد که دارای اختلاف انرژی با انرژی فوتون برهم کنش است. سپس فوتون ساطع شده و فوتون برهم کنش به صورت موازی و با فازهای منطبق حرکت می کنند. یعنی الگوهای موجی دو فوتون با هم هماهنگ هستند. از این ویژگی فیزیکی برای ساخت لیزر استفاده می شود که می تواند یک پرتو منسجم از انرژی نور را در یک باند فرکانسی باریک ساطع کند. [92]
ظرفیت، قدرت ترکیب یک عنصر است. با تعداد پیوندهایی که می تواند به اتم ها یا گروه های دیگر ایجاد کند تعیین می شود. [93] بیرونی ترین لایه الکترونی یک اتم در حالت غیرترکیب آن به عنوان لایه ظرفیتی شناخته می شود و الکترون های موجود در آن پوسته الکترون های ظرفیتی نامیده می شوند . تعداد الکترون های ظرفیت رفتار پیوند با اتم های دیگر را تعیین می کند. اتمها تمایل دارند بهگونهای با یکدیگر واکنش شیمیایی بدهند که لایههای ظرفیت بیرونی آنها را پر کند (یا خالی کند). [94] به عنوان مثال، انتقال یک الکترون منفرد بین اتم ها یک تقریب مفید برای پیوندهایی است که بین اتم هایی با یک الکترون بیشتر از یک پوسته پر و سایر پیوندهایی که یک الکترون کمتر از یک پوسته کامل دارند، تشکیل می شود، مانند در ترکیب کلرید سدیم و سایر نمک های یونی شیمیایی. بسیاری از عناصر دارای ظرفیت های متعدد یا تمایل به اشتراک گذاری تعداد متفاوت الکترون در ترکیبات مختلف هستند. بنابراین، پیوند شیمیایی بین این عناصر، اشکال مختلفی از اشتراک الکترون را به خود می گیرد که فراتر از انتقال ساده الکترون است. به عنوان مثال می توان به عنصر کربن و ترکیبات آلی اشاره کرد . [95]
عناصر شیمیایی اغلب در یک جدول تناوبی نمایش داده می شوند که برای نمایش خواص شیمیایی تکرار شونده چیده شده است، و عناصر با همان تعداد الکترون ظرفیت گروهی را تشکیل می دهند که در همان ستون جدول تراز شده اند. (ردیف های افقی مربوط به پر شدن یک پوسته کوانتومی از الکترون ها است.) لایه بیرونی عناصر در سمت راست جدول کاملاً با الکترون ها پر شده است که منجر به ایجاد عناصر شیمیایی بی اثر می شود که به عنوان گازهای نجیب شناخته می شوند . [96] [97]

مقادیری از اتم ها در حالت های مختلف ماده یافت می شوند که به شرایط فیزیکی مانند دما و فشار بستگی دارد . با تغییر شرایط، مواد می توانند بین جامدات ، مایعات ، گازها و پلاسما جابجا شوند . [98] در یک حالت، یک ماده می تواند در آلوتروپ های مختلف نیز وجود داشته باشد . نمونه ای از این کربن جامد است که می تواند به صورت گرافیت یا الماس وجود داشته باشد . [99] آلوتروپ های گازی نیز وجود دارند، مانند دی اکسیژن و ازن .
در دماهای نزدیک به صفر مطلق ، اتمها میتوانند یک میعان بوز-اینشتین تشکیل دهند ، در این نقطه اثرات مکانیکی کوانتومی، که معمولاً فقط در مقیاس اتمی مشاهده میشوند، در مقیاس ماکروسکوپی آشکار میشوند. [100] [101] این مجموعه فوق سرد اتم سپس به عنوان یک ابر اتم منفرد رفتار می کند ، که ممکن است امکان بررسی اساسی رفتار مکانیکی کوانتومی را فراهم کند. [102]

در حالی که اتم ها برای دیده شدن بسیار کوچک هستند، دستگاه هایی مانند میکروسکوپ تونل زنی روبشی (STM) امکان تجسم آنها را در سطوح جامدات فراهم می کند. این میکروسکوپ از پدیده تونل زنی کوانتومی استفاده می کند که به ذرات اجازه می دهد از سدی عبور کنند که در دیدگاه کلاسیک غیرقابل عبور است. الکترون ها از خلاء بین دو الکترود بایاس تونل می زنند و جریان تونل زنی را فراهم می کنند که به طور نمایی به جدایی آنها وابسته است. یک الکترود یک نوک تیز است که به طور ایده آل به یک اتم ختم می شود. در هر نقطه از اسکن سطح، ارتفاع نوک به گونه ای تنظیم می شود که جریان تونل زنی را در یک مقدار تنظیم شده نگه دارد. اینکه نوک چقدر به سمت سطح حرکت می کند و از آن دور می شود به عنوان مشخصات ارتفاع تعبیر می شود. برای بایاس کم، میکروسکوپ اوربیتالهای الکترونی متوسط را در سراسر سطوح انرژی نزدیک به هم - چگالی محلی حالتهای الکترونیکی نزدیک به سطح فرمی - تصویر میکند . [103] [104] به دلیل فواصل درگیر، هر دو الکترود باید بسیار پایدار باشند. تنها در این صورت می توان تناوب هایی را مشاهده کرد که با اتم های منفرد مطابقت دارند. این روش به تنهایی از نظر شیمیایی خاص نیست و نمی تواند گونه های اتمی موجود در سطح را شناسایی کند.
اتم ها را می توان به راحتی از روی جرم آنها تشخیص داد. اگر یک اتم با حذف یکی از الکترون هایش یونیزه شود ، مسیر حرکت آن هنگام عبور از میدان مغناطیسی خم می شود. شعاع چرخش مسیر یک یون متحرک توسط میدان مغناطیسی توسط جرم اتم تعیین می شود. طیف سنج جرمی از این اصل برای اندازه گیری نسبت جرم به بار یون ها استفاده می کند. اگر نمونه ای حاوی ایزوتوپ های متعدد باشد، طیف سنج جرمی می تواند نسبت هر ایزوتوپ در نمونه را با اندازه گیری شدت پرتوهای مختلف یون تعیین کند. تکنیکهای تبخیر اتمها شامل طیفسنجی نشر اتمی پلاسمای جفت شده القایی و طیفسنجی جرمی پلاسمای جفت شده القایی است ، که هر دو از پلاسما برای تبخیر نمونهها برای تجزیه و تحلیل استفاده میکنند. [105]
توموگراف کاوشگر اتمی دارای وضوح زیر نانومتری در سه بعدی است و می تواند اتم های جداگانه را با استفاده از طیف سنجی جرمی زمان پرواز شناسایی کند . [106]
تکنیکهای انتشار الکترون مانند طیفسنجی فوتوالکترون پرتو ایکس (XPS) و طیفسنجی الکترونی اوگر (AES)، که انرژی اتصال الکترونهای هسته را اندازهگیری میکنند ، برای شناسایی گونههای اتمی موجود در نمونه به روشی غیر مخرب استفاده میشوند. با فوکوس مناسب هر دو را می توان به منطقه خاص تبدیل کرد. یکی دیگر از این روشها، طیفسنجی از دست دادن انرژی الکترون (EELS) است که اتلاف انرژی یک پرتو الکترونی را در یک میکروسکوپ الکترونی عبوری هنگام تعامل با بخشی از نمونه اندازهگیری میکند.
طیف حالت های برانگیخته را می توان برای تجزیه و تحلیل ترکیب اتمی ستاره های دور استفاده کرد . طول موجهای نوری خاص موجود در نور مشاهدهشده از ستارگان را میتوان جدا کرد و به انتقال کوانتیزهشده در اتمهای گاز آزاد مرتبط کرد. این رنگ ها را می توان با استفاده از یک لامپ تخلیه گاز حاوی همان عنصر تکرار کرد. [107] هلیم به این روش در طیف خورشید 23 سال قبل از پیدا شدن در زمین کشف شد. [108]
ماده باریونی حدود 4 درصد از چگالی انرژی کل جهان قابل مشاهده را با چگالی متوسط حدود 0.25 ذره در متر مکعب (بیشتر پروتون ها و الکترون ها) تشکیل می دهد. [109] در کهکشانی مانند راه شیری ، ذرات دارای غلظت بسیار بالاتری هستند، با چگالی ماده در محیط بین ستارهای (ISM) بین 105 تا 109 اتم بر متر مکعب . [110] اعتقاد بر این است که خورشید در داخل حباب محلی قرار دارد ، بنابراین چگالی در همسایگی خورشیدی تنها حدود 103 اتم بر متر مکعب است . [111] ستارگان از ابرهای متراکم در ISM تشکیل میشوند و فرآیندهای تکاملی ستارگان منجر به غنیسازی پیوسته ISM با عناصری پرجرمتر از هیدروژن و هلیوم میشود.
تا 95 درصد از ماده باریونی کهکشان راه شیری در داخل ستارگان متمرکز شده است، جایی که شرایط برای ماده اتمی نامطلوب است. کل جرم باریونی حدود 10 درصد از جرم کهکشان است. [112] باقیمانده جرم یک ماده تاریک ناشناخته است . [113] دمای بالا در داخل ستارگان باعث میشود که بیشتر «اتمها» کاملاً یونیزه شوند، یعنی همه الکترونها را از هسته جدا میکند. در بقایای ستارهها - به استثنای لایههای سطحی آنها - یک فشار بسیار زیاد ، لایههای الکترونی را غیرممکن میکند.
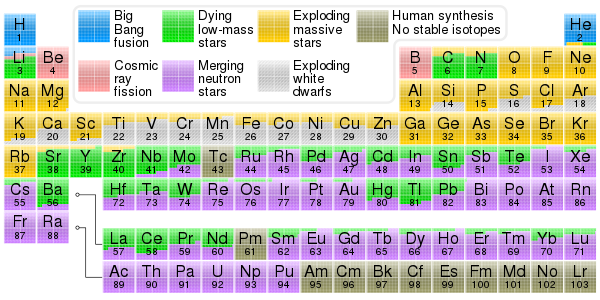
تصور می شود که الکترون ها از مراحل اولیه انفجار بزرگ در کیهان وجود داشته باشند . هسته های اتمی در واکنش های سنتز هسته تشکیل می شوند . در حدود سه دقیقه، بیگ بنگ بیشتر هلیوم ، لیتیوم و دوتریوم در جهان و شاید مقداری بریلیم و بور را تولید کرد . [114] [115] [116]
همه جا حاضر بودن و پایداری اتم ها به انرژی اتصال آنها بستگی دارد ، به این معنی که یک اتم انرژی کمتری نسبت به یک سیستم غیر محدود هسته و الکترون دارد. در جایی که دما بسیار بالاتر از پتانسیل یونیزاسیون است ، ماده به شکل پلاسما وجود دارد - گازی از یونهای با بار مثبت (احتمالاً هستههای خالی) و الکترونها. وقتی دما به زیر پتانسیل یونیزاسیون میرسد، اتمها از نظر آماری مطلوب میشوند. اتم ها (کامل با الکترون های مقید) 380000 سال پس از بیگ بنگ بر ذرات باردار تسلط یافتند - دوره ای به نام نوترکیب ، زمانی که جهان در حال انبساط به اندازه کافی سرد شد تا الکترون ها به هسته ها متصل شوند. [117]
از زمان انفجار بزرگ، که کربن یا عناصر سنگینتری تولید نکرد، هستههای اتمی در ستارگان از طریق فرآیند همجوشی هستهای برای تولید بیشتر عنصر هلیوم و (از طریق فرآیند آلفای سهگانه ) توالی عناصر از کربن به بالا ترکیب شدهاند . اتو کردن ; [118] برای جزئیات بیشتر به سنتز هسته ستاره ای مراجعه کنید .
ایزوتوپ هایی مانند لیتیوم-6 و همچنین مقداری بریلیم و بور از طریق پوسته شدن پرتوهای کیهانی در فضا تولید می شوند . [119] این اتفاق زمانی رخ میدهد که یک پروتون پرانرژی به هسته اتم برخورد میکند و باعث میشود تعداد زیادی نوکلئون به بیرون پرتاب شوند.
عناصر سنگینتر از آهن در ابرنواخترها و ستارگان نوترونی در حال برخورد از طریق فرآیند r و در ستارگان AGB از طریق فرآیند s تولید شدند که هر دو شامل جذب نوترون توسط هستههای اتمی هستند. [120] عناصری مانند سرب عمدتاً از طریق واپاشی رادیواکتیو عناصر سنگینتر تشکیل میشوند. [121]
بیشتر اتمهایی که زمین و ساکنان آن را تشکیل میدهند به شکل کنونی خود در سحابی حضور داشتند که از یک ابر مولکولی فرو ریخت و منظومه شمسی را تشکیل داد . بقیه نتیجه تجزیه رادیواکتیو هستند و نسبت نسبی آنها را می توان برای تعیین سن زمین از طریق تاریخ گذاری رادیومتری استفاده کرد . [122] [123] بیشتر هلیوم در پوسته زمین (حدود 99٪ هلیوم حاصل از چاه های گاز، همانطور که با فراوانی کمتر هلیوم 3 نشان داده شده است ) محصول فروپاشی آلفا است . [124]
چند اتم ناچیز روی زمین وجود دارد که در ابتدا وجود نداشتند (یعنی "اولیه" نبودند) و همچنین نتایج واپاشی رادیواکتیو نیز وجود نداشت. کربن 14 به طور مداوم توسط پرتوهای کیهانی در جو تولید می شود. [125] برخی از اتم های روی زمین به طور مصنوعی یا عمدا یا به عنوان محصولات جانبی راکتورهای هسته ای یا انفجارها تولید شده اند. [126] [127] از عناصر فرااورانی - آنهایی که اعداد اتمی آنها بیشتر از 92 است - فقط پلوتونیوم و نپتونیم به طور طبیعی در زمین وجود دارند. [128] [129] عناصر فرااورانی دارای طول عمر رادیواکتیو کمتر از سن کنونی زمین هستند [130] و بنابراین مقادیر قابل شناسایی از این عناصر مدتهاست که تجزیه شده اند، به استثنای آثار پلوتونیوم-244 که احتمالاً توسط غبار کیهانی رسوب کرده است. [122] ذخایر طبیعی پلوتونیوم و نپتونیم با جذب نوترون در سنگ معدن اورانیوم تولید می شوند. [131]
زمین تقریباً شامل1.33 × 10 50 اتم. [132] اگرچه تعداد کمی از اتمهای مستقل گازهای نجیب مانند آرگون ، نئون و هلیوم وجود دارد ، 99 درصد اتمسفر به شکل مولکولهایی از جمله دیاکسید کربن و اکسیژن و نیتروژن دو اتمی متصل است . در سطح زمین، اکثریت قریب به اتفاق اتم ها با هم ترکیب می شوند و ترکیبات مختلفی از جمله آب ، نمک ، سیلیکات ها و اکسیدها را تشکیل می دهند . اتم ها همچنین می توانند برای ایجاد موادی که از مولکول های مجزا تشکیل نشده اند، ترکیب شوند، از جمله کریستال ها و فلزات مایع یا جامد . [133] [134] این ماده اتمی ترتیبات شبکه ای را تشکیل می دهد که فاقد نوع خاصی از نظم قطع شده در مقیاس کوچک مرتبط با ماده مولکولی است. [135]
همه هستههای با اعداد اتمی بالاتر از 82 ( سرب ) رادیواکتیو هستند. هیچ هسته ای با عدد اتمی بیش از 92 ( اورانیوم ) به عنوان هسته اولیه روی زمین وجود ندارد و عناصر سنگین تر معمولا نیمه عمر کوتاه تری دارند. با این وجود، ممکن است یک « جزیره پایداری » شامل ایزوتوپهای نسبتاً طولانی از عناصر فوقسنگین [136] با اعداد اتمی 110 تا 114 وجود داشته باشد. [137] پیش بینی ها برای نیمه عمر پایدارترین هسته هسته ای در جزیره از چند دقیقه تا میلیون ها سال متغیر است. [138] در هر صورت، عناصر فوق سنگین (با Z > 104) به دلیل افزایش دافعه کولن (که منجر به شکافت خود به خودی با نیمه عمر کوتاه فزاینده می شود) در غیاب هر گونه اثرات تثبیت کننده وجود ندارند . [139]
هر ذره ماده دارای یک ذره ضد ماده با بار الکتریکی مخالف است. بنابراین، پوزیترون یک پادالکترون با بار مثبت و آنتی پروتون معادل یک پروتون با بار منفی است . هنگامی که یک ماده و ذره ضد ماده مربوطه به هم می رسند، یکدیگر را از بین می برند. به همین دلیل، همراه با عدم تعادل بین تعداد ماده و ذرات پادماده، ذرات دوم در جهان نادر هستند. اولین علل این عدم تعادل هنوز به طور کامل شناخته نشده است، اگرچه نظریه های باریوژنز ممکن است توضیحی ارائه دهند. در نتیجه هیچ اتم ضد ماده در طبیعت کشف نشده است. [140] [141] در سال 1996، همتای پادماده اتم هیدروژن ( پاد هیدروژن ) در آزمایشگاه CERN در ژنو سنتز شد . [142] [143]
اتمهای عجیب و غریب دیگری با جایگزینی یکی از پروتونها، نوترونها یا الکترونها با ذرات دیگری که بار مشابهی دارند ایجاد شدهاند. به عنوان مثال، یک الکترون را می توان با یک میون پرجرم تر جایگزین کرد و یک اتم مویونی را تشکیل داد . از این نوع اتم ها می توان برای آزمایش پیش بینی های اساسی فیزیک استفاده کرد. [144] [145] [146]
2,000,000,000,000,000,000,000 (یعنی 2 هفتصد میلیارد) اتم اکسیژن در یک قطره آب و دو برابر اتم هیدروژن وجود دارد.