قلیاییت (از عربی : القلوية ، رومی : al-qaly ، روشن ، خاکستر شوره ) [1] ظرفیت آب برای مقاومت در برابر اسیدی شدن است . [2] نباید آن را با پایه که یک اندازه گیری مطلق در مقیاس pH است، اشتباه گرفت . قلیاییت قدرت محلول بافری است که از اسیدهای ضعیف و بازهای مزدوج آنها تشکیل شده است . با تیتر کردن محلول با اسیدی مانند HCl اندازه گیری می شود تا زمانی که pH آن به طور ناگهانی تغییر کند یا به نقطه پایانی مشخصی برسد که در آن اتفاق می افتد . قلیاییت بر حسب واحدهای غلظت، مانند meq/L ( میلیاکیوالان در لیتر )، µeq/kg (میکرو معادل در کیلوگرم)، یا mg/L CaCO 3 (میلیگرم در لیتر کربنات کلسیم ) بیان میشود. [3] هر یک از این اندازهگیریها مربوط به مقدار اسید اضافه شده به عنوان تیترانت است .
در آبهای شیرین ، بهویژه آنهایی که در زمینهای غیرآهکی قرار دارند ، قلیائیت کم است و یونهای زیادی را در بر میگیرد. از سوی دیگر، در اقیانوس ها، قلیاییت به طور کامل توسط کربنات و بی کربنات به اضافه سهم کمی از بورات تسلط دارد . [4]
اگرچه قلیایییت در درجه اول اصطلاحی است که توسط لیم شناسان [5] و اقیانوس شناسان [3] استفاده می شود ، [3] توسط هیدرولوژیست ها برای توصیف سختی موقت نیز استفاده می شود . علاوه بر این، اندازه گیری قلیاییت در تعیین توانایی یک جریان برای خنثی کردن آلودگی اسیدی ناشی از بارندگی یا فاضلاب مهم است . این یکی از بهترین معیارهای سنجش حساسیت جریان به ورودی های اسید است. [6] میتواند تغییرات طولانیمدتی در قلیاییت نهرها و رودخانهها در پاسخ به اختلالات انسانی مانند باران اسیدی ناشی از انتشار SOx و NOx ایجاد کند . [7]
در سال 1884، پروفسور ویلهلم (ویلیام) دیتمار از کالج اندرسون، که اکنون دانشگاه استراثکلاید است ، 77 نمونه آب دریای بکر از سراسر جهان را که توسط اکسپدیشن چلنجر بازگردانده شده بود، تجزیه و تحلیل کرد . او دریافت که در آب دریا یونهای اصلی در یک نسبت ثابت قرار دارند و این فرضیه یوهان گئورگ فورشامر را تأیید میکند که اکنون به عنوان اصل نسبتهای ثابت شناخته میشود. با این حال، یک استثنا وجود داشت. دیتمار دریافت که غلظت کلسیم در اعماق اقیانوس اندکی بیشتر است و این افزایش را قلیایی نامید. [ نیازمند منبع ]
همچنین در سال 1884، سوانت آرنیوس پایان نامه های دکترای خود را ارائه کرد که در آن از وجود یون ها در محلول دفاع می کرد و اسیدها را به عنوان دهنده یون هیدرونیوم و بازها را به عنوان اهدا کننده یون هیدروکسید تعریف می کرد . برای آن کار، او در سال 1903 جایزه نوبل شیمی را دریافت کرد .
قلیاییت تقریباً به مقدار مولی بازها در یک محلول اطلاق می شود که می تواند توسط یک اسید قوی به گونه های بدون بار تبدیل شود. به عنوان مثال، 1 مول HCO-
3در محلول نشان دهنده 1 معادل مولی است، در حالی که 1 مول CO2-
32 معادل مولی است زیرا دو برابر یون H + برای متعادل کردن بار لازم است. بار کل یک محلول همیشه برابر با صفر است. [8] این منجر به تعریف موازی قلیایی می شود که بر اساس تعادل بار یون ها در یک محلول است.
یونهای خاصی از جمله Na + ، K + ، Ca 2 + ، Mg 2 + ، Cl- ، SO2-
4، و نه-
3" محافظه کارانه " هستند به طوری که تحت تأثیر تغییرات دما، فشار یا pH قرار نمی گیرند. [8] دیگران مانند HCO-
3تحت تأثیر تغییرات pH، دما و فشار قرار می گیرند. با جداسازی یونهای محافظهکار در یک طرف این معادله تعادل بار، یونهای غیرمحافظهکاری که پروتون را میپذیرند یا اهدا میکنند و بنابراین قلیائیت را تعریف میکنند، در سمت دیگر معادله قرار میگیرند.
این تعادل بار و تعادل پروتون ترکیبی را قلیایی کل می نامند . [9] قلیاییت کل (بسیار) تحت تأثیر دما، فشار یا pH قرار نمی گیرد و بنابراین خود یک اندازه گیری محافظه کارانه است که سودمندی آن را در سیستم های آبی افزایش می دهد. همه آنیون ها به جز HCO-
3و CO2-
3غلظت کمی در آب های سطحی زمین ( نهرها، رودخانه ها و دریاچه ها) دارند. بنابراین قلیاییت کربناتی که برابر با [ HCO است-
3] + 2 [ CO2-
3] نیز تقریباً برابر با کل قلیائیت آبهای سطحی است. [8]
قلیاییت توانایی یک محلول برای خنثی کردن اسیدها به نقطه هم ارزی کربنات یا بی کربنات را اندازه گیری می کند که برای بسیاری از مطالعات اقیانوس شناسی/لیمنولوژی به صورت pH 4.5 تعریف شده است. [10] قلیاییت برابر است با مجموع استوکیومتری بازهای موجود در محلول. در بیشتر آبهای سطح زمین، قلیاییت کربناته بیشتر قلیائیت کل را تشکیل میدهد، زیرا بهدلیل رخداد و انحلال معمول سنگهای کربناته و سایر فرآیندهای هوازدگی زمینشناسی که آنیونهای کربناته تولید میکنند. سایر اجزای طبیعی رایج که می توانند به قلیایی بودن کمک کنند عبارتند از: بورات ، هیدروکسید ، فسفات ، سیلیکات ، آمونیاک محلول ، و بازهای مزدوج اسیدهای آلی (مثلا استات ). محلول های تولید شده در آزمایشگاه ممکن است حاوی تعداد نامحدودی از گونه ها باشد که در قلیایی بودن نقش دارند. قلیاییت اغلب به صورت معادل مولی در هر لیتر محلول یا هر کیلوگرم حلال داده می شود. در زمینههای تجاری (مثلاً صنعت استخرهای شنا) و زمینههای نظارتی، قلیاییت ممکن است بر حسب بخش در میلیون کربنات کلسیم معادل (ppm CaCO 3 ) داده شود [ نیاز به منبع ] . گاهی اوقات قلیاییت به اشتباه به جای پایه استفاده می شود . به عنوان مثال، افزودن CO 2 PH محلول را کاهش می دهد، در نتیجه باز بودن را کاهش می دهد در حالی که قلیاییت بدون تغییر باقی می ماند (نمونه زیر را ببینید).
انواع تیترانت ها ، نقاط پایانی و شاخص ها برای روش های مختلف اندازه گیری قلیایی مشخص شده است. اسیدهای کلریدریک و سولفوریک تیترهای رایج اسیدی هستند، در حالی که فنل فتالئین ، متیل رد و بروموکرزول سبز شاخص های رایج هستند. [11]
در آب های زیرزمینی یا آب دریا ، قلیایی کل اندازه گیری شده برابر با:
(زیرنویس T غلظت کل گونه در محلول را همانطور که اندازه گیری می شود نشان می دهد. این با غلظت آزاد مخالف است که مقدار قابل توجهی از فعل و انفعالات جفت یونی را که در آب دریا رخ می دهد در نظر می گیرد.)
قلیاییت را می توان با تیتر کردن نمونه با اسید قوی اندازه گیری کرد تا زمانی که تمام ظرفیت بافر یون های فوق بالاتر از pH بی کربنات یا کربنات مصرف شود. این نقطه از نظر عملکرد روی pH 4.5 تنظیم شده است. در این مرحله، تمام پایههای مورد نظر به گونههای سطح صفر پروتونه شدهاند، بنابراین دیگر باعث قلیایی نمیشوند. در سیستم کربنات یونهای بی کربنات [ HCO-
3] و یون های کربنات [ CO2-
3] در این pH به اسید کربنیک [H 2 CO 3 ] تبدیل شده اند . به این pH نقطه هم ارزی CO 2 نیز می گویند که در آن جزء اصلی در آب CO 2 حل می شود که در یک محلول آبی به H 2 CO 3 تبدیل می شود. در این مرحله هیچ اسید یا باز قوی وجود ندارد. بنابراین، قلیاییت با توجه به نقطه هم ارزی CO 2 مدل و کمی سازی می شود . از آنجا که قلیاییت با توجه به نقطه هم ارزی CO 2 اندازه گیری می شود ، انحلال CO 2 ، اگرچه اسید و کربن معدنی محلول را اضافه می کند، قلیاییت را تغییر نمی دهد. در شرایط طبیعی، انحلال سنگ های اساسی و افزودن آمونیاک [NH 3 ] یا آمین های آلی منجر به افزودن باز به آب های طبیعی در نقطه هم ارزی CO 2 می شود . باز محلول در آب PH را افزایش می دهد و مقدار معادل CO 2 را به یون بی کربنات و یون کربنات تیتر می کند. در حالت تعادل، آب حاوی مقدار معینی قلیائیت است که توسط غلظت آنیون های اسید ضعیف ایجاد می شود. برعکس، افزودن اسید آنیونهای اسید ضعیف را به CO 2 تبدیل می کند و افزودن مداوم اسیدهای قوی می تواند باعث شود که قلیاییت کمتر از صفر شود. [12] برای مثال، واکنشهای زیر در طول افزودن اسید به محلول معمولی آب دریا اتفاق میافتد:
از واکنشهای پروتونهسازی بالا میتوان دریافت که بیشتر بازها برای تبدیل شدن به گونهای خنثی، یک پروتون (H + ) مصرف میکنند و در نتیجه قلیاییت را یک برابر در هر معادل افزایش میدهند. CO2-
3با این حال، قبل از تبدیل شدن به یک گونه سطح صفر (CO 2 ) دو پروتون مصرف می کند، بنابراین قلیاییت را دو در هر مول CO افزایش می دهد.2-
3. [H + ] و [ HSO-
4] خاصیت قلیایی را کاهش می دهند، زیرا آنها به عنوان منابع پروتون عمل می کنند. آنها اغلب به صورت جمعی به عنوان [H + ] T نشان داده می شوند .
قلیاییت معمولاً به صورت mg/L به صورت CaCO 3 گزارش می شود . (در این مورد ربط "as" مناسب است زیرا قلیاییت حاصل از مخلوطی از یون ها است اما "گویی" گزارش شده است که همه اینها به دلیل CaCO 3 است .) این می تواند به میلی اکی والان در هر لیتر (meq/L) تبدیل شود. با تقسیم بر 50 ( مگاوات تقریبی CaCO 3 تقسیم بر 2).
افزودن (یا حذف) CO 2 به یک محلول، قلیایی بودن آن را تغییر نمی دهد، زیرا واکنش خالص همان تعداد معادل گونه های کمک کننده مثبت (H + ) را با گونه های کمک کننده منفی ( HCO) تولید می کند.-
3و/یا CO2-
3). افزودن CO 2 به محلول pH آن را کاهش می دهد، اما قلیایی بودن آن را تحت تاثیر قرار نمی دهد.
در تمام مقادیر pH:
فقط در مقادیر pH بالا (پایه):
افزودن CO 2 به محلول در تماس با یک جامد می تواند (به مرور زمان) بر خاصیت قلیایی تأثیر بگذارد، به ویژه برای مواد معدنی کربناته در تماس با آب های زیرزمینی یا آب دریا. انحلال (یا بارش) سنگ کربناته تأثیر زیادی بر قلیایی بودن دارد. این به این دلیل است که سنگ کربنات از CaCO 3 تشکیل شده است و تجزیه آن باعث اضافه شدن Ca 2 + و CO می شود.2-
3به محلول. Ca 2+ بر قلیایی بودن تأثیر نمی گذارد، اما CO2-
32 واحد قلیائیت را افزایش می دهد. افزایش انحلال سنگ کربناته توسط اسیدی شدن از باران اسیدی و استخراج معدن به افزایش غلظت قلیایی در برخی از رودخانه های اصلی در سراسر شرق ایالات متحده کمک کرده است [7] واکنش زیر نشان می دهد که چگونه باران اسیدی، حاوی اسید سولفوریک، می تواند تأثیر قلیایی رودخانه را افزایش دهد. افزایش مقدار یون بی کربنات:
روش دیگر نوشتن این است:
هرچه PH کمتر باشد، غلظت بی کربنات بیشتر خواهد بود. این نشان می دهد که اگر مقدار بی کربنات تولید شده بیشتر از مقدار H + باقی مانده پس از واکنش باشد، چگونه PH پایین می تواند منجر به قلیائیت بالاتر شود. از آنجایی که میزان اسید موجود در آب باران کم است، به این صورت است. اگر این آب زیرزمینی قلیایی بعداً با اتمسفر تماس پیدا کند، می تواند CO 2 را از دست بدهد ، کربنات را رسوب دهد و در نتیجه دوباره کمتر قلیایی شود. هنگامی که مواد معدنی کربناته، آب و اتمسفر همه در تعادل هستند، واکنش برگشت پذیر است
نشان می دهد که pH با غلظت یون کلسیم مرتبط خواهد بود، با pH پایین تر با غلظت یون کلسیم بالاتر. در این حالت، هرچه PH بالاتر باشد، یون بی کربنات و کربنات بیشتری وجود خواهد داشت، برخلاف وضعیت متناقضی که در بالا توضیح داده شد، که در آن فرد تعادلی با جو ندارد.
در اقیانوس، قلیائیت به طور کامل توسط کربنات و بی کربنات به اضافه سهم کوچکی از بورات تسلط دارد . [4]
بنابراین معادله شیمیایی قلیایی بودن در آب دریا به صورت زیر است:
روش های زیادی برای تولید قلیایی در اقیانوس ها وجود دارد . شاید شناخته شده ترین انحلال کربنات کلسیم برای تشکیل Ca2 + و CO باشد.2-
3(کربنات). یون کربنات پتانسیل جذب دو یون هیدروژن را دارد. بنابراین باعث افزایش خالص قلیائیت اقیانوس می شود. انحلال کربنات کلسیم در مناطقی از اقیانوس که نسبت به کربنات کلسیم کمتر از حد اشباع هستند، رخ می دهد.
افزایش سطح دی اکسید کربن در جو ، به دلیل انتشار دی اکسید کربن ، منجر به افزایش جذب CO2 از جو به اقیانوس ها می شود. [13] این بر خاصیت قلیایی اقیانوس تأثیر نمی گذارد [14] : 2252 اما منجر به کاهش مقدار pH می شود (به نام اسیدی شدن اقیانوس ). [15] افزایش قلیایی اقیانوس به عنوان یکی از گزینهها برای افزودن قلیایی به اقیانوس و بنابراین بافر در برابر تغییرات pH پیشنهاد شده است. [16] : 181
فرآیندهای بیولوژیکی در بازه های زمانی کوتاه (دقیقه تا قرن ها) تأثیر بسیار بیشتری بر قلیایی بودن اقیانوس ها دارند. [17] نیترات زدایی و کاهش سولفات در محیطهای با اکسیژن محدود رخ میدهد. هر دوی این فرآیندها یون های هیدروژن را مصرف می کنند (در نتیجه قلیاییت را افزایش می دهند) و گازهایی (N 2 یا H 2 S) آزاد می کنند که در نهایت به اتمسفر می روند. نیتریفیکاسیون و اکسیداسیون سولفید هر دو با آزاد کردن پروتون ها به عنوان محصول جانبی واکنش های اکسیداسیون، قلیاییت را کاهش می دهند. [18]
قلیایی بودن اقیانوس ها در طول زمان تغییر می کند، به طور قابل توجهی در مقیاس های زمانی زمین شناسی (هزاره ها). تغییرات در تعادل بین هوازدگی زمینی و رسوب مواد معدنی کربناته (به عنوان مثال، به عنوان تابعی از اسیدی شدن اقیانوس) محرک های اصلی قلیایی بودن در اقیانوس ها در دراز مدت هستند. [19] در بازههای زمانی انسانی، میانگین قلیایی بودن اقیانوس نسبتاً پایدار است. [20] تنوع فصلی و سالانه میانگین قلیایی اقیانوس بسیار کم است. [21]
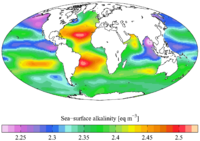
قلیاییت بر اساس مکان بسته به تبخیر / بارش، فرارفت آب، فرآیندهای بیولوژیکی و فرآیندهای ژئوشیمیایی متفاوت است. [4]
اختلاط تحت سلطه رودخانه نیز نزدیک به ساحل رخ می دهد. در نزدیکی دهانه یک رودخانه بزرگ قوی ترین است. در اینجا، رودخانه ها می توانند به عنوان منبع یا غرق قلیایی عمل کنند. A T خروجی رودخانه را دنبال می کند و با شوری رابطه خطی دارد. [21]
قلیائیت اقیانوسی نیز از روندهای کلی بر اساس عرض و عمق پیروی می کند. نشان داده شده است که A T اغلب با دمای سطح دریا (SST) نسبت معکوس دارد . بنابراین، به طور کلی با عرض و عمق زیاد افزایش می یابد. در نتیجه، مناطق بالارونده (جایی که آب از اعماق اقیانوس به سطح رانده می شود) نیز ارزش قلیایی بالاتری دارند. [22]
برنامه های زیادی برای اندازه گیری، ثبت و مطالعه قلیائیت اقیانوسی به همراه بسیاری از ویژگی های دیگر آب دریا مانند دما و شوری وجود دارد. این موارد عبارتند از: GEOSECS (مطالعه بخشهای اقیانوس ژئوشیمیایی)، [23] TTO/NAS (ردیابهای گذرا در اقیانوس/مطالعه آتلانتیک شمالی)، JGOFS (مطالعه مشترک جریان جهانی اقیانوس)، [24] WOCE (آزمایش گردش اقیانوس جهانی)، [ 25] CARINA (دی اکسید کربن در اقیانوس اطلس). [26]
{{citation}}: CS1 maint: DOI از سپتامبر 2024 غیرفعال است ( پیوند )بسته های زیر وضعیت سیستم کربنات را در آب دریا (شامل pH) محاسبه می کنند: