
شوری ( / s ə ˈ l ɪ n ɪ t i / ) شوری یا مقدار نمک محلول در یک آب است که آب شور نامیده می شود (همچنین به شوری خاک مراجعه کنید ). معمولاً بر حسب گرم در لیتر یا گرم بر کیلوگرم (گرم نمک در هر لیتر/کیلوگرم آب؛ دومی بدون بعد و برابر با ‰) اندازه گیری می شود.
شوری عامل مهمی در تعیین بسیاری از جنبههای شیمیایی آبهای طبیعی و فرآیندهای بیولوژیکی درون آن است و یک متغیر حالت ترمودینامیکی است که همراه با دما و فشار ، بر ویژگیهای فیزیکی مانند چگالی و ظرفیت گرمایی آب حاکم است.
خط خطی با شوری ثابت ایزوهالین یا گاهی ایزوهال نامیده می شود .
شوری در رودخانهها، دریاچهها و اقیانوسها از نظر مفهومی ساده است، اما از نظر فنی برای تعریف و اندازهگیری دقیق آن چالش برانگیز است. از نظر مفهومی شوری مقدار نمک محلول آب است. نمک ها ترکیباتی مانند کلرید سدیم ، سولفات منیزیم ، نیترات پتاسیم و بی کربنات سدیم هستند که در یون ها حل می شوند. غلظت یون های کلرید محلول گاهی اوقات به عنوان کلریت نامیده می شود. از نظر عملیاتی، ماده محلول به عنوان ماده ای تعریف می شود که می تواند از یک فیلتر بسیار ریز عبور کند (از لحاظ تاریخی فیلتری با اندازه منافذ 0.45 میکرومتر، اما بعدا [ چه زمانی؟ ] معمولاً 0.2 میکرومتر). [2] شوری را می توان به صورت کسر جرمی بیان کرد ، یعنی جرم ماده محلول در یک واحد جرم محلول.
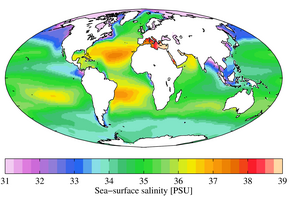
آب دریا معمولاً دارای شوری جرمی در حدود 35 گرم بر کیلوگرم است، اگرچه مقادیر پایین تر در نزدیکی سواحل که رودخانه ها وارد اقیانوس می شوند، معمول است. رودخانهها و دریاچهها میتوانند طیف وسیعی از شوری را داشته باشند، از کمتر از 0.01 گرم در کیلوگرم [3] تا چند گرم در کیلوگرم، اگرچه مکانهای زیادی وجود دارد که شوری بالاتری در آنها یافت میشود. شوری دریای مرده بیش از 200 گرم بر کیلوگرم است . [4] بارش معمولا دارای TDS 20 میلی گرم بر کیلوگرم یا کمتر است. [5]
هر اندازه منافذ در تعریف استفاده شود، مقدار شوری حاصل از یک نمونه معین از آب طبیعی بیش از چند درصد (%) تغییر نخواهد کرد . با این حال، اقیانوسشناسان فیزیکی که در اقیانوسهای پرتگاه کار میکنند ، اغلب نگران دقت و مقایسهپذیری اندازهگیریهای محققان مختلف، در زمانهای مختلف، تا تقریباً پنج رقم مهم هستند . [6] یک محصول آب دریا در بطری معروف به آب دریا استاندارد IAPSO توسط اقیانوس شناسان برای استانداردسازی اندازه گیری های خود با دقت کافی برای برآورده کردن این نیاز استفاده می شود.
مشکلات اندازه گیری و تعریف به این دلیل به وجود می آیند که آب های طبیعی حاوی مخلوط پیچیده ای از عناصر مختلف از منابع مختلف (نه همه از نمک های محلول) در اشکال مولکولی مختلف هستند. خواص شیمیایی برخی از این اشکال به دما و فشار بستگی دارد. اندازه گیری بسیاری از این اشکال با دقت بالا دشوار است و در هر صورت تجزیه و تحلیل شیمیایی کامل هنگام آنالیز نمونه های متعدد عملی نیست. تعاریف عملی متفاوتی از شوری ناشی از تلاشهای مختلف برای توضیح این مشکلات، تا سطوح مختلف دقت است، در حالی که هنوز استفاده از آن نسبتاً آسان است.
به دلایل عملی، شوری معمولاً به مجموع جرم زیرمجموعهای از این ترکیبات شیمیایی محلول (به اصطلاح شوری محلول ) مربوط میشود، نه به جرم ناشناخته نمکهایی که این ترکیب را به وجود آورده است (یک استثنا زمانی است که آب دریا مصنوعی باشد. ایجاد شده است). برای بسیاری از اهداف، این مجموع را می توان به مجموعه ای از هشت یون اصلی در آب های طبیعی محدود کرد، [7] [8] اگرچه برای آب دریا با بالاترین دقت، هفت یون فرعی اضافی نیز گنجانده شده است. [6] یونهای اصلی بر ترکیب غیر آلی اکثر (اما به هیچ وجه همه) آبهای طبیعی غالب هستند. استثناها شامل برخی دریاچه های گودال و آب های برخی از چشمه های گرمابی است .
غلظت گازهای محلول مانند اکسیژن و نیتروژن معمولاً در توصیف شوری گنجانده نمی شود. [2] با این حال، گاز دی اکسید کربن ، که زمانی که حل می شود تا حدی به کربنات ها و بی کربنات ها تبدیل می شود ، اغلب شامل می شود. سیلیکون به شکل اسید سیلیسیک ، که معمولاً به عنوان یک مولکول خنثی در محدوده pH اکثر آبهای طبیعی ظاهر میشود، ممکن است برای برخی اهداف (مثلاً زمانی که روابط شوری/چگالی بررسی میشود) گنجانده شود.
اصطلاح شوری برای اقیانوس شناسان معمولاً با یکی از مجموعه ای از تکنیک های اندازه گیری خاص همراه است. همانطور که تکنیکهای غالب تکامل مییابند، توصیفهای مختلف شوری نیز تغییر میکنند. شوری تا حد زیادی با استفاده از تکنیک های تیتراسیون قبل از دهه 1980 اندازه گیری شد. تیتراسیون با نیترات نقره می تواند برای تعیین غلظت یون های هالید (عمدتا کلر و برم ) برای بدست آوردن کلر استفاده شود . سپس کلر در یک فاکتور ضرب شد تا تمام اجزای دیگر محاسبه شود. شوری نادسن به دست آمده بر حسب واحد در هزار (ppt یا ‰ ) بیان می شود.
استفاده از اندازهگیریهای هدایت الکتریکی برای تخمین محتوای یونی آب دریا منجر به توسعه مقیاسی به نام مقیاس عملی شوری 1978 (PSS-78) شد. [9] [10] شوری های اندازه گیری شده با استفاده از PSS-78 واحد ندارند.پسوند psu یا PSU (که نشان دهنده واحد عملی شوری است ) گاهی به مقادیر اندازه گیری PSS-78 اضافه می شود. [11] افزودن PSU به عنوان یک واحد پس از مقدار "به طور رسمی نادرست و به شدت منع شده است". [2]
در سال 2010 استاندارد جدیدی برای خواص آب دریا به نام معادله ترمودینامیکی آب دریا 2010 ( TEOS-10 ) معرفی شد که از شوری مطلق به عنوان جایگزینی برای شوری عملی و دمای محافظه کارانه به عنوان جایگزینی برای دمای بالقوه حمایت می کند . [6] این استاندارد شامل مقیاس جدیدی به نام مقیاس شوری ترکیب مرجع است . شوری مطلق در این مقیاس به صورت کسر جرمی بر حسب گرم بر کیلوگرم محلول بیان می شود. شوری در این مقیاس با ترکیب اندازهگیریهای هدایت الکتریکی با سایر اطلاعاتی که میتواند تغییرات منطقهای در ترکیب آب دریا را توضیح دهد، تعیین میشود. آنها همچنین می توانند با اندازه گیری چگالی مستقیم تعیین شوند.
نمونه ای از آب دریا از اکثر مکان ها با کلرینیت 19.37 ppt، دارای شوری Knudsen 35.00 ppt، شوری عملی PSS-78 حدود 35.0، و TEOS-10 شوری مطلق حدود 35.2 گرم بر کیلوگرم خواهد بود. رسانایی الکتریکی این آب در دمای 15 درجه سانتی گراد 42.9 mS/cm است. [6] [12]
در مقیاس جهانی، بسیار محتمل است که تغییرات آب و هوایی ناشی از انسان به تغییرات مشاهده شده شوری سطحی و زیرسطحی از دهه 1950 کمک کرده باشد، و پیش بینی تغییرات شوری سطح در سراسر قرن بیست و یکم نشان می دهد که مناطق تازه اقیانوس همچنان تازه تر و شورتر خواهند شد. مناطق به شورتر شدن ادامه خواهند داد. [13]
شوری به عنوان ردیاب توده های مختلف عمل می کند. آب سطحی برای جایگزینی آب غرق شده به داخل کشیده می شود که در نهایت به اندازه کافی سرد و شور می شود تا غرق شود. توزیع شوری به شکل گیری گردش اقیانوسی کمک می کند.
لیمنولوژیست ها و شیمیدانان اغلب شوری را بر حسب جرم نمک در واحد حجم تعریف می کنند که بر حسب واحد میلی گرم در لیتر یا گرم در لیتر بیان می شود. [7] به طور ضمنی، اگرچه اغلب بیان نمی شود، این مقدار فقط در برخی از دمای مرجع اعمال می شود زیرا حجم محلول با دما تغییر می کند. مقادیر ارائه شده به این روش معمولاً به ترتیب 1٪ دقیق هستند. Limnologists همچنین از هدایت الکتریکی یا "رسانایی مرجع" به عنوان نماینده ای برای شوری استفاده می کنند. این اندازهگیری ممکن است برای اثرات دما تصحیح شود و معمولاً در واحد میکرو S/cm بیان میشود .
آب رودخانه یا دریاچه با شوری حدود 70 میلی گرم در لیتر معمولاً دارای رسانایی ویژه در دمای 25 درجه سانتیگراد بین 80 تا 130 μS/cm است. نسبت واقعی به یون های موجود بستگی دارد. [14] رسانایی واقعی معمولاً حدود 2٪ در هر درجه سانتیگراد تغییر می کند، بنابراین رسانایی اندازه گیری شده در دمای 5 درجه سانتیگراد ممکن است فقط در محدوده 50-80 μS/cm باشد.
اندازه گیری چگالی مستقیم نیز برای تخمین شوری، به ویژه در دریاچه های بسیار شور استفاده می شود . [4] گاهی اوقات چگالی در یک دمای خاص به عنوان نماینده ای برای شوری استفاده می شود. در زمانهای دیگر، یک رابطه تجربی شوری / چگالی ایجاد شده برای یک آب خاص برای تخمین شوری نمونهها از یک چگالی اندازهگیری شده استفاده میشود.
آبهای دریایی، آبهای اقیانوس هستند که اصطلاح دیگری برای آن دریاهای euhaline هستند . شوری دریاهای اوهالین 30 تا 35 ‰ است. دریاها یا آب های شور دارای شوری در محدوده 0.5 تا 29 ‰ و دریاهای متاهلین از 36 تا 40 ‰ هستند. همه این آبها تالاسیک در نظر گرفته میشوند ، زیرا شوری آنها از اقیانوس گرفته میشود و اگر شوری در طول زمان زیاد تغییر نکند (در اصل ثابت) به عنوان همیوهالین تعریف میشود. جدول سمت راست، اصلاح شده از Por (1972)، [15] [16] از "سیستم ونیز" (1959) پیروی می کند. [17]
در مقابل محیطهای همیوهالین، محیطهای پویکیلوهالین خاصی (که ممکن است تالاسیک نیز باشند ) هستند که در آنها تنوع شوری از نظر بیولوژیکی قابل توجه است. [18] شوری آب Poikilohaline ممکن است از 0.5 تا بیش از 300 ‰ باشد. ویژگی مهم این است که این آب ها تمایل به تغییر در شوری در برخی محدوده های بیولوژیکی معنی دار به صورت فصلی یا در برخی مقیاس های زمانی تقریباً مشابه دیگر دارند. به زبان ساده، اینها توده های آبی با شوری کاملاً متغیر هستند.
آب بسیار شور که نمکها از آن متبلور میشوند (یا در شرف کریستال شدن هستند)، آب نمک نامیده میشوند .
شوری یک عامل اکولوژیکی از اهمیت قابل توجهی است که بر انواع موجوداتی که در یک بدن آب زندگی می کنند تأثیر می گذارد. همچنین، شوری بر انواع گیاهانی که در یک بدنه آبی یا در زمینی که از آب (یا از آب زیرزمینی ) تغذیه میشود، رشد میکنند. [19] گیاهی که با شرایط شور سازگار است، هالوفیت نامیده می شود . هالوفیت هایی که نسبت به شوری کربنات سدیم باقیمانده متحمل هستند ، گیاهان گلاسه یا شوره یا باریلا نامیده می شوند . ارگانیسم ها (بیشتر باکتری ها) که می توانند در شرایط بسیار شور زندگی کنند، به عنوان اکسترموفیل ها یا هالوفیل ها طبقه بندی می شوند . ارگانیسمی که می تواند طیف وسیعی از شوری ها را تحمل کند یوریهالین است .
حذف نمک ها از آب پرهزینه است و میزان نمک عامل مهمی در استفاده از آب است که باعث شرب و مناسب بودن برای آبیاری می شود . افزایش شوری در دریاچه ها و رودخانه ها در ایالات متحده مشاهده شده است که به دلیل نمک معمولی جاده و سایر نمک زدا کننده های نمک در رواناب است. [20]
درجه شوری در اقیانوس ها محرک گردش اقیانوس جهان است که در آن تغییرات چگالی به دلیل تغییرات شوری و تغییرات دما در سطح اقیانوس باعث ایجاد تغییراتی در شناوری می شود که باعث غرق شدن و بالا آمدن توده های آب می شود. تصور میشود که تغییرات در شوری اقیانوسها به تغییرات جهانی در دیاکسید کربن کمک میکند، زیرا آبهای شور بیشتر محلول کمتری در کربن دیاکسید هستند. علاوه بر این، در دوره های یخبندان، هیدروگرافی به گونه ای است که یکی از دلایل احتمالی کاهش گردش خون، تولید اقیانوس های طبقه بندی شده است. در چنین مواردی، فرورانش آب از طریق گردش ترموهالین دشوارتر است.
شوری نه تنها محرک گردش اقیانوس است، بلکه تغییرات در گردش اقیانوس نیز بر شوری تأثیر می گذارد، به ویژه در اقیانوس اطلس شمالی زیرقطبی که در آن از سال 1990 تا 2010 افزایش مشارکت آب ذوب گرینلند با افزایش انتقال آب های شور اقیانوس اطلس به سمت شمال خنثی شد. [13] [21] [22] [23] با این حال، آبهای اقیانوس اطلس شمالی از اواسط دهه 2010 به دلیل افزایش جریان آب ذوب گرینلند شیرینتر شدهاند. [13] [24]
{{cite book}}: CS1 maint: چندین نام: فهرست نویسندگان ( پیوند ){{cite web}}: CS1 maint: چندین نام: فهرست نویسندگان ( پیوند )